






- 2.2氯及其化合物(第三课时)课件+教案+练习 课件 86 次下载
- 2.3物质的量(第一课时)课件+教案+练习 课件 84 次下载
- 2.3物质的量(第三课时)课件+教案+练习 课件 82 次下载
- 3.1铁及其化合物(第一课时)课件+教案+练习 课件 80 次下载
- 3.1铁及其化合物(第二课时)课件+教案+练习 课件 84 次下载
高中人教版 (2019)第二章 海水中的重要元素——钠和氯第三节 物质的量说课课件ppt
展开一、新课导入二、探究气体体积与粒子数之间的关系 (知识点1:影响物质体积大小的因素)三、探究气体体积与物质的量之间的关系 (知识点2:气体摩尔体积)四、探究不同温度、压强下的气体摩尔体积(知识点3)五、阿伏伽德罗定律及其推论
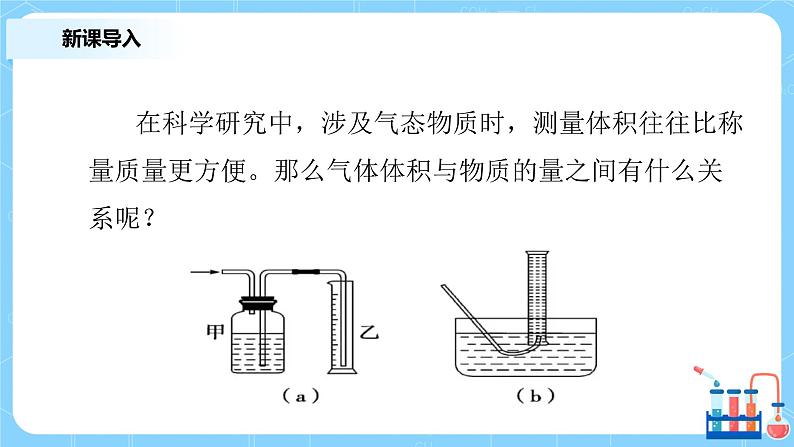
在科学研究中,涉及气态物质时,测量体积往往比称量质量更方便。那么气体体积与物质的量之间有什么关系呢?
但实际生活中,气体一般用体积表示。
任务一 探究气体体积与粒子数的关系
请思考在0℃、101kPa下: 22.4L氢气含______个H2分子 44.8L氢气含______个H2分子
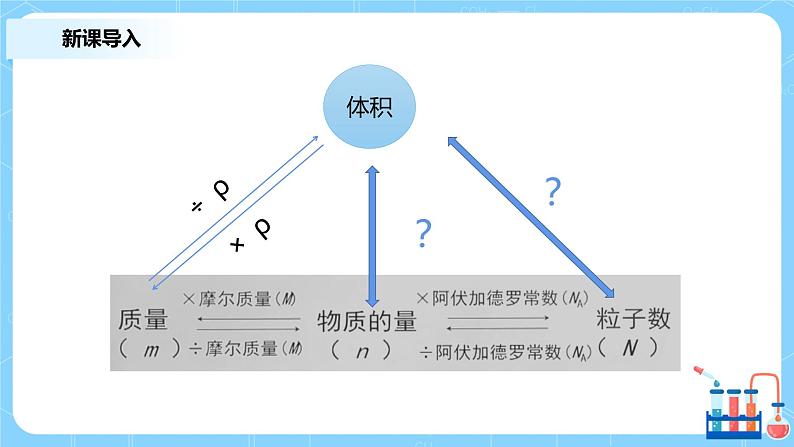
思路一: 气体总体积 ÷ 每个分子的体积 = 粒子数思路二: V × ρ = m n × NA = 粒子数
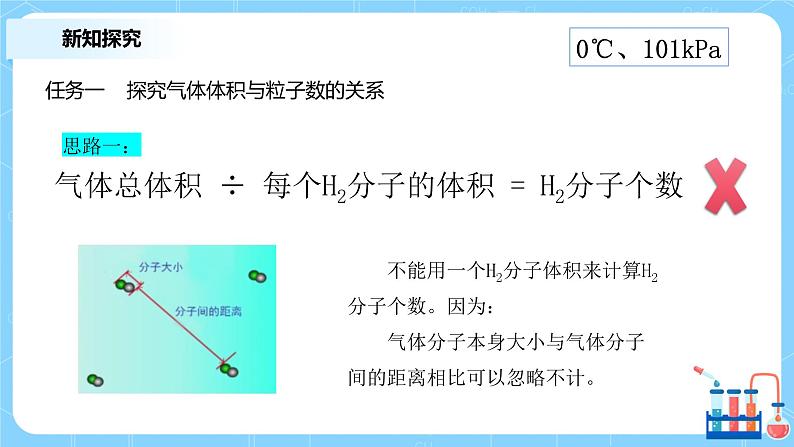
气体总体积 ÷ 每个H2分子的体积 = H2分子个数
不能用一个H2分子体积来计算H2分子个数。因为: 气体分子本身大小与气体分子间的距离相比可以忽略不计。
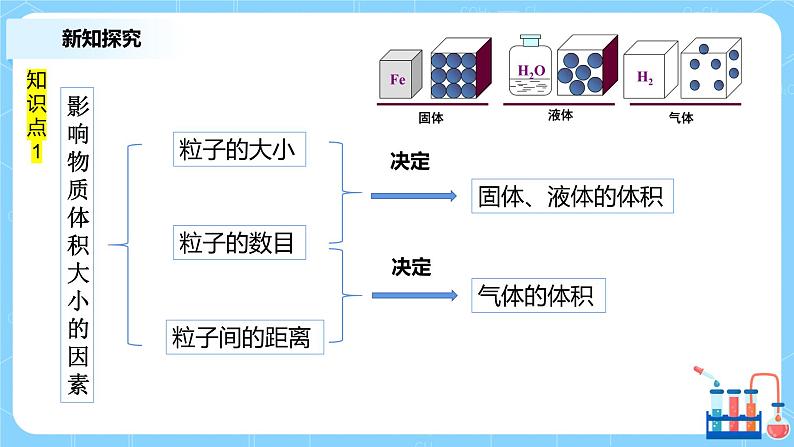
影响物质体积大小的因素
成正比关系,且都为1:22.4
请思考以下1ml不同种气体的体积:
任务二 探究气体体积与物质的量之间的关系
知识点2 气体摩尔体积
任务四 探究不同温度、压强下的气体摩尔体积
判断下列正误:(1)标准状况下,1ml任何物质的体积都约为22.4L。 (2)1ml气体的体积约为22.4L。 (3)标准状况下,1 ml的O2和N2混合气(任意比),其体积约为22.4L。(4) 22.4L气体所含分子数一定大于11.2L气体所含的分子数。
错误,未指明气体体积是否在相同温度和压强下测定的。
3.设NA为阿伏加德罗常数的值。下列叙述正确的是( ) A.18g冰水混合物中有NA个原子和10NA个电子 B.常温常压下16gO2和O3混合气体含有NA个氧原子 C.标准状况下,33.6L水含有1.5NA个水分子 中含有0.3NA个原子
解析: 冰水混合物为纯净物,18g冰水混合物所含水的物质的量为1ml,则含有的原子数为3NA,含有电子数为10NA。 O2和O3均由O原子构成,故16g混合物中含有的氧原子的物质的量=16g/16g⋅ml−1=1ml。故含氧原子为NA个。 标准状况下,水为液体,故不能根据标准状况下的气体摩尔体积来计算其物质的量。 没有指明是否为标准状况下,则气体摩尔体积未知,故无法计算2.24LCO2含有的原子数。
4.设NA为阿伏加德罗常数的值。下列叙述正确的是( ) A.标准状况下,22.4LH2O含有的分子数目为NA. B.标准状况下,11.2LHe(氦气)含有的分子数目为NA C.常温常压下,48gO3中含有的氧原子数目为3NA D.44gCO2所占的体积约为22.4L
解析:标准状况下,H2O不是气体,故不能运用22.4L/ml进行计算,A错误;标准状况下,11.2LHe的物质的量为0.5ml,分子数目为0.5NA,B错误;48 gO3中含有O原子的物质的量 =48g/16g·ml−1= 3ml,因此含有的氧原子数目为3NA,C正确;未指明气体是否处于标准状况下,故不能确定44gCO2所占的体积,D错误。
阿伏伽德罗定律及其推论
(1)定律 : ①内容:同温同压下,相同体积的任何气体都含有相同的分子数。 ②适用范围;任何气体(单一气体或混合气体)。(2)推论:阿伏加德罗定律的几个推论均可由理想气体状态方程PV=nRT推出,式中R为一常数。
所含原子数不一定相等。如Ne、H2、NH3等
例题:下列关于同温同压下的两种气体12C18O和14N2的判断正确的是( ) A.体积相等时密度相等 B.原子数相等时具有的中子数相等 C.体积相等时具有的电子数相等 D.质量相等时具有的质子数相等
解析:PV=nRT。同温同压下,相同体积的任何气体都含有相同的分子数。
同温同压,同体积下:密度之比=摩尔质量之比
n = m/M ,m同,M不同,则n不同
1个12C18O分子中有16个中子,1个14N2中中子数为14.
请思考: 在生成和科学实验中,我们常常要用到溶液,一般我们不是称量它们的质量,而是量取它们的体积。那么,液体体积与物质的量有什么关系呢?
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量优质ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量优质ppt课件,共60页。PPT课件主要包含了物质的量的单位,物质的量的简单计算等内容,欢迎下载使用。
高中第三节 物质的量优秀ppt课件: 这是一份高中第三节 物质的量优秀ppt课件,共48页。PPT课件主要包含了酒精的度数,物质的量浓度及计算,物质的量浓度,物质的量浓度计算,cK+,mol·L-1,还有什么疑问,课堂小结等内容,欢迎下载使用。
人教版 (2019)必修 第一册第三节 物质的量优秀ppt课件: 这是一份人教版 (2019)必修 第一册第三节 物质的量优秀ppt课件,共27页。PPT课件主要包含了物质的量考点,看谁做得既准又快,数字+mol+化学式,两概念,牛刀小试,成功体验,2四计算,N=n×NA,02×1019,你学会了吗等内容,欢迎下载使用。














