衡水金卷先享题考前悟题——化学
展开
这是一份衡水金卷先享题考前悟题——化学,共5页。
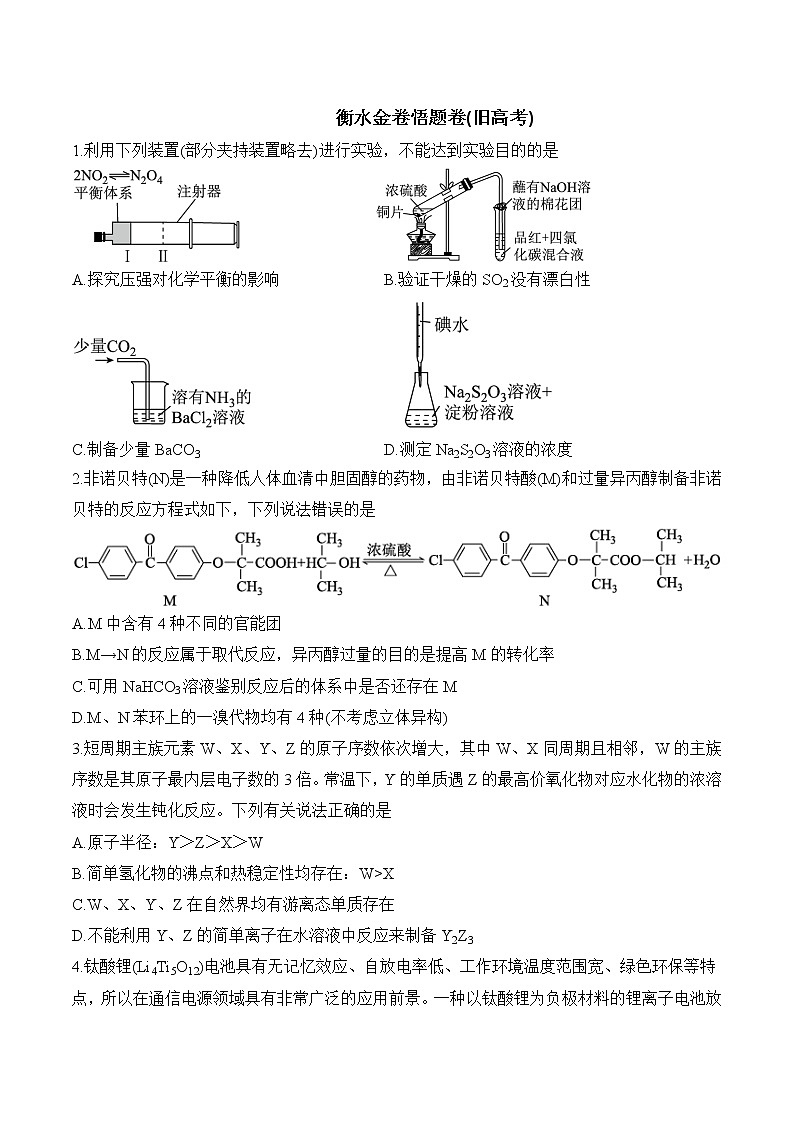
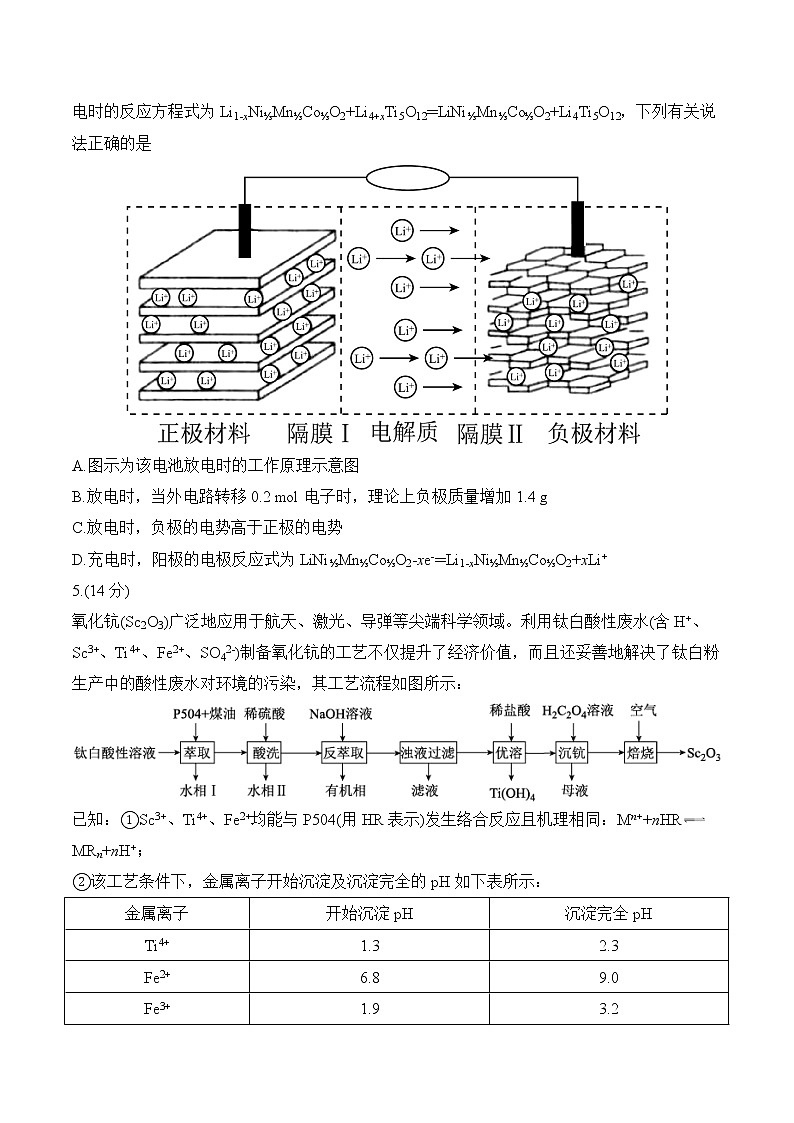
衡水金卷悟题卷(旧高考)1.利用下列装置(部分夹持装置略去)进行实验,不能达到实验目的的是 A.探究压强对化学平衡的影响 B.验证干燥的SO2没有漂白性 C.制备少量BaCO3 D.测定Na2S2O3溶液的浓度2.非诺贝特(N)是一种降低人体血清中胆固醇的药物,由非诺贝特酸(M)和过量异丙醇制备非诺贝特的反应方程式如下,下列说法错误的是A.M中含有4种不同的官能团B.M→N的反应属于取代反应,异丙醇过量的目的是提高M的转化率C.可用NaHCO3溶液鉴别反应后的体系中是否还存在MD.M、N苯环上的一溴代物均有4种(不考虑立体异构)3.短周期主族元素W、X、Y、Z的原子序数依次增大,其中W、X同周期且相邻,W的主族序数是其原子最内层电子数的3倍。常温下,Y的单质遇Z的最高价氧化物对应水化物的浓溶液时会发生钝化反应。下列有关说法正确的是A.原子半径:Y>Z>X>WB.简单氢化物的沸点和热稳定性均存在:W>XC.W、X、Y、Z在自然界均有游离态单质存在D.不能利用Y、Z的简单离子在水溶液中反应来制备Y2Z34.钛酸锂(Li4Ti5O12)电池具有无记忆效应、自放电率低、工作环境温度范围宽、绿色环保等特点,所以在通信电源领域具有非常广泛的应用前景。一种以钛酸锂为负极材料的锂离子电池放电时的反应方程式为Li1-xNi⅓Mn⅓Co⅓O2+Li4+xTi5O12═LiNi⅓Mn⅓Co⅓O2+Li4Ti5O12,下列有关说法正确的是A.图示为该电池放电时的工作原理示意图B.放电时,当外电路转移0.2 mol电子时,理论上负极质量增加1.4 gC.放电时,负极的电势高于正极的电势D.充电时,阳极的电极反应式为LiNi⅓Mn⅓Co⅓O2-xe-═Li1-xNi⅓Mn⅓Co⅓O2+xLi+5.(14分)氧化钪(Sc2O3)广泛地应用于航天、激光、导弹等尖端科学领域。利用钛白酸性废水(含H+、Sc3+、Ti4+、Fe2+、SO42-)制备氧化钪的工艺不仅提升了经济价值,而且还妥善地解决了钛白粉生产中的酸性废水对环境的污染,其工艺流程如图所示:已知:①Sc3+、Ti4+、Fe2+均能与P504(用HR表示)发生络合反应且机理相同:Mn++nHRMRn+nH+;②该工艺条件下,金属离子开始沉淀及沉淀完全的pH如下表所示:金属离子开始沉淀pH沉淀完全pHTi4+1.32.3Fe2+6.89.0Fe3+1.93.2Sc3+4.05.0回答下列问题:(1)萃取相比(O/W)指的是萃取时有机相与被萃取的酸性废水的体积比。“萃取”工序中萃取相比与Sc3+的萃取率如下表所示:萃取相比(O/W)1∶101∶151∶201∶251∶301∶351∶40Sc3+的萃取率/%95959583756258则该工序中应选择的适宜O/W是 ,O/W高于此值的缺点是 。(2)水相Ⅱ的主要成分为FeSO4和少量Ti(SO4)2,则Sc3+、Ti4+、Fe2+三种离子中与P504络合能力最强的是 (填离子符号),其络合机理为 (用离子方程式表示)。(3)“反萃取”工序中加入NaOH溶液的目的为 ,“浊液过滤”工序中所得滤液中溶质的主要成分为 (填化学式)。(4)“优溶”工序中加入盐酸时应调节溶液的pH范围为 。(5)“沉钪”工序中得到的Sc2(C2O4)3·6H2O在“焙烧”工序中反应时,焙烧温度区间和其得到的固体产物如下表所示:草酸钪络盐焙烧温度区间(K)固体失重百分率(%)生成的含钪化合物Sc2(C2O4)3·6H2O(摩尔质量为462 g/mol)383~42319.48A463~50823.38B583~87370.13C化合物A的化学式为 ,由B生成C的化学方程式为 。参考答案及解析1.D【解析】通过拉伸或推进注射器活塞可探究压强对化学平衡的影响,A项正确;通过制备得到的SO2不能使品红+四氯化碳混合液褪色的实验现象,可验证干燥的SO2没有漂白性,B项正确;溶有NH3的BaCl2溶液呈碱性,通入少量CO2可制得BaCO3,C项正确;碘水应装在酸式滴定管中,D项错误。2.C【解析】M中含有的官能团有氯原子、羰基、醚键、羧基,共4种,A项正确;M→N的反应属于酯化反应,酯化反应属于取代反应,异丙醇过量的目的是提高M的转化率,B项正确;浓硫酸和M均能与NaHCO3溶液反应放出气体,故不能用NaHCO3溶液鉴别反应后的体系中是否还存在M,C项错误;由M、N的结构可知,二者苯环上的一溴代物均有4种,D项正确。3.D【解析】由题给信息可推知,W、X、Y、Z分别为O、F、Al、S。原子半径:Al>S>O>F,A项错误;H2O的沸点高于HF,但HF的热稳定性更好,B项错误;铝元素和氟元素在自然界中不存在游离态的单质,C项错误;在水溶液中Al3+、S2-相遇会发生相互促进的水解反应,生成Al(OH)3沉淀和H2S气体,D项正确。4.D【解析】由Li+移动方向可知,题给图示为该电池充电时的工作原理示意图,A项错误;放电时,负极的电极反应式为Li4+xTi5O12-xe-═Li4Ti5O12+xLi+,负极质量减小,B项错误;放电时,负极的电势低于正极的电势,C项错误;充电时,左侧电极为阳极,电极反应式为LiNi⅓Mn⅓Co⅓O2-xe-═Li1-xNi⅓Mn⅓Co⅓O2+xLi+,D项正确。5.(14分)(1)1∶20(1分) 萃取剂使用量大,增大生产成本(1分,其他合理答案也给分)(2)Sc3+(2分) Sc3++3HRScR3+3H+(1分)(3)将ScR3、TiR4转化为不溶于P504有机相的Sc(OH)3和Ti(OH)4(2分) NaR(1分)(4)2.3≤pH<4.0(2分)(5)Sc2(C2O4)3·H2O(2分) 2Sc2(C2O4)3+3O22Sc2O3+12CO2(2分)【解析】(1)由表中数据可知,O/W小于1∶20,Sc3+的萃取率低;当O/W大于等于1∶20,Sc3+的萃取率相同,但有机相使用量大,增大生产成本,因此“萃取”工序中应选择的适宜O/W是1∶20。(2)由已知①可知,Sc3+、Ti4+、Fe2+三种离子均能与HR发生络合反应,Sc3+的络合机理为Sc3++3HRScR3+3H+;由水相Ⅱ的主要成分为FeSO4和少量Ti(SO4)2 可知,“酸洗”工序是将FeR2和部分TiR4从有机相中去除,故与P504络合能力最强的离子是Sc3+。(3)结合后续的工序可知,“反萃取”工序中加入NaOH溶液的目的为将ScR3、TiR4转化为不溶于P504有机相的Sc(OH)3和Ti(OH)4 ;“浊液过滤”工序中所得滤液中溶质的主要成分为NaR。(4)“优溶”工序中加入稀盐酸的目的是调节溶液的pH使Sc(OH)3溶解,但不能使Ti(OH)4溶解,由已知②可知,应调节溶液的pH范围为2.3≤pH<4.0。(5)根据题给表格数据可知,Sc2(C2O4)3·6H2O的相对分子质量为462,设初始有1 mol Sc2(C2O4)3·6H2O,在383~423 K时失重率为19.48%,失重质量为462 g×19.48%≈90 g,即失去了5 mol H2O,则化合物A的化学式为Sc2(C2O4)3·H2O;在463~508 K时失重率为23.38%,失重质量为462 g×23.38%≈108 g,即失去了6 mol H2O,则化合物B的化学式为Sc2(C2O4)3;在583~873 K时失重率为70.13%,失重质量为462 g×70.13%≈324 g,剩余质量为2 mol Sc和3 mol O的质量之和,则化合物C的化学式为Sc2O3,故由B生成C的化学方程式为2Sc2(C2O4)3+3O22Sc2O3+12CO2。
相关试卷
这是一份衡水金卷先享题考前悟题——新教材新高考化学考前悟题,共4页。试卷主要包含了旧高考考前悟题第3题,旧高考考前悟题第4题,5 kJ·ml-1;,01 ml CO2和0,3 kJ·ml-1等内容,欢迎下载使用。
这是一份2023新高考化学【衡水金卷·先享题·信息卷】模拟试题(辽宁卷)06,文件包含39171139_2023新高考化学衡水金卷·先享题·信息卷模拟试题辽宁卷06pdf、39171139_2023新高考化学衡水金卷·先享题·信息卷模拟试题辽宁卷06答案pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
这是一份2023新高考化学【衡水金卷·先享题·信息卷】模拟试题(辽宁卷)04,文件包含39171137_2023新高考化学衡水金卷·先享题·信息卷模拟试题辽宁卷04pdf、39171137_2023新高考化学衡水金卷·先享题·信息卷模拟试题辽宁卷04答案pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。









