





2022年中考化学一轮复习 微专题06 解密工艺流程题
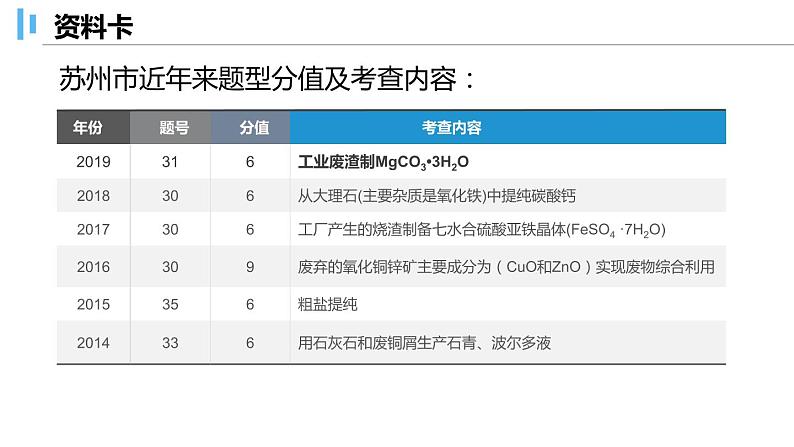
展开苏州市近年来题型分值及考查内容:
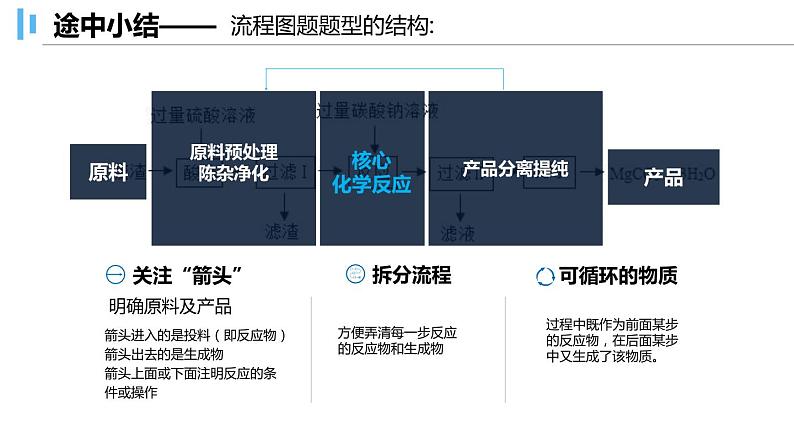
例1.(2019•苏州)实验室以一种工业废渣(主要成分为MgCO3、MgO和SiO2)为原料制备MgCO3•3H2O.其主要实验过程如图:
已知:SiO2不溶于水,常温下不与硫酸、碳酸钠反应。
(1)“酸溶”时发生反应的化学方程式为 和 。(2)“过滤Ⅱ”所得滤液中含有的主要离子有 (填离子符号)。(3)“反应”步骤前后均有过滤,能否省去“过滤Ⅰ”只进行“过滤Ⅱ”。 (填“能”或“否”),理由是 。(4)“酸溶”时所加硫酸溶液不宜过量太多的原因是 。
MgO+H2SO4=MgSO4+H2O
MgCO3+H2SO4=MgSO4+H2O+CO2↑
Na+、SO42−、CO32−
避免制备产品消耗更多的碳酸钠
例2.(2017.苏州)某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4 ·7H2O),其工艺流程如下:
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式分别为 FeO+H2SO4=FeSO4+ H2O 、 。(2)为提高“浸取”步骤的反应速率,可采取的具体措施有______________、 (写2条,不考虑“搅拌”和 “使用催化剂”)。
Fe2O3 +3H2SO4=Fe2 (SO4)3+3H2O
(3)“还原”步骤的日的是将Fe抖转化为Fe2+,试剂X可用SO2或Fe。 ① 若试剂X是SO2,转化原理为SO2+Fe2 (SO4)3+2Y =2FeSO4+2H2SO4, 则Y的化学式是_________。 ② 若试剂X是Fe,转化原理为Fe+Fe2 (SO4)3=3FeSO4。测得“还原”后溶液 的pH明显增大,其原因是 。
铁消耗过量的硫酸,溶液酸性减弱
流程图题答题的那点儿套路
流程中所用的原料通常要进行预处理,如研磨、水浸、酸或碱浸、灼烧等。
增大物质间的接触面积,使反应(或溶解)快速充分进行
通过加水溶解,使可溶物进入溶液,与不溶物通过过滤分离
RAW MATERIL PRETREATMENT
通过加酸或碱溶液,使物质发生化学反应而溶解,与不溶物通过过滤分离
硅酸钠( Na2SiO3 )是我国优先发展的精细化学品。用某种石英砂矿石( 主要成分是SiO2 ,还含有少量的CuO、Na2SO4、Na2CO3 )制备硅酸钠( Na2SiO3 )的流程如下:
资料: SiO,既不溶于水,也不与盐酸反应。请问答下列问题:(1)“研磨”的目的是 。(2)检验“洗涤a”已洗净的方法 。
增大接触面积,使反应或溶解快速充分
为了提高“浸取”步骤的反应速率 ,可采取的措施
(2017.苏州)某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备七水合硫酸亚铁晶体(FeSO4 ·7H2O),其工艺流程如下:
根据信息书写流程中的化学方程式
WRITING EQUATIONS
若用已知物书写的方程式配不平,可根据反应物或生成物一方所缺的原子(通常是氧原子或氢、氧原子) , 考虑添加氧气或水
辨箭头判断反应物和生成物
箭头由物质指向方框(设备或步骤)的是反应物,箭头离开方框指向的物质是生成物。
根据元素守恒与反应规律
CONTROL OF CONDITIONS
控制溶液的酸碱度,使(或避免某些反应的发生;在一定pH范围内 ,使某些金属离子开始沉淀或者沉淀完全
通常防止某种物质温度过高时会分解(如碳酸氢铵、双氧水、不溶性碱等)、挥发(如浓盐酸)、熔化等;防止某种副反应的发生
某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)。
在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见表。为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为是 ;
6.7 ≤ pH < 8.6
UTILIZATION OF RAW MATERIALS
作为反应物参与流程反应,又在后面的反应中生成的物质;有箭头回转指向前面方框的即是可循环利用的物质;不一定都有箭头显示,需根据具体反应判断
为了增大原料转化率,工业流程中所用的试剂往往过量,要注意过量的试剂留在了滤液还是滤渣里,回答物质成分时不要漏写
有些副产品在农业生产中可作肥料
粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯。实验中,为把少量可溶性杂质CaCl2、MgCl2一并除去,实验方案设计如下,请据此回答问题。
(1)Ca(OH)2溶液的pH (填“>”、“=”或“<”)7。步骤①反应的化学方 程式为 。(2)步骤③操作a的名称是 。步骤④加入适量盐酸的目的是除去滤液中的 Na2CO3和 。
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有 。
氯化亚铜(CuCI)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCI的制备流程如下:
(3)“操作a’的名称是 。本流程中可以循环利用的物质(水除外)是 (写化学式)
(2018.苏州)从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下:
(1)反应池I中用硝酸不用稀硫酸的主要原因是 ;(2)反应池II中加入氨水的日的是 ;(3)反应池II生成碳酸钙的化学方程式是 ;(4)过滤II中所得滤液在农业生产中的一种用途是 。
流程中少不了的分离、提纯等操作
OPERATIONS INVOLVED
如果溶液中的溶质只有一种,通过蒸发获得晶体的操作即:蒸发结晶如果溶液中的溶质不止一种,需要通过蒸发结晶获得其中一种溶质,其操作步骤是:蒸发结晶一→趁热过滤
当看到由方框中引出固体与液体两路物质,必然是经过了过滤操作
由于流程中获得的溶液通常是常温时的不饱和溶液,若要进行降温结晶操作,则操作步骤是:
蒸发浓缩→降温结晶→过滤→洗涤、干燥
资料: SiO,既不溶于水,也不与盐酸反应。(3)“酸浸“的化学方程式为 。(4)“碱浸"的化学方程式为 。(5)“操作a”包含蒸发浓缩、 、过滤、洗涤、干燥等一系列操作。
洗涤:通常有水洗、冰水洗涤、醇洗、饱和溶液洗
洗去固体表面残留溶液中的杂质,减少晶体在洗涤过程中的溶解损耗(适用于温度高时溶解度明显增大的固体)
洗去固体表面残留溶液中的杂质(适用于常温时溶解度小的固体)
洗去固体表面残留溶液中的杂质,减少晶体在洗涤过程中的溶解损耗(适用于常温时溶解度较大的固体)
洗去固体表面残留溶液中的杂质,减少晶体在洗涤过程中的溶解损耗。若物质在潮湿环境中易变质:可水洗后醇洗,目的是:使晶体快速干燥,避免在潮湿环境中变质
(3)“操作a’的名称是 。本流程中可以循环利用的物质(水除外)是 (写化学式)(4)不用“水洗”的而用是“醇洗”的原因是 。
快速除去水分,防止氧化变质
INSPECTION OF SUBSTANCES
首先要判断晶体表面残留溶液里的溶质成分,再根据其性质选择适当的试剂检验。由于洗涤液中物质浓度低,应该选用较灵敏的特征反应,如产生不溶性的沉淀.检验方法:
检验流程中沉淀是否完全
静置,往,上层清液中继续滴加某种试剂(与前面所加试剂相同) , 若没有沉淀产生,说明沉淀完全(或所加试剂足量)
(或所加试剂是否足量)
取最后一次洗涤液,滴加某种溶液,
若无明显现象,说明洗涤干净
资料: SiO,既不溶于水,也不与盐酸反应。请问答下列问题:(1)“研磨”的目的是 。(2)检验“洗涤a”已洗净的方法 。
取最后一-次洗涤液少许于试管中,滴入氯化钡溶液,若无明显现象,则沉淀已洗净
中考化学复习专题突破三工艺流程题教学课件: 这是一份中考化学复习专题突破三工艺流程题教学课件,共34页。PPT课件主要包含了HCl,Mg2+,置换反应,除去B中的MgO,复分解反应,作氮肥合理即可,复分解,稀硫酸,SiO2,H2O等内容,欢迎下载使用。
中考化学复习专题二工艺流程题课件: 这是一份中考化学复习专题二工艺流程题课件,共40页。PPT课件主要包含了专题二工艺流程题,回答下列问题,置换反应,CaOH2,NH4Cl,复分解反应,7~91,CaCl2,铁架台带铁圈,Fe+等内容,欢迎下载使用。
初中化学中考复习 微专题05解密推断题-2022年中考化学一轮复习【微专题突破】精品课件: 这是一份初中化学中考复习 微专题05解密推断题-2022年中考化学一轮复习【微专题突破】精品课件,共20页。PPT课件主要包含了做题技巧,读懂题意,找突破口,顺藤摸瓜,各个击破,突破口,特征组成,H2O2,H2O,物质之最等内容,欢迎下载使用。












