2020-2021学年第二节 离子反应第1课时习题
展开请同学们认真完成 [练案3]
一、选择题(每小题只有一个选项符合题意)
1.下列物质中,含有自由移动的Cl-的是( B )
A.KClO3溶液 B.CaCl2溶液
C.KCl晶体D.液态氯化氢
解析:A中KClO3溶于水电离出K+和ClOeq \\al(-,3);B中CaCl2溶于水电离出Ca2+和Cl-;C中KCl晶体不发生电离;D中液态HCl不发生电离。
2.下表是常见的几种酸、碱、盐在水溶液中电离出离子的情况,根据表中信息分析正确的是( B )
A.在水溶液中电离出H+的物质一定是酸
B.在水溶液中电离出金属阳离子和酸根阴离子的物质一定是盐
C.盐在溶液中电离出来的阳离子一定是金属阳离子
D.碱在溶液中电离出的离子一定是金属阳离子和OH-
解析:NaHSO4属于盐,在水溶液中电离出来的离子有H+,但不属于酸,A错误;盐由金属阳离子(或铵根离子)和酸根阴离子构成,则在水溶液中电离出金属阳离子和酸根阴离子的物质一定是盐,B正确;NH4Cl在溶液中电离出来的阳离子为NHeq \\al(+,4),而不是金属阳离子,C错误;NH3·H2O属于碱,在溶液中电离出的阳离子是NHeq \\al(+,4),不是金属阳离子,D错误。
二、选择题(每小题有1个或2个选项符合题意)
3.下列关于电解质溶液的叙述正确的是( AB )
A.阳离子和阴离子总数不一定相等
B.阳离子带的正电荷总数和阴离子带的负电荷总数一定相等
C.除阴、阳离子外,溶液中不再含有其他粒子
D.NaCl溶液的导电性一定与KCl溶液的导电性相同
解析:依据溶液呈电中性可知,电解质溶液中阳离子带的正电荷总数与阴离子带的负电荷总数相等但阴、阳离子总数不一定相等,A正确、B正确;电解质溶液中,一定含有H2O分子,有的还含有电解质分子,C错误;NaCl和KCl两溶液中单位体积内自由移动的离子的数目未知,故无法比较其导电性强弱,D错误。
三、非选择题
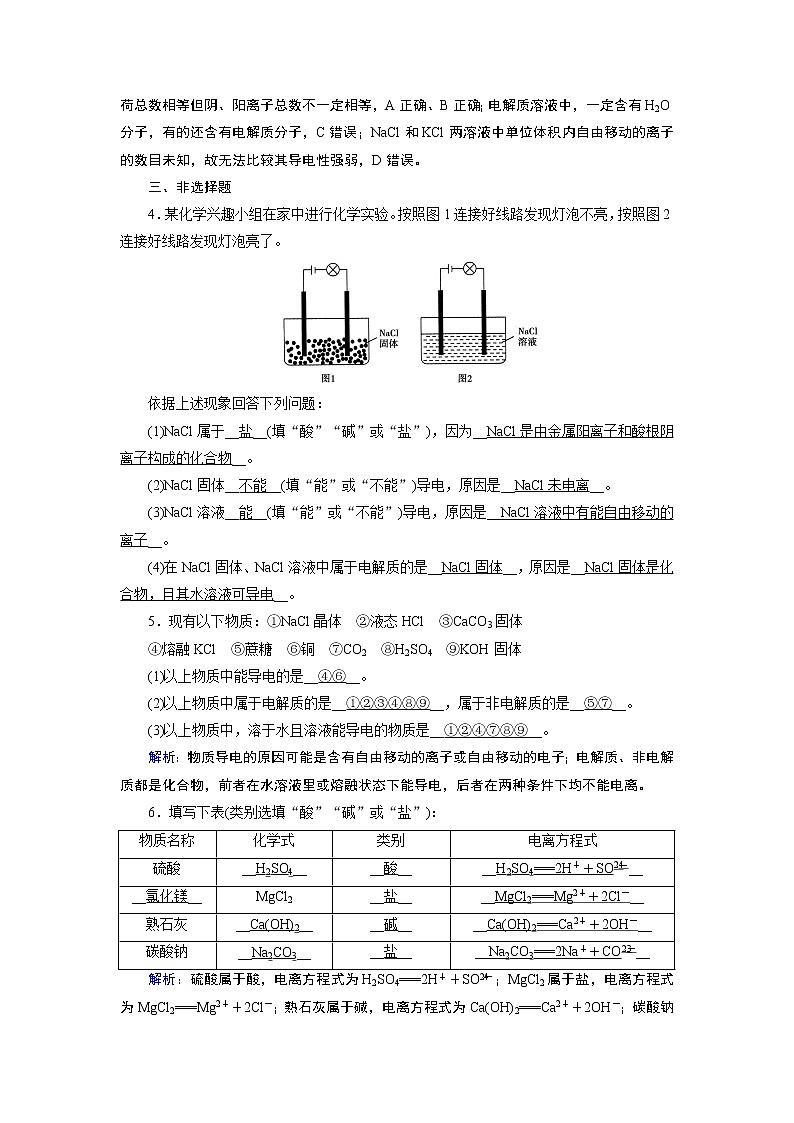
4.某化学兴趣小组在家中进行化学实验。按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮了。
依据上述现象回答下列问题:
(1)NaCl属于__盐__(填“酸”“碱”或“盐”),因为__NaCl是由金属阳离子和酸根阴离子构成的化合物__。
(2)NaCl固体__不能__(填“能”或“不能”)导电,原因是__NaCl未电离__。
(3)NaCl溶液__能__(填“能”或“不能”)导电,原因是__NaCl溶液中有能自由移动的离子__。
(4)在NaCl固体、NaCl溶液中属于电解质的是__NaCl固体__,原因是__NaCl固体是化合物,且其水溶液可导电__。
5.现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体
④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
(1)以上物质中能导电的是__④⑥__。
(2)以上物质中属于电解质的是__①②③④⑧⑨__,属于非电解质的是__⑤⑦__。
(3)以上物质中,溶于水且溶液能导电的物质是__①②④⑦⑧⑨__。
解析:物质导电的原因可能是含有自由移动的离子或自由移动的电子;电解质、非电解质都是化合物,前者在水溶液里或熔融状态下能导电,后者在两种条件下均不能电离。
6.填写下表(类别选填“酸”“碱”或“盐”):
解析:硫酸属于酸,电离方程式为H2SO4===2H++SOeq \\al(2-,4);MgCl2属于盐,电离方程式为MgCl2===Mg2++2Cl-;熟石灰属于碱,电离方程式为Ca(OH)2===Ca2++2OH-;碳酸钠属于盐,电离方程式为Na2CO3===2Na++COeq \\al(2-,3)。
7.现有10种物质:①铜 ②稀硫酸 ③氯化氢 ④氨气 ⑤空气 ⑥二氧化碳 ⑦酒精 ⑧氯化钠 ⑨硫酸钡 ⑩氯气
按照下表中提示的信息,把符合左栏条件的物质的化学式或名称填入右栏相应的位置。
解析:题给10种物质中稀硫酸和空气属于混合物。HCl溶于水可电离出H+、Cl-,其水溶液能导电(但在熔融状态下不存在自由移动的离子,不导电),故HCl属于电解质。BaSO4是难溶性电解质。NH3、CO2的水溶液虽然能导电,但不是它们本身发生了电离,而是它们与水发生了反应,生成了电解质NH3·H2O和H2CO3,故它们属于非电解质。铜属于单质,不是化合物;稀硫酸是混合物,也不是化合物,故二者既不是电解质,也不是非电解质,但都能导电。
8.酸、碱、盐溶液能够导电,是因为这些物质溶于水时电离出自由移动的阴、阳离子。
(1)在酸的溶液里,酸根离子所带__负电荷__的总数等于酸电离时生成的__H+__的总数;在碱的溶液里,跟金属离子结合的__OH-__的总数等于这种金属离子所带__正电荷__的总数;在盐的溶液中,金属(或铵根)离子所带__正电荷__的总数等于酸根离子所带__负电荷__的总数。
(2)下列物质的电离方程式如下:
HClO4===H++ClOeq \\al(-,4);
Ba(OH)2===Ba2++2OH-;
Fe2(SO4)3===2Fe3++3SOeq \\al(2-,4);
KHSO4===K++H++SOeq \\al(2-,4)。
属于酸的物质为__HClO4__(写化学式,下同);属于碱的物质为__Ba(OH)2__;属于盐的物质为__Fe2(SO4)3、KHSO4__。
(3)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是__纯碱__。
②上述物质中既不是电解质也不是非电解质的是__盐酸__。依据是__盐酸是混合物,不是化合物__。
③写出纯碱的电离方程式:__Na2CO3===2Na++COeq \\al(2-,3)__。
解析:(1)溶液呈电中性,其中阴离子所带的负电荷总数等于阳离子所带的正电荷总数。(2)根据酸、碱、盐的概念判断。(3)纯碱是Na2CO3,属于盐,不是碱;盐酸是HCl的水溶液,是混合物,既不是电解质,也不是非电解质。Na2CO3的电离方程式为Na2CO3===2Na++COeq \\al(2-,3)。
溶质
酸
盐
碱
HCl
H2SO4
NaCl
NaHSO4
NH4Cl
NaOH
NH3·H2O
电离出的离子
H+、
Cl-
H+、
SOeq \\al(2-,4)
Na+、
Cl-
Na+、H+、
SOeq \\al(2-,4)
NHeq \\al(+,4)、
Cl-
Na+、
OH-
NHeq \\al(+,4)、
OH-
物质名称
化学式
类别
电离方程式
硫酸
__H2SO4__
__酸__
__H2SO4===2H++SOeq \\al(2-,4)__
__氯化镁__
MgCl2
__盐__
__MgCl2===Mg2++2Cl-__
熟石灰
__Ca(OH)2__
__碱__
__Ca(OH)2===Ca2++2OH-__
碳酸钠
__Na2CO3__
__盐__
__Na2CO3===2Na++COeq \\al(2-,3)__
序号
符合的条件
物质的化学式或名称
(1)
混合物
__②稀硫酸__⑤空气__
(2)
电解质,但熔融状态下并不导电
__③氯化氢__
(3)
电解质,但难溶于水
__⑨BaSO4__
*(4)
非电解质
__④NH3__⑥CO2__⑦酒精__
(5)
既不是电解质,也不是非电解质,但本身能导电
__①铜__②稀硫酸__
高中化学人教版 (2019)选择性必修3第二节 烯烃 炔烃第1课时一课一练: 这是一份高中化学人教版 (2019)选择性必修3第二节 烯烃 炔烃第1课时一课一练,共6页。
高中人教版 (2019)第四节 羧酸 羧酸衍生物第1课时课后练习题: 这是一份高中人教版 (2019)第四节 羧酸 羧酸衍生物第1课时课后练习题,共7页。试卷主要包含了关于乙酸的下列说法不正确的是,下列说法正确的是等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修3第二节 醇酚第1课时习题: 这是一份高中化学人教版 (2019)选择性必修3第二节 醇酚第1课时习题,共7页。试卷主要包含了下列说法中正确的是,乙醇分子中不同的化学键如图等内容,欢迎下载使用。













