

2021河南省九师联盟下学期高二6月联考化学含答案
展开www.ks5u.com九师联盟2020-2021学年下学期高二6月联考
化学
考生注意:
1.本试卷分第I卷(选择题)和第II卷(非选择题)两部分。满分100分,考试时间90分钟。
2.考生作答时,请将答案答在答题卡上。第I卷每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;第II卷请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 35.5 Fe 56 Cu 64 Ag 108
第I卷(选择题 共42分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的4个选项中,只有一项是符合题目要求的。
1.下列物质都曾用作制造口罩或面巾的材料,其中主要成分属于合成高分子化合物的是
A.丝 B.棉 C.聚丙烯 D.活性炭
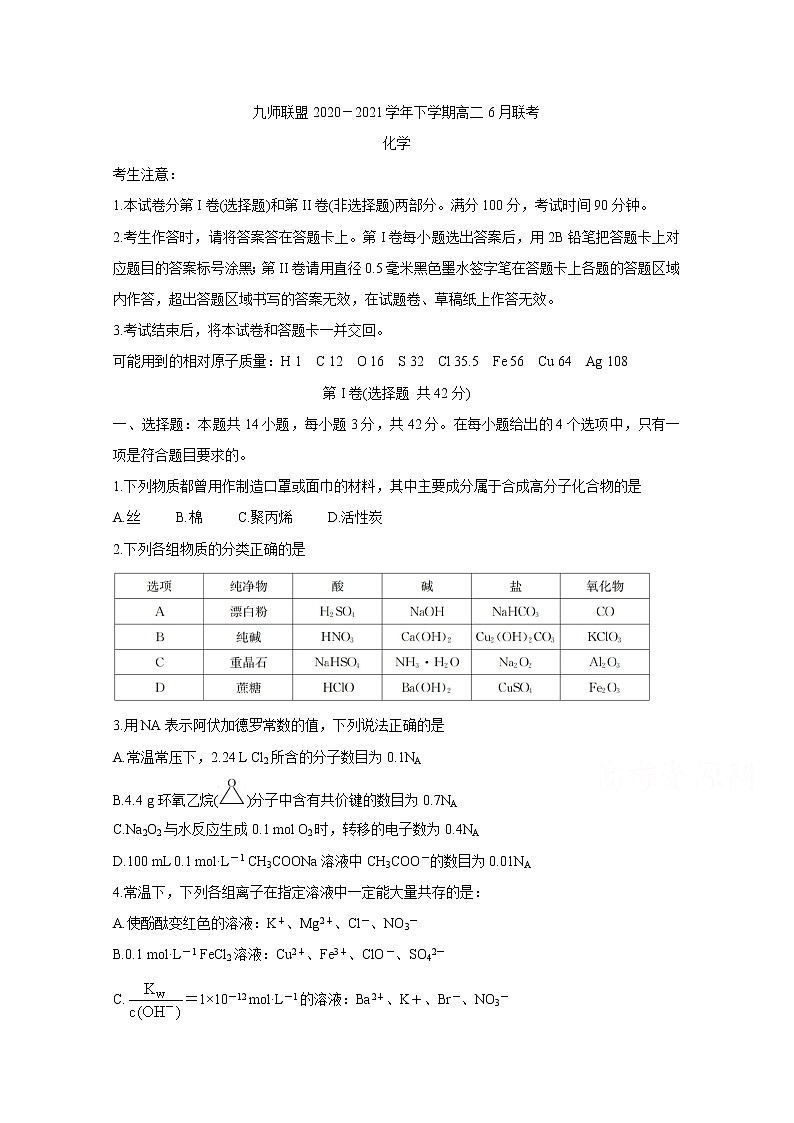
2.下列各组物质的分类正确的是
3.用NA表示阿伏加德罗常数的值,下列说法正确的是
A.常温常压下,2.24 L Cl2所含的分子数目为0.1NA
B.4.4 g环氧乙烷()分子中含有共价键的数目为0.7NA
C.Na2O2与水反应生成0.1 mol O2时,转移的电子数为0.4NA
D.100 mL 0.1 mol·L-1 CH3COONa溶液中CH3COO-的数目为0.01NA
4.常温下,下列各组离子在指定溶液中一定能大量共存的是:
A.使酚酞变红色的溶液:K+、Mg2+、Cl-、NO3-
B.0.1 mol·L-1 FeCl2溶液:Cu2+、Fe3+、ClO-、SO42-
C.=1×10-12 mol·L-1的溶液:Ba2+、K+、Br-、NO3-
D.由水电离出的c(H+)=1×10-13 mol·L-1的溶液:NH4+、Na+、HCO3-、Cl-
5.下列实验操作能达到实验目的的是
A.用装置甲制取Cl2 B.用装置乙除去CO2中的少量HCl
C.用装置丙收集NH3 D.用装置丁从MgCl2溶液中获得无水MgCl2
6.下列关于常见有机物的说法正确的是
A.用酸性KMnO4溶液除去甲烷中的乙烯
B.石油分馏时,得到的产品均为纯净物
C.乙醇、水均能与钠反应,且现象相同
D.在加热条件下,葡萄糖能与含氢氧化钠的氢氧化铜悬浊液发生反应
7.下列说法正确的是
A.铁制器具表面涂油,可防止其锈蚀
B.SO2使氯水褪色,证明SO2具有漂白性
C.在空气中蒸干FeSO4溶液可获得FeSO4固体
D.浓盐酸敞口放置浓度会降低,说明其具有吸水性
8.下列化学反应的离子方程式表示正确的是
A.向NaOH溶液中通入足量的CO2:CO2+2OH-=CO32-+H2O
B.向澄清石灰水中加入少量的NaHCO3:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
C.向KAl(SO4)2溶液中加入Ba(OH)2溶液至SO42-沉淀完全:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
D.向Fe(OH)3沉淀中滴加氢碘酸(HI的水溶液):Fe(OH)3+3H+=Fe3++3H2O
9.相比锂离子电池,钠离子电池具有原材料丰富、成本低、无过放电特性等优点。一种可充电钠离子电池的工作原理如右图所示(两电极材料均不溶于水,P为+5价),下列说法正确的是
A.放电过程中Ti元素的化合价由+4降低到+3
B.充放电过程中电解质溶液中c(Na+)基本保持不变
C.充电过程中Na+通过离子交换膜从右室移向左室
D.充电时阴极反应为Na2Cu[Fe(CN)6]-e-=NaCu[Fe(CN)6]+Na+
10.已知断裂1 mol化学键吸收的能量如下表所示:
则反应CH2=CH2(g)+H2(g)=C2H6(g)的△H为
A.+267 kJ·mol-1 B.-267 kJ·mol-1 C.+123 kJ·mol-1 D.-123 kJ·mol-1
11.短周期主族元素X、Y、Z、W的原子序数依次增大,X.Y同周期且相邻,Y是地壳中含量最多的元素,Z是短周期中原子半径最大的主族元素,W的单质常温下是一种淡黄色固体。下列叙述正确的是
A.元素的非金属性:X>Y>W
B.Z的单质在空气中燃烧生成阴、阳离子个数比为1:1的氧化物
C.Y的简单气态氢化物的稳定性强于W的
D.工业上一般采用电解对应盐的水溶液制Z单质
12.下列有关实验的现象和结论都正确,且二者具有因果关系的是
13.工业上可由苯和丙烯合成异丙苯:
下列说法错误的是
A.异丙苯分子中所有碳原子可能在同一平面内 B.异丙苯分子的一溴代物共有5种
C.可以用溴水鉴别异丙苯和丙烯 D.丙烯能发生加成反应、氧化反应
14.常温下,向20 mL 0.01 mol·L-1 H2C2O4溶液中滴加0.01 mol·L-1 NaOH溶液,混合溶液pH与所加NaOH溶液体积的关系如图所示。下列说法正确的是
A.a点溶液:c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-)
B.b点溶液:c(HC2O4-)>c(C2O42-)>c(H2C2O4)
C.c点溶液:c(Na+)=2[c(H2C2O4)+c(HC2O4-)+c(C2O42-)]
D.d点溶液中由水电离产生的c(H+)<1×10-7 mol·L-1
第II卷(非选择题 共58分)
二、非选择题:共58分。第15~17题为必考题,每个试题考生都必须作答,第18~19题为选考题,考生根据要求作答。
(一)必考题:共43分。
15.(14分)过氧化镁(MgO2)产品中常混有少量MgO,甲、乙两小组分别设计了两种实验方案
测定样品中过氧化镁的质量分数。
方案I:取一定量过氧化镁样品,加入少量的MnO2,搅拌使其充分混合,再向其中滴加足量的稀硫酸(如图1)。
方案II:称取0.1000 g样品置于碘量瓶中,加入足量KI溶液和稀硫酸,滴加几滴指示剂X,
摇匀后在暗处静置5min,然后用0.1000 mol·L-1 Na2S2O3的标准溶液滴定至终点(如图2),消耗Na2S2O3溶液30.00 mL。(已知:I2+2Na2S2O3=Na2S4O6+2NaI)
回答下列问题:
(1)方案I实验前检验气密性的方法是 。仪器a的名称是 ,使用该仪器的优点是 。
(2)广口瓶内发生的化学反应方程式为:MgO2+H2SO4=MgSO4+H2O2, 。
(3)方案II滴定过程中若操作过慢,导致结果 (填“偏高”“偏低”或“无影响”)。指示剂X为 ,判断到滴定终点的现象为 。
(4)根据方案II实验数据,样品中过氧化镁的质量分数为 。
l6.(15分)以镍黄铁矿为原料制备Ni(OH)2的工艺流程如下:
已知:①高镍锍的主要成分为Ni、Fe、Co、Cu的低价硫化物及合金;
②氧化性:Ni3+>Co3+>H2O2>Fe3+;
③Ksp[Ni(OH)2]=1×10-15,Ksp[Co(OH)2]=5×10-15,Ksp[Co(OH)3]=1×10-44。
回答下列问题:
(1)“酸浸”时,H2SO4溶液需过量,其目的是 。
(2)“氧化”时反应的化学方程式为 ,若用NaClO代替H2O2溶液,使0.2 mol Fe2+转化为Fe3+,则需NaClO至少为 mol。
(3)“除铁”的原理是 。
(4)“过滤”时滤渣1的主要成分是 。
(5)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是 。若“沉镍”后的滤液中c(Ni2+)<1×10-5 mol·L-1,则滤液的pH> 。
(6)“除钴”时,发生反应的离子方程式为 。
17.(14分)烟气中含有高浓度的SO2、NOx,在排放前必须进行脱硫、脱硝处理。回答下列问题:
(1)利用CH4可以将氮的氧化物还原为N2。
已知:N2(g)+O2(g)=2NO(g) △H1=+180.5 kJ·mol-1
CH4(g)+2O2(g)CO2(g)+2H2O(g) △H2=-802.3 kJ·mol-1
则反应CH4(g)+4NO(g)2N2(g)+CO2(g)+2H2O(g)的△H= kJ·mol-1。
(2)在体积为1 L的恒容密闭容器里,充入0.5 mol CH4和1 mol NO2,发生反应为:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g),测得n(NO2)随温度变化如图1所示。
①a点时,反应是否已达平衡状态? (填“是”或“否”)。
②该反应正反应的△H (填“>”或“<”)0。
③当反应体系中, (填“能”或“不能”)说明反应达平衡状态。
④T2℃时该反应的平衡常数为 。
(3).工业上可以用Na2SO3溶液吸收SO2,并用电解法处理吸收后所得NaHSO3溶液以实现吸收液的回收再利用(装置如图2所示)。电源a端为 极,阳极的电极反应式为 。
(二)选考题:共15分。请考生从给出的两道试题中任选一题作答。如果多做,则按所做的第一题计分。
18.[选修3:物质结构与性质](15分)
铁、铜等金属及其化合物在生产、生活中用途非常广泛。回答下列问题:
(1)Fe(CO)5可用作抗震剂,通过下列反应获得:Fe+5COFe(CO)5。
①基态Fe原子核外电子排布式为 ,其原子核外未成对电子数为 。
②与CO具有相同空间构型和键合形式的阴离子是 (填化学式),CO分子中σ键与π键数目之比为 ,C、N、O三种元素第一电离能由小到大的顺序为 。
(2)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)2(H2O)4]+,中心离子Fe3+的配位数为 ,配体是 ,H2O分子中O原子的杂化方式为 。
(3)一种含有Fe、Cu、S三种元素的化合物的晶胞如右图所示(晶胞底面为正方形),该化合物的化学式为 ,若晶胞的底面边长为a pm,晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,该晶胞的高为 pm。
19.[选修5:有机化学基础](15分)
6-硝基胡椒基酸(J)是合成心血管药物米络沙星的中间体,以芳香族化合物A为原料合成J的一种合成路线如下:
已知:连在同一个碳原子上的两个羟基易脱去一个水分子形成羰基。
回答下列问题:
(1)A的化学名称为 。
(2)B→C的反应类型为 。
(3)E的结构简式为 ,F中含氧官能团的名称是 (任写两种)。
(4)芳香族化合物X是H的一种同分异构体,X能发生银镜反应和水解反应,其核磁共振氢谱有四组峰,峰的面积之比为1:2:2:1,写出一种符合题目要求的X的结构简式: 。
(5)G→H的化学方程式为 。
(6)设计由邻苯二酚()和乙醇为原料制备[]的合成路线: (无机试剂任选)。
2021河南省商周联盟高二下学期6月联考化学试题PDF版含答案: 这是一份2021河南省商周联盟高二下学期6月联考化学试题PDF版含答案,文件包含2020-2021学年高二6月联考-化学pdf、2020-2021学年高二6月联考-化学DApdf等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。
2021河南省商周联盟高二下学期6月联考化学试题PDF版含答案: 这是一份2021河南省商周联盟高二下学期6月联考化学试题PDF版含答案,文件包含2020-2021学年高二6月联考-化学pdf、2020-2021学年高二6月联考-化学DApdf等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。
2021河南省商周联盟高二下学期6月联考化学试题PDF版含答案: 这是一份2021河南省商周联盟高二下学期6月联考化学试题PDF版含答案,文件包含2020-2021学年高二6月联考-化学pdf、2020-2021学年高二6月联考-化学DApdf等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。












