

2021江西省高安中学高一上学期第一次段考(B)化学试题含答案
展开江西高安中学 2020—2021学年上学期第一次月考
高一年级化学试题(B卷)
可能用到的相对原子质量:H-1 C-12 O-16 Al-27 S-32 Na-23 N-14 K-39
Cl-35.5 Ba-137 Cu-64 Mg-24 He-4
一、选择题(共16小题,每小题3 分,共48分,每小题只有一个正确答案)
1.已知丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1 g/mL,沸点约为55℃。要从水与丙酮的混合物里将丙酮分离出来,下列方法中最合理的是( )
A.蒸馏 B.分液 C.过滤 D.蒸发
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.在标准状况下,含有NA个氦原子的氦气(He)的体积约为11.2L
B.在常温常压下,11.2L Cl2含有的分子数为0.5NA
C.标准状况下,11.2L四氯化碳含有的分子数为0.5NA
D.25℃,1.01KPa,64gSO2中含有的原子数为3NA
3.Ag气体甲与Bg气体乙所含的分子数相等,下列说法中不正确的是( )
A.气体甲与气体乙的相对分子质量之比为A:B
B.等质量的气体甲与气体乙的分子数之比为B:A
C.同温同压下,同体积的甲气体与乙气体的质量之比为B:A
D. 同温同压下,甲气体与乙气体的密度之比为A:B
4. 500mL Al2(SO4)3溶液中含Al3+5.4 g,则溶液中SO42—的物质的量浓度是( )
A. 0.4mol·L-1 B. 0.6mol·L-1 C. 0.5mol·L-1 D. 0.2 mol·L-1
5. 取100 mL 0.3 mol/L和300 mL 0.25 mol/L的硫酸钾溶液注入500 mL容量瓶中,加水稀释至刻度线,该混合溶液中K+的物质的量浓度是 ( )
A.0.21 mol/L B.0.42 mol/L C.0.56 mol/L D.0.26 mol/L
6 . 在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比是8∶1∶2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比是( )
A. 1∶1∶1 B. 1∶2∶4 C. 1∶3∶2 D. 1∶4∶2
7.若以ω1和ω2分别表示浓度为a mol/L和b mol/L酒精溶液的质量分数,且知2a=b,则下列推断正确的是( )(已知酒精密度为0.77g/cm3)
A.2ω1=ω2 B.ω2﹤2ω1 C.ω2>2ω1 D.ω1<ω2<2ω1
8. 下列关于胶体的叙述正确的是( )
A. 用平行光线照射NaOH溶液和Fe(OH)3胶体时,产生的现象相同
B. 向氢氧化铁胶体中滴加氯化钠溶液会产生沉淀
C. Fe(OH)3胶体粒子在电场的作用下将向阴极运动,说明Fe(OH)3胶体带正电
D. 将饱和FeCl3溶液滴入沸水中,至出现红褐色的沉淀,即得Fe(OH)3胶体
9. 下列说法正确的是( )
A. 液态HCl、固态AgCl均不导电,所以HCl、AgCl是非电解质
B. NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质
C. 碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物
D. 非金属氧化物不一定是酸性氧化物,金属氧化物也不一定碱性氧化物
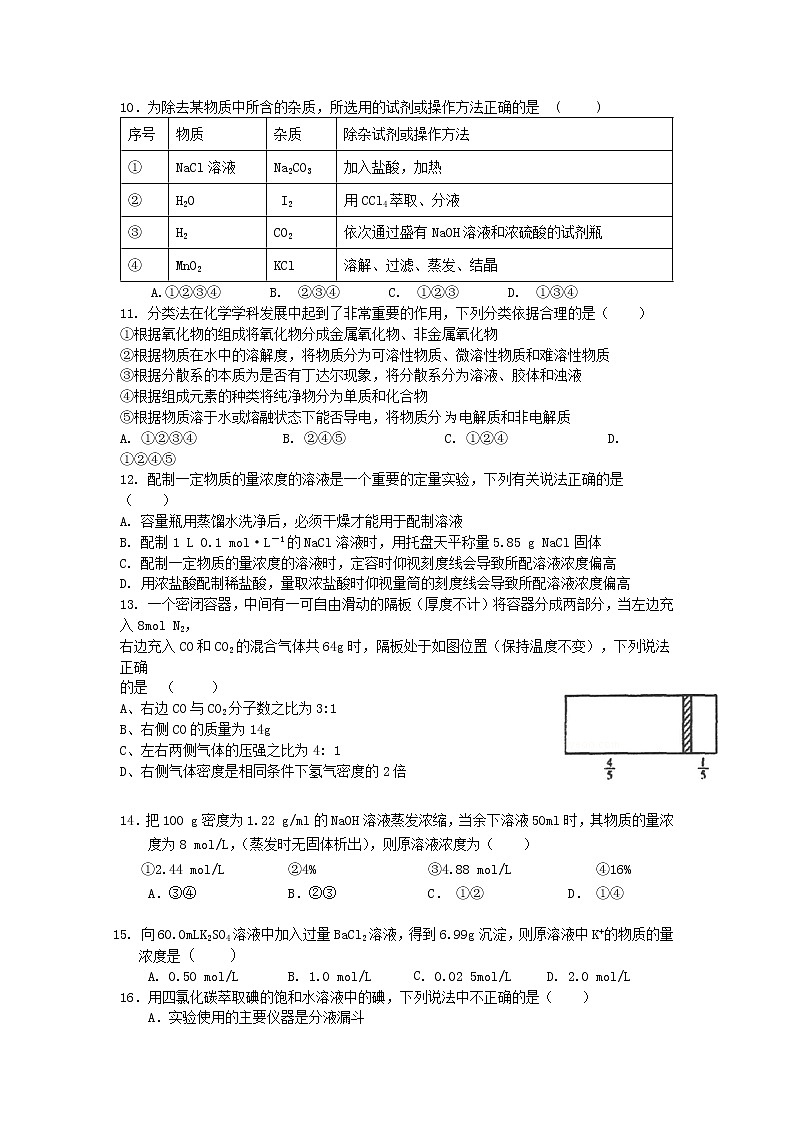
10.为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是 ( )
序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
① | NaCl溶液 | Na2CO3 | 加入盐酸,加热 |
② | H2O | I2 | 用CCl4萃取、分液 |
③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的试剂瓶 |
④ | MnO2 | KCl | 溶解、过滤、蒸发、结晶 |
A.①②③④ B. ②③④ C. ①②③ D. ①③④
11. 分类法在化学学科发展中起到了非常重要的作用,下列分类依据合理的是( )
①根据氧化物的组成将氧化物分成金属氧化物、非金属氧化物
②根据物质在水中的溶解度,将物质分为可溶性物质、微溶性物质和难溶性物质
③根据分散系的本质为是否有丁达尔现象,将分散系分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据物质溶于水或熔融状态下能否导电,将物质分电解质和非电解质
A. ①②③④ B. ②④⑤ C. ①②④ D. ①②④⑤
12. 配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是( )
A. 容量瓶用蒸馏水洗净后,必须干燥才能用于配制溶液
B. 配制1 L 0.1 mol·L-1的NaCl溶液时,用托盘天平称量5.85 g NaCl固体
C. 配制一定物质的量浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏高
D. 用浓盐酸配制稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高
13. 一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入8mol N2,
右边充入CO和CO2的混合气体共64g时,隔板处于如图位置(保持温度不变),下列说法正确
的是 ( )
A、右边CO与CO2分子数之比为3:1
B、右侧CO的质量为14g
C、左右两侧气体的压强之比为4: 1
D、右侧气体密度是相同条件下氢气密度的2倍
14.把100 g密度为1.22 g/ml的NaOH溶液蒸发浓缩,当余下溶液50ml时,其物质的量浓度为8 mol/L,(蒸发时无固体析出),则原溶液浓度为( )
①2.44 mol/L ②4% ③4.88 mol/L ④16%
A.③④ B.②③ C. ①② D. ①④
15. 向60.0mLK2SO4溶液中加入过量BaCl2溶液,得到6.99g沉淀,则原溶液中K+的物质的量浓度是( )
A. 0.50 mol/L B. 1.0 mol/L C. 0.02 5mol/L D. 2.0 mol/L
16.用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是( )
A.实验使用的主要仪器是分液漏斗
B.碘在四氯化碳中的溶解度比在水中的溶解度大
C.碘的四氯化碳溶液呈紫红色
D.分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出
二、非选择题(本题包括5道小题,共52分)
17.Ⅰ.(8分)
(1)下列物质能导电的是_______,属于电解质的是_________,属于非电解质的是 ____________。
A、碳酸氢钠固体 B、硫酸溶液 C、液态纯醋酸 D、Fe(OH)3胶体
E、乙醇 F、二氧化碳 G、水银
(2)写出实验室制备Fe(OH)3胶体的化学方程式_________________________ 。
Ⅱ.(6分)
(1)某气体在标准状况下的密度为1.25 g·L-1。该气体的相对分子质量为______ 。
(2)取1.43g Na2CO3•10H2O溶于水配成100ml溶液,则Na2CO3物质的量浓度为 __________ mol/L.
(3)同温同压下,体积比为1:2:3所组成的N2、O2和CO2混合气体33.6g在标准状况下体积为 __________ L.
18. (10分)现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3
晶体,相应的实验流程如图所示。已知NaNO3的溶解度受温度的影响较大。
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X ,沉淀A 。
(2)上述实验流程中①②③步均要进行的实验操作是 (填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是 。
(4)按此实验方案得到的溶液3中肯定含有 (填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的 (填化学式),之后通过蒸发浓缩, (填操作名称),过滤,洗涤、低温烘干可获得NaNO3晶体,。
19.(12分)实验室欲用KOH固体配制1.0 mol·L-1的KOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤并转移洗涤液 ⑦定容 ⑧冷却 其正确的操作顺序为__________________。必须用到的玻璃仪器有烧杯、胶头滴管、________________。
(2)某同学欲称量KOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为________ g ;
要完成本实验该同学应称出________ g KOH。
(3)使用容量瓶前必须进行的一步操作是_______ _。
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是________(填字母)。
A.所用KOH已经潮解 B.向容量瓶中加水未到刻度线
C.配制溶液定容时,仰视容量瓶刻度线 D.有少量KOH溶液残留在烧杯里
E.KOH固体溶解后,没冷却到室温就将溶液转移至容量瓶中
F.用带游码的托盘天平称5.4 g KOH(1 g以下用游码)时误用了“左码右物”方法
⑸若实验室要用63%的浓HNO3(其密度为1.4 g·mL-1)配制500 mL 0.50 mol·L-1稀HNO3,应量取63%的浓硝酸______ mL
20.(8分)某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
实验步骤如下:
①连接好实验装置,检查装置的气密性。
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0mL,换算成标准状况下氧气的体积为279.7mL。
⑤准确称量试管和残留物的质量为15.55g。
根据上述实验过程,回答下列问题:
(1)写出氯酸钾分解制O2 的化学方程式_____________。
(2)以下是测量收集的气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同;
②使试管和广口瓶内气体都冷却至室温;
③读取量筒内液体的体积。
进行③的实验操作时,若仰视读数,则读取的氧气体积______ _(填“偏大”“偏小”或“无影响”)。
(3)计算实验过程中产生氧气的物质的量是_____ mol;
实验测得氧气的气体摩尔体积是______(最后一空保留小数点后两位)。
三、计算题(共8分)
21.常温下,在27.5g水中溶解12.5g CuSO4·5H2O恰好达到饱和,该溶液密度为1.2g/cm3.试计算
⑴求该溶液的质量分数。 ⑵求该溶液中CuSO4的物质的量的浓度。
⑶20ml该CuSO4溶液与2mol/L的NaOH溶液恰好完全反应,写出反应方程式,并求需要NaOH溶液多少毫升?
高一年级化学试题(B卷)答案
一、选择题
1—5、B D C B B 6—10. D C B D C 11—16. C D A A B D
二、非选择题
17.Ⅰ. BDG, AC, EF
Ⅱ.(1)28 (2)0.05 (3)20.16
18. (除标注外,其余每空1分)
(1)AgNO3 BaSO4
(2)过滤
(3)除去过量的Ba2+和Ag+(2分)
(4)Na2CO3 HNO3(2分) 冷却结晶(2分)
19. (1)②①③⑧⑤⑥⑦④ 250mL容量瓶、玻璃棒
(2)27.4 14.0
(3)查漏
(4)BE ⑸17.8
20.(1)2KClO3=2KCl+3O2 (反应条件自己补上)
(2)偏小(2分)
(3) 0.0125(2分) 22. 38 L/mol(2分)
21. ⑴20% ⑵1.5mol/L ⑶30mL
2021江西省高安中学高二上学期期末考试化学试题含答案: 这是一份2021江西省高安中学高二上学期期末考试化学试题含答案
2021中山中山纪念中学高一上学期第一次段考化学试题含答案: 这是一份2021中山中山纪念中学高一上学期第一次段考化学试题含答案,共12页。试卷主要包含了00128g/mL, 单选题等内容,欢迎下载使用。
2021江西省高安中学高一上学期期末考试化学试题含答案: 这是一份2021江西省高安中学高一上学期期末考试化学试题含答案,共8页。试卷主要包含了5 Fe 56,2 L H2 O含有相同分子数,1ml电子,24L,排尽装置内的空气,防止氧气干扰等内容,欢迎下载使用。












