





所属成套资源:人教版高中化学选修一同步PPT课件+教案
人教版 (2019)选择性必修1第四节 化学反应的调控教学ppt课件
展开
这是一份人教版 (2019)选择性必修1第四节 化学反应的调控教学ppt课件,文件包含人教版化学选修一24《化学反应的调控》课件pptx、人教版化学选修一24《化学反应的调控》教学设计docx等2份课件配套教学资源,其中PPT共16页, 欢迎下载使用。
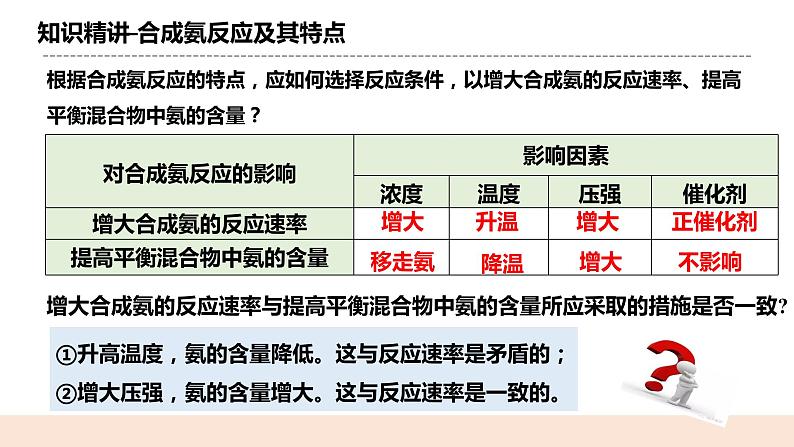
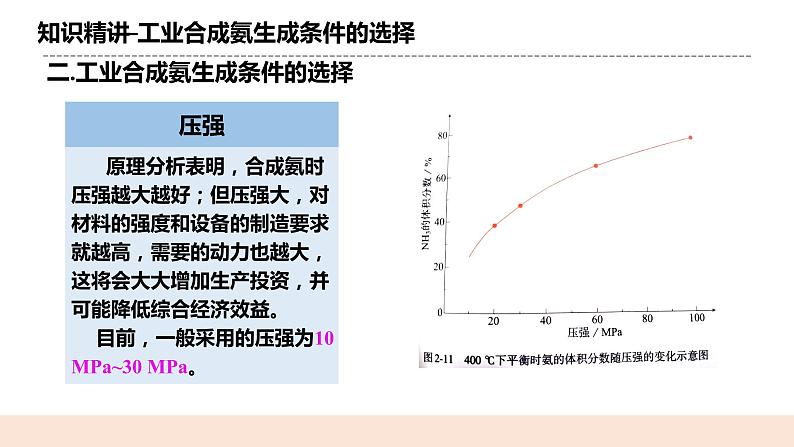
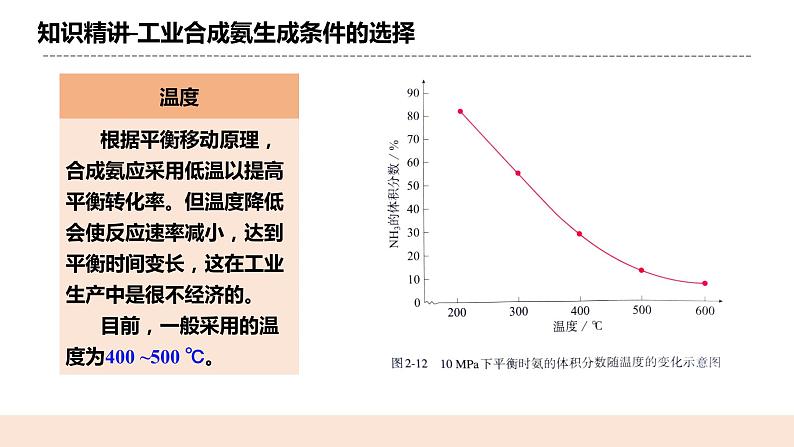
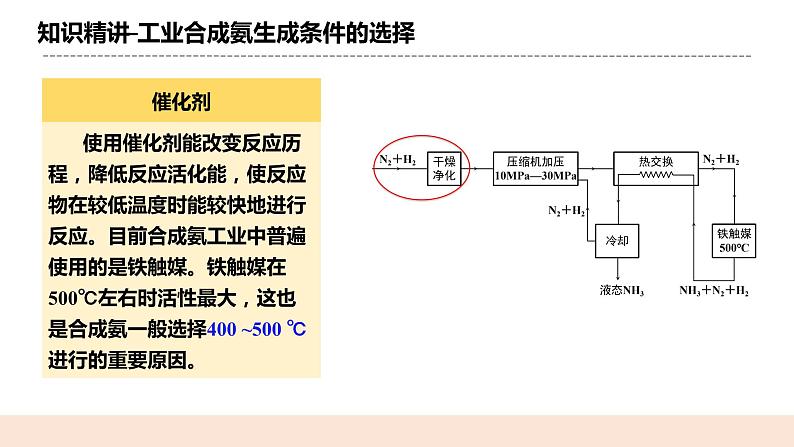
人教版化学选修一《化学反应的调控》教学设计课题名化学反应的调控教学目标1.知道如何应用化学反应速率和化学平衡分析合成氨的适宜条件,体会应用化学原理分析化工生产条件的思路和方法,发展变化观念与平衡思想的学科核心素养。2.在合成氨适宜条件的讨论中,形成多角度分析化学反应和化工生产条件的思路,体会化学反应原理的应用价值。教学重点1应用化学反应速率和化学平衡分析合成氨的适宜条件教学难点应用化学反应速率和化学平衡分析合成氨的适宜条件教学准备教师准备:课件、例题学生准备:复习影响化学平衡的因素知识教学过程一.新课导入氨是重要的无机化工产品之一,合成氨工业在国民经济中占有重要地位。农业上使用的氮肥,例如尿素、硝酸铵、磷酸铵、氯化铵以及各种含氮复合肥,都是以氨为原料的。 合成氨是大宗化工产品之一,世界每年合成氨产量已达到1亿吨以上,其中约有80%的氨用来生产化学肥料,20% 作为其它化工产品的原料。 二.知识精讲(一)合成氨反应及其特点N2(g)+3H2(g) 2NH3(g) ΔH=−92.4 kJ•mol−11.合成氨反应是可逆反应2.由化学方程式中的化学计量数关系可知,正反应是气体分子数减小的反应。3.根据ΔH=−92.4 kJ•mol−1可知,正反应是放热反应。根据合成氨反应的特点,应如何选择反应条件,以增大合成氨的反应速率、提高平衡混合物中氨的含量?对合成氨反应的影响影响因素浓度温度压强催化剂增大合成氨的反应速率增大升温增大正催化剂提高平衡混合物中氨的含量移走氨降温增大不影响增大合成氨的反应速率与提高平衡混合物中氨的含量所应采取的措施是否一致? ①升高温度,氨的含量降低。这与反应速率是矛盾的; ②增大压强,氨的含量增大。这与反应速率是一致的。 (二)工业合成氨生成条件的选择1.压强原理分析表明,合成氨时压强越大越好;但压强大,对材料的强度和设备的制造要求就越高,需要的动力也越大,这将会大大增加生产投资,并可能降低综合经济效益。 目前,一般采用的压强为10 MPa~30 MPa。 2.温度根据平衡移动原理,合成氨应采用低温以提高平衡转化率。但温度降低会使反应速率减小,达到平衡时间变长,这在工业生产中是很不经济的。 目前,一般采用的温度为400 ~500 ℃。 3.催化剂使用催化剂能改变反应历程,降低反应活化能,使反应物在较低温度时能较快地进行反应。目前合成氨工业中普遍使用的是铁触媒。铁触媒在500℃左右时活性最大,这也是合成氨一般选择400 ~500 ℃进行的重要原因。 4.浓度为提高平衡转化率,工业上采取迅速冷却的方法,使氨气变成液氨并及时分离,分离后的原料气N2和H2,并及时补充循环使用,使反应物保持一定的浓度。 工业合成氨生成条件的选择 工业合成氨的适宜条件压强10~30 MPa 温度400~500 ℃ 催化剂铁触媒浓度N2和H2的的投料比为1∶2.8,及时分离氨 (三)调控化学反应需考虑的问题 1.反应限度:要考虑尽量增大反应物的_转化率 _,充分利用原料。 2.反应速率:要选择较快的__反应速率___,提高单位时间内的产量。 3.生产要求:要考虑设备的要求和技术条件。 三.课堂小结1.合成氨反应及其特点 2.工业合成氨生成条件的选择 3.调控化学反应需考虑的问题 四.随堂练习1.在合成氨工业中,为增加NH3的日产量,实施下列措施的变化过程中 与平衡移动无关的是( B ) A.不断将氨分离出来 B.使用催化剂 C.采用700 K左右的高温而不是900 K的高温 D.采用2×107 Pa~5×107 Pa的压强 2.有关合成氨工业的说法中,正确的是( B ) A.增大H2的浓度,可提高H2的转化率 B.由于氨易液化,N2、H2在实际生产中会循环使用,所以总体来说氨的产率很高 C.合成氨工业的反应温度控制在400~500 ℃,目的是使化学平衡向正反应方向移动 D.合成氨厂采用的压强是10 MPa~30 MPa,因为该压强下铁触媒的活性最大 布置作业化学课时作业《化学反应的调控》板书设计化学反应的调控1.合成氨反应及其特点 2.工业合成氨生成条件的选择 3.调控化学反应需考虑的问题教学反思本节课内容较简单,是对前面所学知识的应用,教师在授课时,应注意引导学生利用所学知识解决实际问题。
相关课件
这是一份高中化学人教版 (2019)选择性必修1第四节 化学反应的调控完美版ppt课件,共3页。
这是一份人教版 (2019)选择性必修1第四节 化学反应的调控优秀课件ppt,共22页。PPT课件主要包含了知识回顾,催化剂,影响平衡的因素,制尿素,制纯碱,制硝酸,制冷剂,合成氨的应用,思考探究,3便宜等内容,欢迎下载使用。
这是一份高中第四节 化学反应的调控优秀ppt课件,共16页。PPT课件主要包含了基础巩固,能力提升等内容,欢迎下载使用。











