





所属成套资源:全套鲁科版高中化学选择性必修2教学PPT课件
鲁科版 (2019)选择性必修2第2节 几种简单的晶体结构模型背景图ppt课件
展开
这是一份鲁科版 (2019)选择性必修2第2节 几种简单的晶体结构模型背景图ppt课件,共60页。PPT课件主要包含了课前自主学习,非金属单质,非金属化合物,氧化物,sp3,°28′,正四面体,2堆积方式,较弱的分子间作用力,分子间作用力等内容,欢迎下载使用。
学习任务一 共价晶体的结构和性质任务驱动: 怎样从原子结构角度理解金刚石、硅和锗的熔点和硬度依次下降?
2.共价晶体与物质的类别
3.共价晶体的熔、沸点(1)共价晶体由于原子间以较强的共价键相结合,熔化时必需破坏共价键,而破坏它们需要很高的温度,所以共价晶体具有_____的熔点。(2)结构相似的共价晶体,原子半径越___,键长越___,键能越___,晶体的熔点越___。
【想一想】含有共价键的晶体都是共价晶体吗?提示:共价晶体中都有共价键,但含有共价键的不一定是共价晶体。如CO2、H2O等分子晶体中也含有共价键。
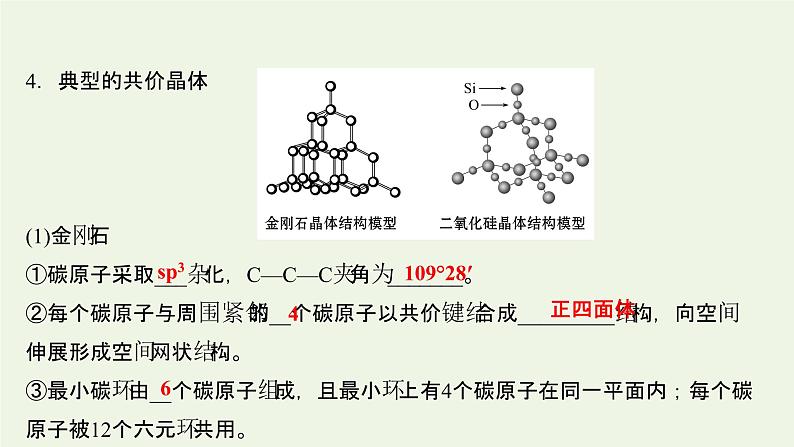
4.典型的共价晶体(1)金刚石①碳原子采取___杂化,C—C—C夹角为_______。②每个碳原子与周围紧邻的__个碳原子以共价键结合成_________结构,向空间伸展形成空间网状结构。③最小碳环由__个碳原子组成,且最小环上有4个碳原子在同一平面内;每个碳原子被12个六元环共用。
(2)晶体硅把金刚石中的C原子换成Si原子,得到晶体硅的结构,不同的是Si—Si键长___C—C键长。(3)二氧化硅晶体①Si原子采取___杂化,正四面体内O—Si—O键角为_______。②每个Si原子与__个O原子形成__个共价键,__原子位于正四面体的中心,__原子位于正四面体的顶点,同时每个O原子被__个硅氧正四面体共用;每个O原子和__个Si原子形成__个共价键,晶体中Si原子与O原子个数比为____。③最小环上有___个原子,包括__个O原子和__个Si原子。
【想一想】(1)SiO2是二氧化硅的分子式吗?提示:不是。二氧化硅为共价晶体,晶体中不存在单个分子,其化学式为Si与O的最简个数比,而不是分子式。(2)在SiC晶体中,最小的环上有几个原子?1 ml SiO2中含有Si—O键的物质的量是多少?提示:在SiC晶体中,最小的环上有6个原子,其中有3个硅原子,3个碳原子;在1 ml SiO2中含4 ml Si—O键。
学习任务二 分子晶体的结构与物质类别任务驱动:我们知道冰容易熔化,干冰容易汽化,碘晶体容易升华,你知道这些晶体为什么具有上述的特殊性质吗?它们的结构是怎样的呢?
2.分子晶体的物理性质(1)分子间以___________________相结合,分子晶体熔化时克服_____________,不破坏共价键,一般具有_____的熔点、沸点和_____的硬度,_____的挥发性。(2)组成和结构相似,晶体中不含氢键的物质,相对分子质量越大,分子间作用力越___,熔、沸点越___。
3.分子晶体与物质的类别
4.三种典型的分子晶体的组成和结构(1)碘晶体①碘晶体的晶胞是一个长方体,在它的_________________各有1个I2分子,每个晶胞中有__个I2分子。②I2分子之间以_________结合。
(2)干冰晶体①干冰中的CO2分子间只存在_________,不存在_____。②每个晶胞中有__个CO2分子,___个原子;每个CO2分子周围等距离紧邻的CO2分子数为___个。③干冰晶体中分子之间通过_________相结合,熔化时分子内的化学键_______。
(3)冰晶体①水分子之间的主要作用力是_____,当然也存在_________。②_____有方向性,它的存在迫使在___________的水分子与___________方向的__个相邻水分子互相吸引。
【想一想】 (1)晶体冰中水分子和氢键数目有什么关系?提示:晶体冰中每个水分子可以与紧邻的4个水分子形成氢键(不是2个);每个水分子平均形成2个氢键(不是4个)。
(2)为什么说冰晶胞的结构和金刚石的晶胞结构相似?提示:冰晶胞的结构和金刚石的晶胞结构相似,每个晶胞平均拥有8个水分子。晶体中C、O均采用sp3杂化,均与4个其他原子形成四面体结构单元,因此,冰晶胞的结构与金刚石的晶胞结构有一定的相似性。
学习任务三 晶体结构的复杂性任务驱动:石墨同层中所有碳原子都以共价键相连,构成平面网状结构,这类似共价晶体的结构特点,层与层之间有范德华力相连,这类似于分子晶体,石墨中有自由电子,能导电,这又类似于金属晶体,那么石墨属于什么晶体?1.石墨晶体
【想一想】(1)石墨晶体为什么具有导电性?提示:石墨晶体中每个C原子未参与杂化的轨道中含有1个未成对电子,能形成遍及整个平面的大π键,由于电子可以在整个六边形网状平面上运动,因此石墨沿平行的层能导电。(2)稀有气体由单原子构成,它属于共价晶体吗?提示:不是,它属于分子晶体。
(3)石墨为什么很软?提示:石墨为层状结构,各层之间是范德华力结合,容易滑动,所以石墨很软。(4)石墨的熔沸点为什么很高(高于金刚石)?提示:原因之一:石墨各层均为平面网状结构,碳原子之间既有C—C键又有大π键,故熔沸点很高。由于金刚石内只有C—C键没有大π键,所以石墨的熔点高于金刚石。
3.结构复杂的晶体——硅酸钠晶体
相关课件
这是一份鲁科版 (2019)选择性必修2第2节 几种简单的晶体结构模型教学ppt课件,共60页。PPT课件主要包含了NO1,NO2,NO3,点击右图进入等内容,欢迎下载使用。
这是一份高中第3章 不同聚集状态的物质与性质第2节 几种简单的晶体结构模型教学课件ppt,共60页。PPT课件主要包含了课前自主学习,非金属单质,非金属化合物,氧化物,sp3,°28′,正四面体,2堆积方式,较弱的分子间作用力,分子间作用等内容,欢迎下载使用。
这是一份高中化学鲁科版 (2019)选择性必修2第2节 几种简单的晶体结构模型多媒体教学课件ppt,共60页。PPT课件主要包含了内容索引,知识铺垫,自主梳理,金刚石晶体结构,二氧化硅晶体结构,碘晶体结构,干冰晶体结构,面心立方结构,冰晶体结构,苯甲酸晶体微观结构等内容,欢迎下载使用。









