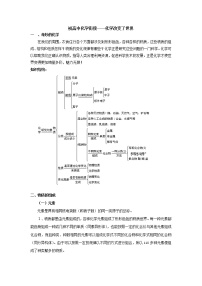
18.初高中化学衔接——水及常见溶液
展开初高中化学衔接——水及常见溶液
课标要求
1.认识水的组成,知道纯水与矿泉水、硬水与软水的区别。
2.了解吸附、沉淀、过滤和蒸馏等净化水的常用方法。
3.认识溶解现象,知道水是最重要的溶剂,酒精、汽油等也是常见的溶剂。
4.了解饱和溶液和溶解度的含义。
5.能进行溶质质量分数 的简单计算。
7.了解结晶现象。
8.能说出一些常见的乳化现象。[来源:学,科,网Z,X,X,K]
9.了解溶液在生产、生活中的重要意义。
10.利用溶解性表或溶解度曲线,查阅有关物质的溶解性或溶解度。[来源:学_科_网Z_X_X_K]
11.探究氯化钠、硝酸铵、氢氧化钠三种物质在水中溶解时的温度变化。
中考导向
各地中考关于水的考查主要是将水的知识和生、产、生活实际相结合,命题由单一型转向综合型,考查水资源的利用和保护的方法,体现开发水、利用水、保护水的德育功能。以水为材料将构成物质的粒子图示化,综合考查物质的组成、变化和分类是最近几年各地的命题趋势。
各地关于溶液的考查主要以选择题和填空题为主,主要体现在:溶液的概念和组成,饱和溶液和不饱和溶液的知识,这些知识的考查多放在具体的实例和现象中,和其他知识穿插在一起。溶解度和溶解度曲线的考查,多强调对溶解度的理解,考查溶解度曲线的应用。溶质质量分数很少单独考查,多数是和化学方程式的计算结合起来。一定溶质质量分数溶液的配制多出现在实验探究题中,考查配制的步骤和仪器的使用。
复习该部分要注意对溶液、饱和溶液、溶解度、溶解度曲线、溶质质量分数等概念的深该理解,做习题时要有针对性进行训练,做到一题多得,举一反三。
考点1:水的组成
题型:常以填空题、简答题形式出现。
考试趋势分析:水的组成实验探究是中考的一大热点。
典例讲解:
例1.有关电解水实验的下列叙述中,错误的是( )
A.可证明水由氢、氧元素组成
B.与电源正极相连的一端产生氧气
C.正、负极产生的气体质量比是1∶2
D.在水中加少量稀硫酸可增强水的导电性
解析:在电解水的实验中,水中加少量稀硫酸可增强水的导电性,与电源正极相连产生的是氧气,负极产生的是氢气,说明水中含有氧元素和氢元素,,故A、B、D正确;正、负极产生的体积比是1:2,质量比是8:1,故C错。
答案:C[来源:学科网]
例2水是生命之源,既普通又宝贵。下列有关水的说法正确的是( )
A.水通电生成氢气和氧气,因此水是由氢元素和氧元素组成的
B.自然界的水经过滤后就得到软水
C.为了节约用水,可以用工业废水直接浇灌农田
D.水蒸发时水分子不断运动,水结冰时水分子静止不动
解析:水通电生成氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据反应前后元素的种类不变,可推知水是由氢元素和氧元素组成的,A为正确选项。自然界的水经过滤后只是除去了不溶性杂质,其中可能还含有较多的可溶性钙、镁化合物,是硬水,煮沸后才可得到软水,故B为错项;工业废水中含有大量污染物,直接浇灌农田有害作物生长,从而影响人体健康,节约用水指的是不浪费水,提高水的利用效益,C为错项;水不论是在气态还是固态,都是由许许多多的水分子构成的,水分子都是在不断运动的,只是运动的速率不同而已,故D为错项。
答案:A[来源:Zxxk.Com]
考点2.水的净化
题型:试题将以选择题、填空题、探究题的形式出现。
考试趋势分析:水的净化方法,市售常见净水器、简易净水器的原理等在中考中经常出现,是中考的一大热点
典例讲解:
例3自然界中几乎不存在纯净的水,若要对自然界中是水进行净化处理,其中净化程度最高的方法是( )
A.吸附 B.沉降 C.过滤 D.蒸馏
解析:沉降、过滤只能除去水中的难溶性杂质,吸附可以滤去液体中的不溶性物质,还可以吸附一些溶解的杂质,除去臭味,而蒸馏可以将硬水软化,是净化程度最高的方法。
答案:D
例4下列各项与自来水的净化过程无关的是( )
A.吸附 B.沉降 C.电解 D.消毒
解析:吸附、沉降能使人净化,消毒能杀死水中的细菌,而电解过程是水发生了化学反应,生成了氢气和氧气,与水的净化过程无关,故答案选C。
答案:C
考点3.水体污染与防治
题型:选择题、填空题、简答题
考试趋势分析: 以灵活、多样的形式考查保护水资源为内容的命题。
典例讲解:
例5水是世界上最宝贵的资源之一。2009年3月22日第17个世界水日的主题是“跨界水──共享的水、共享的机遇”。下列做法不符合这一主题的是( )
A.加强水资源的保护
B.推动世界各国对水资源进行综合性统筹规划和管理
C.大力推广工业用水循环利用的方式
D.大量开采地下水缓解水资源紧缺
解析:地下水资源是有限的,应合理开发利用地下水缓解水资源紧缺。
答案:D
例6水可以造福人类,但水被污染后却给人类造成灾难。为了防止水的污染,下列各项:①抑制水中所有动、植物的生长;②不任意排放工业废水;③禁止使用农药和化肥;④生活污水经过净化处理后再排放。其中可以采用的方法是( )
A.①② B.②③ C.①④ D.②④
解析:本题考查了防治水体污染 的措施,属于基础题。要防止水的污染,工业废水、生活污水必须经过净化处理后再排放。
答案:D
考点4.溶液的概念
题型:选择题、填空题
考试趋势分析:溶液概念的考查往往与实际生产生活相联系,与身边的物质相结合。如判断碘酒是否为溶液,溶剂是什么,判断植物油、糖等是否能与水形成溶液等。
典例讲解:
例7把少量下列物质放入水中,能形成溶液的是( )
A.小苏打 B.汽油 C.石灰石 D.面粉
解析:溶液是一种均一、稳定的混合物汽油、面粉、石灰石不溶于水,小苏打易溶于水,溶于水后形成溶液。
答案:A
例8下列有关溶液性质的说法中错误的是( )
A.煮沸的咸汤比煮沸的水温度高
B.溶液一定是无色透明的
C.食盐水能导电是因为食盐水中含有较多自由移动的离子
D.消除路面上的积雪可以撒些盐,使冰雪较快融化
解析:溶液具有均一性和稳定性,但溶液不一定是无色的,如FeCl2溶液是浅绿色,FeCl3溶液是黄色的,CuSO4溶液是蓝色的,KMnO4溶液是紫红色的,
答案:B
考点5.溶解度
题型:选择题、填空题
考试趋势分析: 主要考查饱和溶液和不饱和溶液的概念、相互转化方法、判断方法及其与溶质的质量分数的关系,溶解度概念和溶解度曲线的意义。
典例讲解:
例9右图是甲、乙两种固体物质的溶解度曲线,据此判断以下叙述正确的是 ( )
A.甲的溶解度比乙的溶解度大
B.乙的溶解度受温度变化影响较大
C.要从乙的饱和溶液中得到乙,通常采用蒸发溶剂的方法
D.20℃时,甲、乙两种饱和溶液中溶质的质量相等
解析:由溶解度曲线可以看出:乙的溶解度随温度的升高变化不大,要从乙的饱和溶液中得到乙,通常采用蒸发溶剂的方法,故C为正确选项,B为错项。溶解度与温度有关,只有温度大于20℃时,甲的溶解度才大于乙的溶解度,A为错项;20℃时,甲、乙的溶解度相等,则20℃时,甲、乙两种饱和溶液中溶质的质量分数相等,但溶质的质量未必相等,只有溶剂质量相等时,溶质质量才相等,D为错项。
答案:C
例10下图是甲乙两种固体物质的溶解度曲线。据图回答:
(1)P点的含义是___________。
(2)20℃时要使接近饱和的甲溶液变成饱和溶液,可彩的方法有_________(写出一种)
(3)当甲中含有少量乙时,可采用____________的方法提纯甲 。
(4)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为____;若将烧杯内物质升温到50℃(不考虑水蒸发),溶液中变化的是_____(选填A、B、C、D)
A、溶剂的质量
B、溶液的质量
C、溶质的质量分数
D、以上都不变
解析:(1)溶解度曲线上的点表示物质在该点所表示温度下的溶解度,故P点的含义是:30℃时,甲的溶解度为60g。(2)甲的溶解度随温度的升高而显著增大,因此可采用降低温度的方法使20℃时接近饱和的甲溶液变为饱和溶液,也可用增加甲物质或蒸发水的方法。(3)由曲线可以看出,甲的溶解度随温度的升高而显著增大,而乙的溶解度随温度的升高而变化不大,当甲中含有少量乙时,可采用冷却热饱和溶液的方法使甲大部分结晶析出,而乙仍留在溶液里,达到提纯甲的目的。(4)解此题应该注意放入的40g甲物质有没有完全溶解,没溶解的不能算在溶质里,既然固体没有完全溶解,那么所得溶液就是饱和溶液,饱和溶液中
溶解度
100+溶解度
溶质的质量分数= × 100% 。
根据溶解度曲线可知,30℃时,甲的溶解度为60g,意即30℃时,100g水中最多能溶解甲物质60g,50g水中最多能溶解甲物质30g。题目中在30℃时,将40g甲物质放入盛有50g水的烧杯中并不能全部溶解,所得溶液为饱和溶液,其溶质的质量分数为60g/(100g+60g)*100%= 37.5%;若将烧杯内物质升温至50℃,甲的溶解度增大,原来不溶的甲物质继续溶解,溶质质量增大,而溶剂质量不变,则溶液质量增大,溶质的质量分数也增大。
答案:(1)30℃JF ,甲的溶解度为60g(2)降低温度(3)冷却饱和溶液
(4) 37.5% B、C
考点6.溶液的配制
题型:选择题、填空题、简答题
考试趋势分析: 主要考查溶液配制的步骤及产生误差原因的分析。
典例讲解:
例11制作“叶脉书签”需要配制100g12%的NaOH溶液(设水的密度为1g/mL)。下列操作正确的是
A.称量前调节天平平衡时发现指针向右偏转,可调节游码
B.在左右托盘上垫滤纸称取12.0gNaOH固体
C.将准确称取的NaOH固体直接倒入装有水的量筒中溶解
D.选用100mL量筒量取88.0mL的水
解析:称量前调节天平平衡时发现指针向右偏转说明天平没有平衡,应将右边的螺母向里调,而不能调节游码,故A错;NaOH固体易潮解,称量时应放在玻璃器皿里(如小烧杯中)称量,而不能放在滤纸上故B错;量筒不能用来溶解药品,应放在烧杯中,故C错。
答案:D
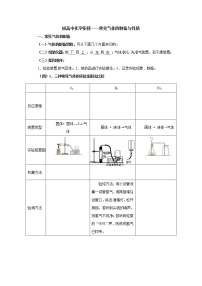
例12下图是配制溶质质量分数一定的氯化钠溶液的有关操作示意图。
⑴写出图中你喜欢的一种仪器名称 ;
⑵配制氯化钠溶液的操作顺序是 (填序号);
①ABCDE ② BDCEA ③DBCAE
⑶指出并纠正图中一处错误: 。
解析:⑴为开放性试题,考查对常见仪器的识记。⑵配制固体溶质的质量分数,其步骤为:计算、称量、溶解,故顺序为BDCEA。⑶通过观察不难发现,图中共有三处错误,取用固体药品时,瓶塞应倒放在桌面上,B中瓶塞正放;称量药品时,应左盘放称量物,右盘放砝码,图D放倒了;用托盘天平称量药品,不能直接放在托盘上,应在托盘上各放一张大小相等的同种的纸。
答案:⑴烧杯、量筒、药匙、托盘天平(合理均给分)⑵② ⑶B的瓶盖应倒放、D称量时,应左盘放称量物,右盘放砝码。用托盘天平称量固体药品时,为防止污染药品,常把药品放在纸上称量。
真题归纳:
一、选择题
1.以下的“水”属于纯净物的是( )
A.雨水 B.消毒水 C.海水 D.蒸馏水
2. 区别硬水和软水,选用的物质是( )
A.明矾 B.石蕊 C.活性炭 D.肥皂水
3.下列有关水的叙述中,错误的是( )
A.水由氢元素和氧元素组成 B.生命活动离不开水
C.水的沸腾属于物理变化 D.任何物质溶于水都不会放热或吸热
4.中水是生活污水经处理后,达到规定水质标准,可在一定范围内再次使用的非饮用水。在将污水净化处理成中水的过程中,除去异味的方法是
A.蒸馏 B.吸附 C.沉淀 D.过滤
5.如图表示a、b两种固体物质的溶解度曲线,下列叙述正确的是
A.a的溶解度大于b的溶解度
B.a、b两种物质的溶解度受温度影响变化较小
C.在t℃a、b两种物质的饱和溶液中溶质质量分数相等
D.当a中含少量b时,可用冷却热饱和溶液的方法提纯a
6.将60℃饱和的硝酸钾溶液降温至20℃,没有发生变化的是( )
A.溶液的质量 B.溶液里溶质的质量
C.溶液里溶剂的质量 D.溶液里溶质的质量分数
7.下列关于溶液的说法,不正确的是( )
A.冷却或加入硝酸钾固体都能使接近饱和的硝酸钾溶液达到饱和
B.汗水浸湿的衣服晾干后出现白色斑迹,是因为水分蒸发后盐分结晶析出
C.氨水是氨气的水溶液,根据气体溶解度变化规律,贮存时要阴凉密封
D.氯化钠在20℃时溶解度是36g,则100g的氯化钠溶液中含有氯化钠36g
8.日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
A.修车工用汽油洗去手上的油污 B.洗发精洗去头发上的油脂
C.洗面奶洗去皮肤上的油脂 D.洗洁精洗去餐具上的油污
9.下列混合物中不属于溶液的是( )
A.食盐水 B.泥水 C.碘酒 D.澄清石灰水
10. “人离不开水,没有水就没有生命”。在生产自来水的过程中不能加入或通入的物质是( )
A.明矾 B.漂白粉 C.臭氧 D.硫酸铜
11.下表是氯化铵在不同温度时的溶解度
温度/℃
20
40
60
80
溶解度/g
40
50
58
68
据此数据,判断下列说法正确的是( )
A.20℃时,氯化铵饱和溶液中氯化铵的质量分数是25%
B.20℃时,70g氯化铵的饱和溶液升温至40℃得到不饱和溶液
C.40℃时,75g氯化铵的饱和溶液中加入25g水后氯化铵的质量分数为30%
D.80℃时,84g的氯化铵饱和溶液降温至60℃时有5g氯化铵析出
12.现有一杯20℃的饱和硝酸钾溶液,欲改变其溶质质量分数,下列方法可行的是( )
A.加入一定量的水 B.恒温蒸发部分水
C.升温到60℃ D.加入一定量的硝酸钾
13.今年3月22日是第十七届“世界水日”,3月22-28日是第二十二届“中国水周”。我国纪念“世界水日”和开展“中国水周”活动的宣传主题为:“落实科学发展观,节约保护水资源”。下列有关水的知识,其中不正确的是( )
A.水是一种最常见的溶剂,自然界中的水大多数含有杂质离子
B.水中Ca2+、Mg2+的增多会引起水体的富营养化污染
C.用煮沸或蒸馏的方法能降低水的硬度
D.在水溶液中发生化学反应,反应速度比较快而且充分
14. 20℃时,NaCl溶解于水的实验数据如下表。则下列叙述正确的是( )
A.②中所得溶液是饱和溶液
B.20℃时10g水最多能溶解4g NaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
15.下列各项中,前者一定大于后者的是( )
A.20℃时KNO3的溶解度、80℃时KNO3的溶解度
B.30℃时:NaCl不饱和溶液的质量分数、NaCl饱和溶液的质量分数
C.10 g镁与足量盐酸反应生成H2的质量、10g铝与足量盐酸反应生成H2的质量
D.NaOH溶于水后溶液的温度、NH4NO3溶于水后溶液的温度
16.下列关于溶液的说法,不正确的是( )
A.冷却或加入硝酸钾固体都能使接近饱和的硝酸钾溶液达到饱和
B.汗水浸湿的衣服晾干后出现白色斑迹,是因为水分蒸发后盐分结晶析出
C.氨水是氨气的水溶液,根据气体溶解度变化规律,贮存时要阴凉密封
D.氯化钠在20℃时溶解度是36g,则100g的氯化钠溶液中含有氯化钠36g
二、填空题
17.右图是甲、乙两种固体物质的溶解度曲线。
(1)t2℃时,甲物质的溶解度为 ;
(2)从图中你还能获得哪些信息?(任填一条) ;
(3)分析t1℃时,将10g乙物质放入100g水中,充分溶
解后所得的溶液是 (填“饱和”或“不饱和”)溶液。
欲使t2℃时乙物质的饱和溶液变为不饱和溶液,可采取的
方法 (任填一种方法)。
18. (1)汽油与酒精分别加入蒸馏水中,能形成溶液的是 。
(2)白糖固体放入口中有清凉感觉。请从溶解现象推测其可能原因是 。
(3)右图是a、b两种固体物质的溶解度曲线。
① 当温度低于20℃时,溶解度:a b (选填“>”“<”或“=”);
② t℃时,将a、b两物质的饱和溶液均加热至40℃(a、b不分解,水分未蒸发),两种溶液中溶质的质量分数:a b(选填“>”“<”或“=”)。
19.碘是紫黑色晶体,可以溶解在汽油中,形成紫红色溶液。
(1)碘的汽油溶液中,溶质是____________,溶剂是____________;
(2)甲、乙、丙三个同学分别画出下面的示意图,表示溶液中碘分子的分布(汽油分子没有画出)。
①如果已同学的示意图符合事实,应该观察到的现象是____________ ;
②根据你在实验中观察到的现象,____________(填甲、乙、丙)的示意图符合事实。
20.位于某著名旅游区的一条母亲河,昔日被严重污染。近年来经过综合治理,河面上已见成群的鸟儿上下翻飞。为确保母亲河的治理成果,某中学环保小组的同学配合环保部门,定期对河水进行取样测试。
(1)除去水样中难溶性的固体,需将水样(填序号)_________;
①加热 ②过滤 ③蒸发 ④冷却
(2)在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量(1)中所得到的液体,滴在试纸上,把试纸显示的颜色与标准比色卡比较,pH大于7,则说明该水样显_______性;
(3)由上述数据分析,该河水的主要污染物可能是(填序号)___________;
①带有酸臭味的城市生活污水 ②化工厂排放的污水
(4)2009年“中国水周”活动的宣传主题为“落实科学发展观,节约保护水资源”。水是生命之源,作为青少年,要珍惜水、保护水,让水造福人类。下列生活习惯应该摈弃的是(填序号)_____________。
①用盆接水洗菜 ②用养鱼水浇花草
③使用节水龙头 ④大量使用含磷洗衣粉洗衣服
21.为了探究“不的净化”过程,某实验小组从护城河中取了水样,观察到:
A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒。
现对水样进行如下处理:
⑴向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒,再向滤液中加入活性炭,利用其 性除去水样中的颜色和异味,该过程属于 变化(填“物理”或“化学”)。
⑵通入氯气杀菌消毒,得到自来水,发生的反应如下:Cl2+H2O=HCl+HClO(次氯酸)。请判断,次氯酸中氯元素的化合价为 。
⑶为了判断得到的自来水是硬水或软水,可加入 进行检验。
⑷将自来水蒸馏得到纯净水,把下列物质分别加入纯净水中,用玻璃棒不断搅拌,能形成无色溶液的是 (填序号)。
A.粉笔灰 B.硫酸铜 C.蔗糖 D.食用油
22. NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图24-1所示,请根据图像和有关信息回答下列问题:
(1)t2 ℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是 。
(2)如图24-2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发)。请判断:该饱和溶液中的溶质是NaNO2、NaCl和M中的 。
(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是 。
(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故。为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息: NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271 ℃,NaCl熔点为801 ℃。
① 小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水(水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察。你认为此方案是否可行 (填“可行”或“不可行”)。
② 该小组其他同学又设计出与小明不同的实验方案,并获得成功。你认为该方案可能是 (只填写一种方案并简单叙述)。[来源:Zxxk.Com]
答案:
1.D 解析:本题考查物质的分类,纯净物只含有一种物质。
2.D 解析:可用肥皂水区别硬水和软水,加入肥皂水后,泡沫较多,浮渣较少的是软水,泡沫较少,浮渣较多的水为硬水。
3.D 解析:物质在溶于水时,有吸热和放热的现象发生,如氢氧化钠溶于水后溶液温度升高,硝酸铵溶于水后溶液温度降低,氯化钠溶于水后溶液温度不变。
4.B 解析:吸附不仅可以滤去液体中的不溶性物质,还可以吸附掉一些溶解的杂质,除去臭味。
5.CD 解析:本题主要考查溶解度曲线、饱和溶液、不饱和溶液的有关知识,难度中等。根据溶解度曲线图可以看出,当温度<t0C时,a的溶解度小于b的溶解度,A错;a的溶解度受温度的影响比较大,B错。
6.C 解析:将60℃饱和的硝酸钾溶液降温至20℃,有硝酸钾晶体析出,发生改变的是:溶液的质量变小,溶质的质量变小,溶解度变小,溶质的质量分数变小;没有发生变化的是溶液里溶剂的质量。
7.D 解析:根据溶解度的定义可知,氯化钠在20℃时溶解度是36g,其含义是:20℃时,100g水中最多能溶解36g氯化钠,而D选项中“100g氯化钠溶液中含有氯化钠36g”没有指明温度和状态且氯化钠溶液应为130g,故不正确,题目要求选不正确的,则D为正确选项。硝酸钾的溶解度随温度的升高而显著增大,降低温度可使接近饱和的硝酸钾溶液达到饱和,加入溶质硝酸钾固体也能使接近饱和的硝酸钾溶液达到饱和,A为错项;汗水中含有盐分,水分蒸发后盐分结晶析出,衣服上出现白色斑迹,B为错项;气体溶解度随温度升高而减小,为防止氨气散逸,贮存氨水时要阴凉、密封,C为错项。
8.A 解析:汽油除去油污属于溶解,不属于乳化。
9.B 解析:溶液具有均一性、稳定性。泥水是悬浊液。
10.D 解析:硫酸铜是重金属盐有毒,不能加入。
11.BD 解析:20℃时,氯化铵饱和溶液中氯化铵的质量分数是=28.57%,A错;氯化铵的溶解度随温度的升高而增大,20℃时,70g氯化铵的饱和溶液升温至40℃,溶液由饱和变成了不饱和溶液,B正确;40℃时50g的氯化铵可形成150g饱和溶液,则75g氯化铵的饱和溶液中所含溶质的质量为25g,加入25克水后氯化铵的质量分数是=25 %,C错;80℃时,84g的氯化铵饱和溶液中含氯化铵34g含水50g,60℃时氯化铵的溶解度为58 g,50 g水中最多溶解氯化铵29g,析出晶体的质量为34g-29g=5g,D正确。
12.A 解析:因原溶液是饱和的,恒温蒸发部分水、加入一定量的硝酸钾溶质的质量分数都没有发生变化。升温到60℃,溶解度变大,溶液由饱和变为不饱为,但溶液的组成没有发生变化,故溶质的质量分数不变。
13.B 解析:富营养化是指在人类活动的影响下,生物所需的氮、磷等营养物质大量进入湖泊、河口、海湾等缓流水体,引起藻类及其他浮游生物迅速繁殖,水体溶解氧量下降,水质恶化,鱼类及其他生物大量死亡的现象,与水中Ca2+、Mg2+的增多没有关系。
14.C 分析表中数据可知,20℃时10g水最多能溶解3.6g NaCl,故②中所得溶液是不饱和溶液, ①所得溶液的溶质质量分数小于20%。
15.D 解析:NaOH溶于水后溶液的温度升高,NH4NO3溶于水后溶液的温度降低。
16.D 解析:氯化钠在20℃时溶解度是36g,则136 g(100g+36 g)的氯化钠溶液中含有氯化钠36g。
17.30g;t1℃时,甲、乙两物质的溶解度相等(凡合理答案均可);不饱和;加溶剂或升高温度
解析:⑴由题中图可见,t20C时甲的溶解度是30g;⑵从图上可以看出t10C时甲和乙的溶解度相同,t20C时甲的溶解度大于乙的溶解度;⑶t10C时乙的溶解度大于10g,所以在该温度下将10g乙放入100g水中得到的是不饱和溶液。
18.(1)酒精 (2)白糖溶解吸热 (3)① < ② =
19.(1)碘,汽油。(2)①底部颜色深 ② 甲
解析:(1)被溶解的物质是溶质,能溶解其他物质的物质是溶剂,碘的汽油溶液中,溶质是碘,溶剂是汽油;(2)①从乙同学的示意图可以看出:底部碘分子分布多,应该观察到的现象为:底部颜色深;②碘溶解在汽油中形成紫红色溶液,具有均一性和稳定性,溶液中任意一部分组成和性质完全相同,故甲的示意图符合事实。
20.(1)② (2)碱 (3)② (4)④
解析:⑴除去水样中难溶性的固体,可采用过滤的的方法;⑵水样的PH>7,说明水样呈碱性;⑷使用含磷洗衣粉,会使水质趋向富营养化,引发近海海水出现 “赤潮”。
【答案】⑴过滤;吸附;物理 ⑵+1 ⑶肥皂水 ⑷C
22.(1)NaNO2>NaCl>M (2)M (3)NaNO2>NaCl>M
(4)① 可行 ②分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl(或分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl)
17.初高中化学衔接——实验的设计与评价: 这是一份17.初高中化学衔接——实验的设计与评价,共11页。
31.初高中化学衔接——原子结构: 这是一份31.初高中化学衔接——原子结构,共8页。学案主要包含了课程目标,学海导航,例题解析,强化训练,参考答案等内容,欢迎下载使用。
3.初高中化学衔接——初中化学常见的几种题型总结: 这是一份3.初高中化学衔接——初中化学常见的几种题型总结,共17页。学案主要包含了典型例题,基础练习,基础练习答案等内容,欢迎下载使用。