




初中科学华师大版九年级上册3 常见的盐习题课件ppt
展开1.(中考·广州)下列关于氯化钠的认识,正确的是( )A.组成:含有钠和氯两种单质B.性质:与盐酸类似,能与碳酸盐反应C.用途:可用于生产金属钠D.生产:常用钠与氯气通过化合反应获得
【点拨】氯化钠中含有钠、氯两种元素,A错误;氯化钠的化学性质与盐酸不类似,不能与碳酸盐反应,B错误;氯化钠可用于生产金属钠,C正确;氯化钠常用海水晒盐的方法或通过盐湖、盐矿获得,D错误。
2.重庆警方曾一次查获近千只被增重的活鸡,每只鸡内都灌注了270 g左右的重晶石粉。重晶石粉主要成分是硫酸钡(BaSO4),密度约为4.5 g/cm3。则( )A.硫酸钡是一种氧化物B.硫酸钡易溶于水C.每只鸡灌注了约60 cm3重晶石粉D.硫酸钡被人误食后,能与胃中盐酸反应
3.下列盐中,大多不溶于水的是( )①磷酸盐 ②碳酸盐 ③硝酸盐④硫酸盐 ⑤盐酸盐A.①② B.②④ C.①③ D.①⑤
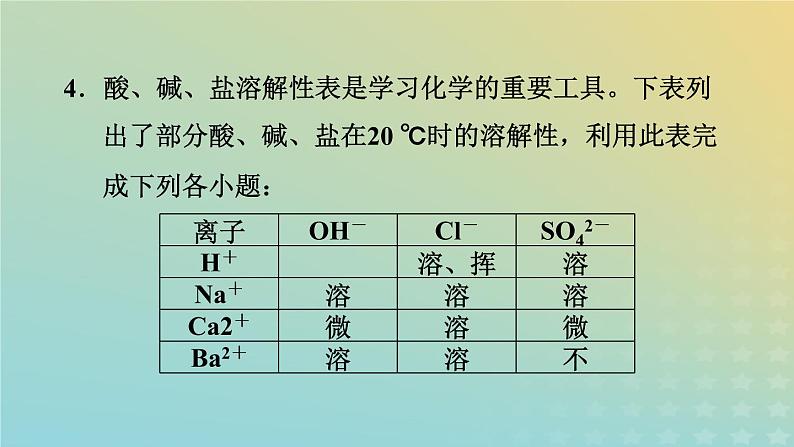
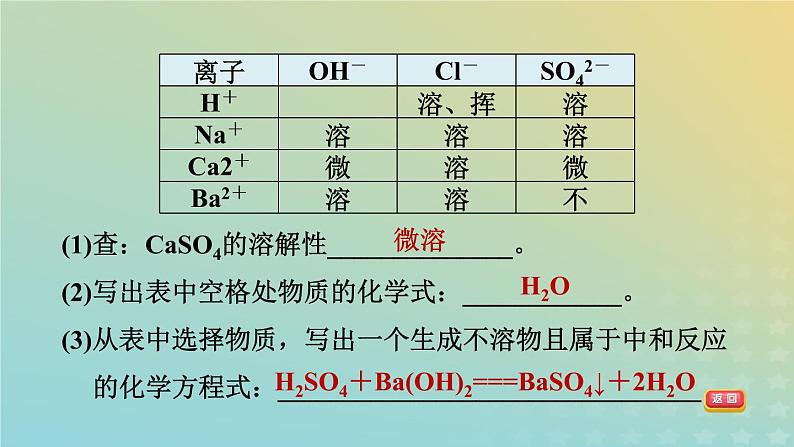
4.酸、碱、盐溶解性表是学习化学的重要工具。下表列出了部分酸、碱、盐在20 ℃时的溶解性,利用此表完成下列各小题:
(1)查:CaSO4的溶解性______________。(2)写出表中空格处物质的化学式:____________。(3)从表中选择物质,写出一个生成不溶物且属于中和反应的化学方程式:________________________________。
H2SO4+Ba(OH)2===BaSO4↓+2H2O
5.用化学方程式表示下列四种盐各是什么酸和什么碱反应的产物:(1)BaSO4:___________________________________。(2)CaCl2 :___________________________________。(3)NaNO3:__________________________________。
Ca(OH)2+ 2HCl===CaCl2+2H2O
NaOH+HNO3===NaNO3+H2O
6.(中考·莆田)多角度看物质,有助于加深对物质的认识。CuSO4是一种常见的盐,请回答:(1)CuSO4溶液显酸性,其pH________(填“>”“<”或“=”)7。(2)CuSO4可以看成是中和反应的产物,其对应的酸为________(填化学式,下同),碱为________。
(3)CuSO4作为反应物,写出一个符合A+B→C+D的化学方程式:__________________________________________。(4)CuSO4作为催化剂,能加快过氧化氢的分解,其化学方程式为_________________________________________。
Fe+CuSO4===FeSO4+Cu(合理即可)
7.在化学实验室,对某种化合物的溶液进行了以下实验:①取少量该溶液加入适量K2SO4溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解;②另取少量该溶液加入适量AgNO3溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解。则溶液中的溶质一定是( )A.BaCl2 B.CuCl2 C.Na2CO3 D.Ba(NO3)2
【点拨】所有的钾盐都能溶于水,加入硫酸钾后生成了不溶于硝酸的白色沉淀应是硫酸钡,所以原化合物提供了钡离子;加入硝酸银也出现了不溶于稀硝酸的白色沉淀,应是氯化银沉淀,所以原溶液提供了氯离子。
8.检验碳酸盐的正确方法是( )A.滴加盐酸,产生使木条火焰熄灭的气体B.滴加BaCl2溶液产生白色沉淀C.加热,产生气体D.滴加盐酸,产生使澄清石灰水变浑浊的气体
9.(2020·温州模拟)下列各组离子在溶液中能大量共存,并能使紫色石蕊溶液变蓝的是( )A.H+、Ba2+、NO 3-、CO 32-B.Ca2+、K+、NO 3-、Cl-C.Na+、Ba2+、OH- 、SO2-D.Na+、Ba2+、OH- 、Cl-
【点拨】H+、CO32-两种离子能结合成碳酸,碳酸不稳定,会分解成水和二氧化碳,不能大量共存,且含有大量H+的溶液不能使紫色石蕊溶液变蓝,选项A错误;四种离子间不能结合成沉淀、气体或水,可以共存,但溶液中不存在可使石蕊溶液变蓝的OH-,选项B错误;Ba2+、SO42-两种离子能结合成硫酸钡沉淀,不能大量共存,选项C错误;四种离子间不能结合成沉淀、气体或水,并且存在OH-,能使紫色石蕊溶液变蓝色,选项D正确。
10.为检测某化工厂排放的废液中是否含有SO42-,同学们设计了如下方案,并进行了实验。
(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是__________。(2)方案Ⅰ和Ⅲ中,结论不成立的方案是____________,理由是____________________________。(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除________的干扰。
方案Ⅰ不能排除Ag+的干扰
【点拨】(3)滴加硝酸钡有白色沉淀生成,不一定是硫酸钡,碳酸钡也是不溶于水的白色沉淀,但碳酸钡沉淀能溶于稀硝酸,硫酸钡不溶于稀硝酸,所以加入稀硝酸是为了排除碳酸根离子的干扰。
11.(2020·济宁)某未知溶液,可能含有Na+、Cu2+、Ba2+、SO42-、Cl-中的几种。为确定溶液中含有的离子,实验如下:①取未知溶液2~3mL于试管中,滴加足量BaCl2溶液,有白色沉淀生成,静置;②取①中上层清液,滴加AgNO3溶液,有白色沉淀生成;③另取未知溶液2~3mL于试管中,滴加NaOH溶液,有蓝色沉淀生成。
分析实验过程,回答:(1)溶液中一定存在的离子是__________________;(2)溶液中一定不存在的离子是________________;(3)溶液中可能存在的离子是__________________。
【点拨】①取未知溶液2~3mL于试管中,滴加足量BaCl2溶液,有白色沉淀生成,说明原溶液中一定存在硫酸根离子,一定不存在钡离子;②取①中上层清液,滴加AgNO3溶液,有白色沉淀生成,因为加入的氯化钡溶液带入了氯离子,所以无法确定原溶液中是否存在氯离子;③另取未知溶液2~3mL于试管中,滴加NaOH溶液,有蓝色沉淀生成,说明原溶液中一定存在铜离子。以上实验过程无法确定原溶液中是否存在钠离子。
12.(2020·绍兴月考) 兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们一起完成以下探究活动:【对固体猜想】猜想I:全部是NaOH。猜想Ⅱ:全部是Na2CO3。猜想Ⅲ:是NaOH和Na2CO3混合物。【实验和推断】
(1) 若加入的A溶液是稀盐酸,现象a为有气泡产生,现象b为无色酚酞试液不变红色,则该实验________(填“能”或“不能”)说明猜想Ⅱ成立。(2) 若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则该实验________(填“能”或“不能”)说明样品中有NaOH。
(3) 若A是CaCl2溶液,当实验现象a为__________________,现象b为____________________,则猜想Ⅲ成立。(4) 【反思】久置的氢氧化钠变质的原因是_____________________________(用化学方程式表示)。
2NaOH+CO2=Na2CO3+H2O
【点拨】(1)加入盐酸,氢氧化钠和碳酸钠都会与盐酸反应,干扰氯氧化钠的验证,不能说明猜想Ⅱ成立;(2)加入氢氧化钙,氢氧化钙与碳酸钠反应会生成氢氧化钠,干扰原物质中氢氧化钠验证,不能说明样品中有氢氧化钠;(3)若A是CaCl2溶液,氯化钙与碳酸钠反应产生碳酸钙沉淀和氯化钠,所以当实验现象a为有白色沉淀,现象b为酚酞试液变红色,说明猜想Ⅲ成立;(4)氢氧化钠变质是吸收空气中二氧化碳反应生成碳酸钠和水,反应方程式为2NaOH+CO2=Na2CO3+H2O。
初中科学华师大版九年级上册3 常见的盐优秀课件ppt: 这是一份初中科学华师大版九年级上册3 常见的盐优秀课件ppt,文件包含《常见的盐》课件第一课时pptx、《常见的盐》练习第一课时doc、《常见的盐》教案第一课时doc、视频wmv等4份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
华师大版九年级上册3 常见的盐课堂教学ppt课件: 这是一份华师大版九年级上册3 常见的盐课堂教学ppt课件,共19页。PPT课件主要包含了1碳酸钠,常见的碳酸盐,溶液变红,碳酸钠的化学性质,1与酸反应,Na2CO3,HCl,H2O,NaCl,CO2等内容,欢迎下载使用。
华师大版九年级上册3 常见的盐教课内容课件ppt: 这是一份华师大版九年级上册3 常见的盐教课内容课件ppt,共14页。PPT课件主要包含了各种各样的盐,盐的定义,氯化钠食盐,盐的水溶液的颜色,盐的溶解性规律等内容,欢迎下载使用。













