





所属成套资源:【新教材】-2022学年高一下学期化学人教版(2019)必修二同步习题(有答案)
人教版 (2019)必修 第二册第二节 化学反应的速率与限度授课ppt课件
展开
这是一份人教版 (2019)必修 第二册第二节 化学反应的速率与限度授课ppt课件,共60页。PPT课件主要包含了不再改变,最大程度,实际可能性,2一等一不变,课堂回眸,2具体实例等内容,欢迎下载使用。
一、 化学反应限度1.可逆反应:
【想一想】 什么是可逆反应?它有什么特点?提示:在同一条件下正反应方向和逆反应方向均能进行的化学反应叫可逆反应。特点如下:
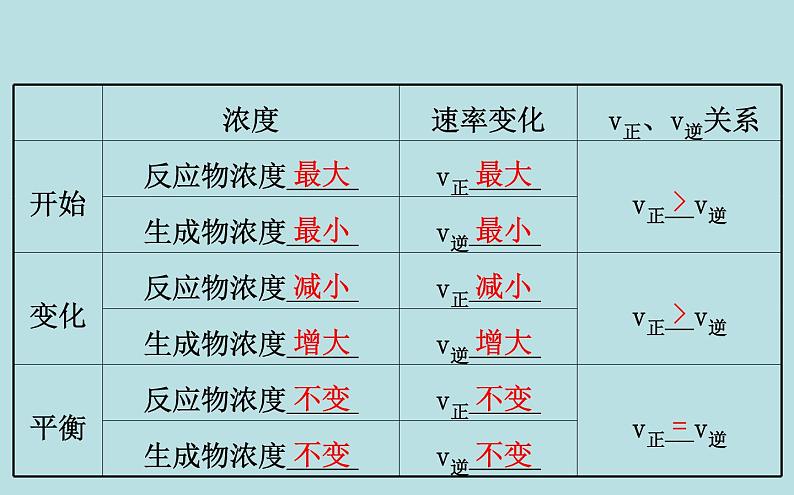
2.化学平衡的建立:(1)化学平衡建立的分析:①浓度对速率的影响的角度:在一定条件下,向反应容器中加入N2和H2发生反应:N2+3H2 2NH3。
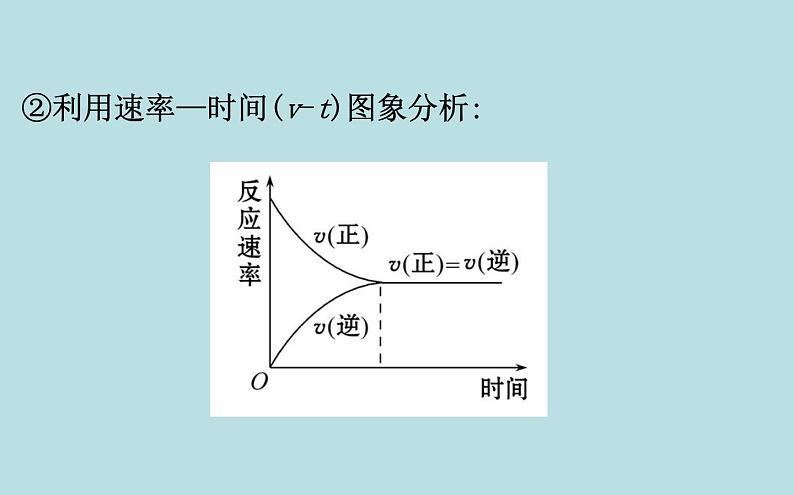
②利用速率—时间(v-t)图象分析:
(2)化学平衡状态的概念:在一定条件下,可逆反应进行到一定程度时,正反应速率和逆反应速率相等,反应物的浓度和生成物的浓度都_________,达到一种表面静止的状态。
【想一想】在已达到平衡的可逆反应2SO2+O2 2SO3中,由18O2代替等物质的量的O2。一段时间后,18O存在于哪些物质中?
提示:化学平衡是动态平衡,18O2代替等物质的量的O2后,18O2与SO2结合生成含18O的SO3,同时含18O的SO3分解,使SO2、O2中也含有18O,因此18O存在于SO2、O2、SO3这三种物质中。
(3)化学反应的限度:①化学平衡状态是可逆反应达到给定条件下所能达到的_________。②任何可逆反应在给定条件下的进行程度都有一定的限度。③改变反应条件可以在一定程度上改变一个化学反应的限度,即改变该反应的化学平衡。
【巧判断】(1)一个可逆反应达到的平衡状态就是该反应所能达到的最大限度。( )提示:×。化学平衡状态是可逆反应达到给定条件下所能达到的最大程度,条件改变限度可能改变。
(2)化学反应达到平衡状态时,该反应停止了。( )提示:×。可逆反应是动态平衡。
(3)可逆反应达到平衡状态时,各反应物、生成物的浓度相等。( )提示:×。可逆反应达到平衡状态时,各反应物、生成物的浓度不再改变,并非相等。
二、化学反应条件的控制1.目的:
2.化工生产中反应条件的调控:(1)考虑因素:化工生产中调控反应条件时,需要考虑控制反应条件的_____和___________。
(2)实例——合成氨生产条件的选择:
【情境·思考】生活中有很多现象都存在化学知识,如炉火越扇越旺,但蜡烛的火焰一扇就灭。
(1)同样是扇风结果为什么不同,试解释其中的原因?提示:“炉火越扇越旺”是扇风为燃烧提供了足量的氧气促进燃烧;“蜡烛的火焰一扇就灭”是由于空气流动带走大量的热量,使温度降低,低于了蜡烛的着火点。
(2)为了提高燃料的燃烧效率,应如何调控燃烧反应的条件?提示:①燃料与空气或氧气接触,且空气要适当过量。②尽可能使燃料充分燃烧,提高能量的转化率。③尽可能充分地利用燃料燃烧所释放出的热量,提高热能的利用率。
知识点 化学反应(限度)平衡状态的理解和判断【重点释疑】1.化学平衡状态的特征——“五字诀”:
2.化学平衡状态判断“三关注”“一等一不变”(1)三关注:①关注反应条件,是恒温恒容,恒温恒压,还是绝热恒容容器;②关注反应特点,是等体积反应,还是非等体积反应;③关注特殊情况,是否有固体参加或生成,或固体的分解反应。
【易错提醒】(1)化学平衡的实质是同种物质的正、逆反应速率相等。用不同物质的正、逆反应速率判断是否达到化学平衡状态时,要根据化学反应速率之比等于化学计量数之比,转化为同种物质的速率进行比较。(2)利用v(正)=v(逆)>0判断平衡状态时注意:反应速率必须是一正一逆,不能都是v(正)或都是v(逆)。
【思考·讨论】某恒温恒容密闭容器中,发生如下反应:2A(g)+B(g) 3C(g)+D(s),混合气体的压强不再改变能否表明该反应已达到平衡状态?
提示:不能。D是固体,反应前后气体的物质的量不变,由于容器的体积不变,故气体的压强始终不变,因此压强不再改变,不能表明该反应已达到平衡状态。
【案例示范】【典例】在一个体积固定的密闭容器中,进行的可逆反应A(s)+3B(g) 3C (g)。下列叙述中表明可逆反应一定达到平衡状态的是 世纪金榜导学号( )
①C的生成速率与C的分解速率相等;②单位时间内生成a ml A,同时生成3 a ml B;③B的浓度不再变化;④混合气体总的物质的量不再发生变化;⑤A、B、C的物质的量之比为1∶3∶3;⑥混合气体的密度不再变化A.①②③ B.①③④⑥ C.①③⑥ D.①③④
【思维建模】解答有关化学平衡标志的思维流程如下:
【解析】选C。①C的生成速率与C的分解速率相等,说明正逆反应速率相等,故①正确;②化学反应速率之比等于化学计量数之比,无论是否达到平衡状态,都存在单位时间内生成a ml A,同时生成3 a ml B,故②错误;③当反应达到化学平衡状态时,各物质的浓度不变,故③正确;④气体反应物与气体生成物的化学计量数之和相等,无论是否达到平衡状态,混合气体总的物质
的量都不变,故④错误;⑤平衡时各物质的物质的量取决于起始配料比以及转化的程度,不能作为判断是否达到平衡状态的依据,故⑤错误;⑥A为固体,当气体的总质量不变时,反应达到平衡状态,故⑥正确。
【母题追问】(1)混合气体的平均相对分子质量不变能否说明该反应达到平衡?提示:能。根据M= ,A是固体,反应前后气体的物质的量不变,但质量是改变的,因此当平均相对分子质量不再改变时,说明达到平衡。
(2)若A为气体,①~⑥中能够说明反应达到平衡状态的有哪些?提示:①③④。A为气体,则反应前后气体的总物质的量不相等,则④能够说明达到平衡;气体的质量和体积都不变,则密度始终不变,不能说明达到平衡。其他与原题一致。
【迁移·应用】 (2019·淮北高一检测)在恒温下的密闭容器中,有可逆反应:2NO+O2 2NO2(正反应为放热反应),不能说明已经达到平衡状态的是世纪金榜导学号( )A.正反应生成NO2的速率和逆反应生成O2的速率相等B.反应容器中压强不变C.混合气体颜色深浅保持不变D.混合气体的平均相对分子质量不随时间变化而变化
【解析】选A。该反应是一个反应前后气体物质的量不相等的反应,因此混合气体的平均相对分子质量、压强以及颜色保持不变,即说明达到平衡。A中表示的速率虽然方向相反 ,但速率之比不等于化学计量数之比,即应该是正反应生成NO2的速率和逆反应生成O2的速率的2倍相等,故A错。
【补偿训练】1.(2019·宿州高一检测)一定温度下,反应A2(g)+B2(g) 2AB(g)达到平衡的标志是 ( )A.单位时间内生成n ml A2同时生成n ml ABB.容器内的总压强不随时间的变化而变化C.单位时间内生成2n ml AB同时生成n ml B2D.单位时间内生成n ml A2同时生成n ml B2
【解析】选C。在一定条件下,判断一个反应是否达到平衡,主要看正逆反应速率是否相等,体系中各组分的浓度(或含量)是否保持不变。A项中,生成A2是逆反应,生成AB是正反应。显然v(正)
相关课件
这是一份高中化学人教版 (2019)必修 第二册第二节 乙烯与有机高分子材料备课ppt课件,共44页。PPT课件主要包含了空间结构,酸性高锰酸钾溶液褪色,原子或原子团,加成反应,聚合度,实验2,实验4等内容,欢迎下载使用。
这是一份人教版 (2019)必修 第二册第一节 化学反应与能量变化背景图ppt课件,共60页。PPT课件主要包含了镁条逐渐溶解,有气泡产生,温度计的示数,木片黏,在烧杯上,放出热量,吸收热量,热量的释放和吸收,释放热量,2实例等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第二册第一节 化学反应与能量变化教课课件ppt,共60页。PPT课件主要包含了锌片上有气泡,铜片上无气泡,不反应,锌片上无气泡,铜片上有气泡,电流表指针偏转,化学能,2原理分析,化学能转化为电能,失电子等内容,欢迎下载使用。











