2023届新高考专用化学二轮复习热考题型--练6 电化学原理与应用
展开练6 电化学原理与应用
(A组)
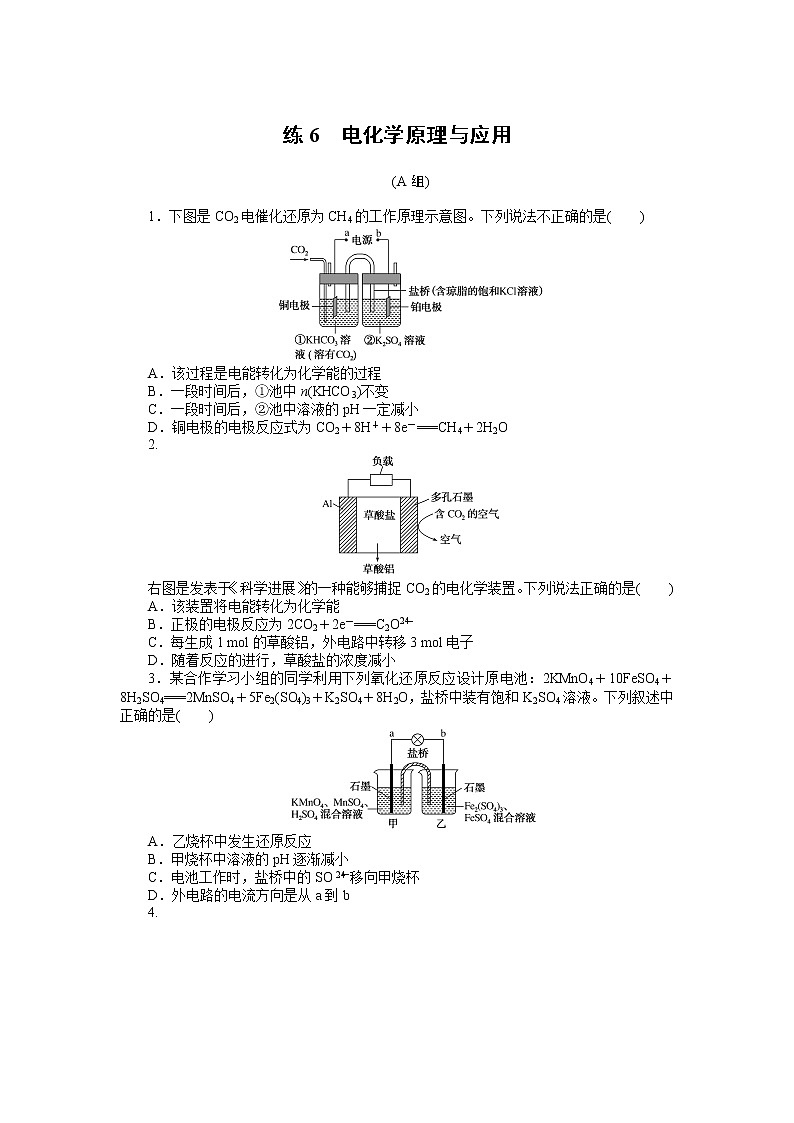
1.下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是( )
A.该过程是电能转化为化学能的过程
B.一段时间后,①池中n(KHCO3)不变
C.一段时间后,②池中溶液的pH一定减小
D.铜电极的电极反应式为CO2+8H++8e-===CH4+2H2O
2.
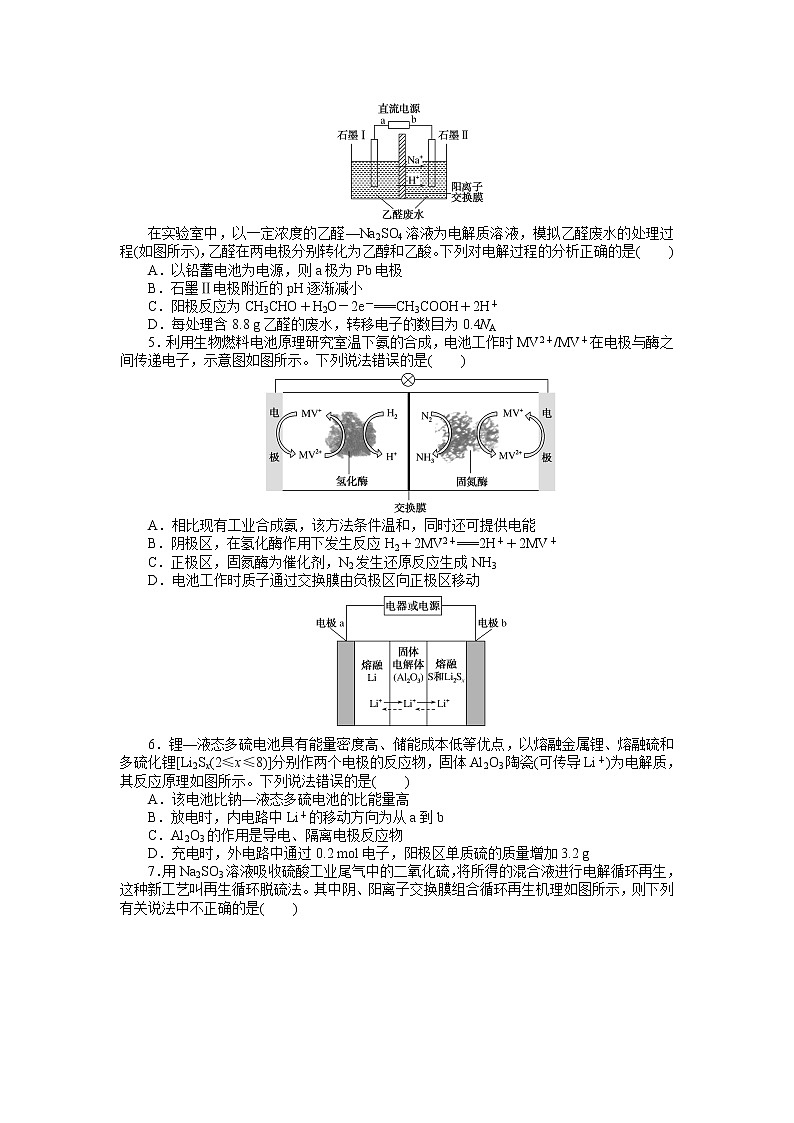
右图是发表于《科学进展》的一种能够捕捉CO2的电化学装置。下列说法正确的是( )
A.该装置将电能转化为化学能
B.正极的电极反应为2CO2+2e-===C2O
C.每生成1 mol的草酸铝,外电路中转移3 mol电子
D.随着反应的进行,草酸盐的浓度减小
3.某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,盐桥中装有饱和K2SO4溶液。下列叙述中正确的是( )
A.乙烧杯中发生还原反应
B.甲烧杯中溶液的pH逐渐减小
C.电池工作时,盐桥中的SO移向甲烧杯
D.外电路的电流方向是从a到b
4.
在实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程(如图所示),乙醛在两电极分别转化为乙醇和乙酸。下列对电解过程的分析正确的是( )
A.以铅蓄电池为电源,则a极为Pb电极
B.石墨Ⅱ电极附近的pH逐渐减小
C.阳极反应为CH3CHO+H2O-2e-===CH3COOH+2H+
D.每处理含8.8 g乙醛的废水,转移电子的数目为0.4NA
5.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。下列说法错误的是( )
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应H2+2MV2+===2H++2MV+
C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D.电池工作时质子通过交换膜由负极区向正极区移动
6.锂—液态多硫电池具有能量密度高、储能成本低等优点,以熔融金属锂、熔融硫和多硫化锂[Li2Sx(2≤x≤8)]分别作两个电极的反应物,固体Al2O3陶瓷(可传导Li+)为电解质,其反应原理如图所示。下列说法错误的是( )
A.该电池比钠—液态多硫电池的比能量高
B.放电时,内电路中Li+的移动方向为从a到b
C.Al2O3的作用是导电、隔离电极反应物
D.充电时,外电路中通过0.2 mol电子,阳极区单质硫的质量增加3.2 g
7.用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )
A.X为直流电源的负极,Y为直流电源的正极
B.阳极区pH增大
C.图中的b>a
D.该过程中的产品主要为H2SO4和H2
8.将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积V L。则下列说法正确的是( )
A.OH-由A端移向B端
B.0<V≤22.4 L时,电池总反应的化学方程式为CH4+2O2+KOH===KHCO3+2H2O
C.22.4 L<V≤44.8 L时,负极电极反应为:CH4+9CO+3H2O-8e-===10HCO
D.V=33.6 L时,溶液中阴离子浓度大小关系为c(CO)>c(HCO)>c(OH-)
(B组)
1.埋在地下的钢管道可以用如图所示方法进行电化学保护。下列说法正确的是( )
A.该方法将电能转化成化学能
B.在此装置中钢管道作正极
C.该方法称为“外加电流的阴极保护法”
D.镁块上发生的电极反应为O2+2H2O+4e-===4OH-
2.某课题组以纳米Fe2O3作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法错误的是( )
A.放电时,负极的电极反应式为Li-e-===Li+
B.放电时,电子通过电解质从Li流向Fe2O3
C.充电时,Fe做阳极,电池逐渐摆脱磁铁吸引
D.充电时,阳极的电极反应式为2Fe+3Li2O-6e-===Fe2O3+6Li+
3.某污水处理厂利用微生物电池将镀铬废水中的Cr2O催化还原,其工作原理如下图所示。下列说法不正确的是( )
A.电池工作过程中电子由a极流向b极
B.b极反应式:Cr2O+6e-+14H+===2Cr3++7H2O
C.电池工作过程中a极区附近溶液的pH增大
D.每处理1 mol Cr2O,可生成33.6 L(标况下)CO2
4.科研人员设计了一种电化学反应器以Na2SO4溶液为电解质,负载纳米MnO2的导电微孔钛膜和不锈钢为电极材料。这种电催化膜反应器可用于正丙醇合成丙酸,装置示意图如图所示,以下叙述错误的是( )
A.微孔钛膜作阴极
B.使用Na2SO4溶液是为了在电解开始时增强溶液导电性
C.正丙醇转化为丙酸的电极反应式为CH3CH2CH2OH+H2O-4e-===CH3CH2COOH+4H+
D.反应器工作时料槽中正丙醇分子向电催化膜移动
5.硼酸(H3BO3)可以通过电解NaB(OH)4溶液的方法制备,工作原理如图所示。下列有关表述错误的是( )
A.M室的电极反应式为2H2O-4e-===O2↑+4H+
B.N室中,进口和出口的溶液浓度大小关系为a%<b%
C.b膜为阴离子交换膜,产品室发生反应为H++[B(OH)4]-===H3BO3+H2O
D.理论上每生成1 mol H3BO3,阴极室可生成5.6 L(标准状况)气体
6.连二亚硫酸钠(Na2S2O4)俗称保险粉,还原性比NaHSO3更强,工业上广泛用于纺织品漂白及作脱氧剂等。工业上可用惰性电极电解NaHSO3溶液得到连二亚硫酸钠(Na2S2O4),如下图所示。下列说法不正确的是( )
A.得到连二亚硫酸钠产品电极反应式为2HSO+2e-===S2O+2OH-
B.a为阳极
C.连二亚硫酸钠产品在阴极得到
D.若不加隔膜,则得不到连二亚硫酸钠
7.
中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法正确的是( )
A.a极为正极
B.随着反应不断进行,负极区的pH不断增大
C.b极的电极反应为MnO2+2H2O+2e-===Mn2++4OH-
D.若消耗0.01 mol葡萄糖,电路中转移0.02 mol电子
8.某锂碘电池结构如图所示,该电池的总反应为2Li+P2VP·nI2===P2VP·(n-1)I2+2LiI。下列说法正确的是( )
A.该电池工作时,锂离子移向a极
B.该电池放电时,锂电极发生还原反应
C.锂电极质量减少0.7 g时,b极转移的电子数为6. 02×1021
D.正极的电极反应式为VP·n+2+2e-===VP·(n-1)+2LiI
微主题3 反应热 电化学 专练2 原电池、电解池的工作原理及应用 热练(含解析)—2024年高考化学二轮复习: 这是一份微主题3 反应热 电化学 专练2 原电池、电解池的工作原理及应用 热练(含解析)—2024年高考化学二轮复习,共8页。试卷主要包含了5 kJ·ml-1;,7 kJ·ml-1;,4 kJ·ml-1,12 ml等内容,欢迎下载使用。
高考化学三轮复习题型精准练题型九电化学原理及应用(含解析): 这是一份高考化学三轮复习题型精准练题型九电化学原理及应用(含解析),共7页。试卷主要包含了单项选择题,不定项选择题等内容,欢迎下载使用。
2023届新高考专用化学二轮复习热考题型--练1 STSE中的化学: 这是一份2023届新高考专用化学二轮复习热考题型--练1 STSE中的化学,共3页。试卷主要包含了下列对有关文献的理解错误的是等内容,欢迎下载使用。












