





- 华师大9上科学1.3 用分解反应制取氧气 课件 课件 1 次下载
- 华师大9上科学1.3 用分解反应制取氧气 教案 教案 2 次下载
- 华师大9上科学2.1 生活中的酸和碱 课件 课件 2 次下载
- 华师大9上科学2.1 生活中的酸和碱 教案 教案 1 次下载
- 华师大9上科学2.2 重要的酸 课件 课件 3 次下载
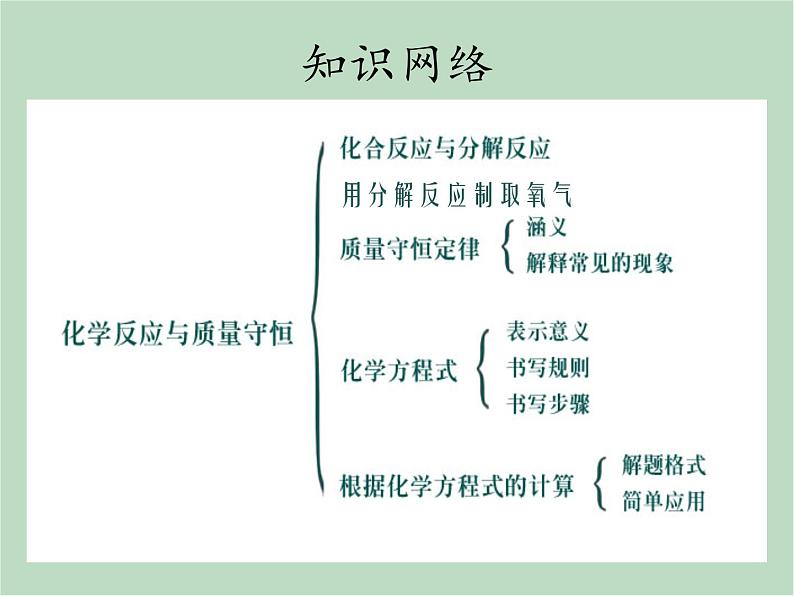
2020-2021学年第1章 化学反应综合与测试复习课件ppt
展开1.一切化学反应都必须遵守 ,该定律的内容是 。2.物质发生化学反应时,只是反应物的原子 生成新物质,反应前后 都没有发生改变,因此化学反应前后各物质的 一定相等。 3.化学方程式是用 表示化学反应的式子,书写化学方程式必须遵守的两个原则是: 。书写化学方程式的步骤依次是:(1)写: ;(2)配: ;(3)标: 。
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
原子的种类、数目、质量
以客观事实为依据;以质量守恒定律为根据
左边写反应物的化学式、右边写生成物的化学式
反应物是氢气和氧气;生成物是水;反应条件是点燃;反应物与生成物质量比为1∶8∶9;反应物与生成物分子个数比为2∶1∶2
5.根据化学方程式的计算(1)根据化学方程式计算的依据①理论依据: 定律。②列比例依据: 和 各物质间的质量比为一定值。(2)根据化学方程式计算的步骤依次是①设: ;②写:写出化学方程式;③找: ;④列: ;⑤求: ;⑥答: 。
没有学过的化学方程式更简单,因为题目中有提示!把题目的提示拿来用就是!
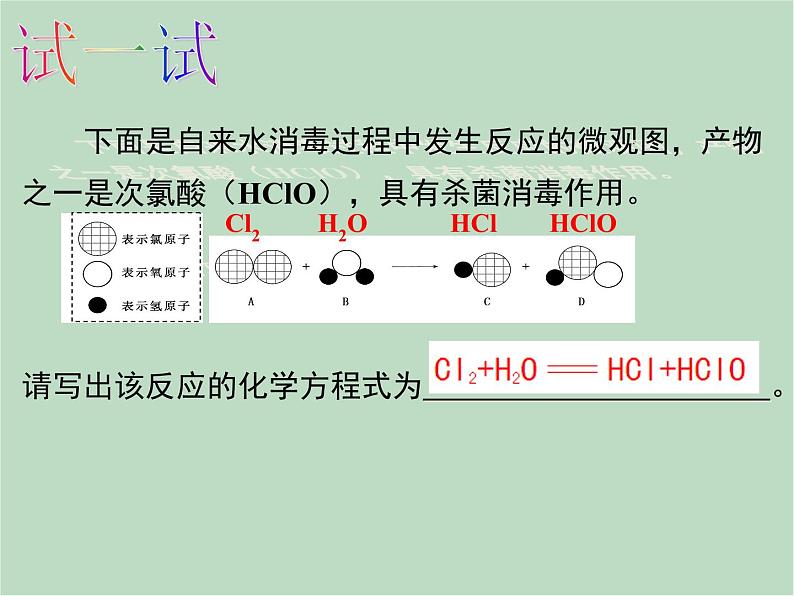
没有学过的化学方程式怎么写?
我国陈乾旺等科学家的最新研究表明,在高温高压下,二氧化碳和金属钠反应产生金刚石和碳酸钠,合成的金刚石最大直径达1.2毫米,完全可以满足工业用途。二氧化碳和反应生成金刚石和碳酸钠的化学方程式为:
CO2+ Na C+ Na2CO3
1.质的方面:表示参加反应是什么物质,结果生成什么物质;表示反应物在什么条件下进行反应。
2.量的方面:表示反应物、生成物各物质之间的分子数比;表示反应物、生成物各物质之间的质量比。
相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 K-39 Ca-40
试计算下列化学式的相对质量
2H2O2 CaCO3 2KClO3 3O2
例1.完全燃烧多少克镁,可生成10克氧化镁?(Mg:24 O:16)
解:设需完全燃烧镁X 。
答:完全燃烧6克镁,可生成10克氧化镁。
2.写出反应的化学方程式
3.找:计算相关物质的相对分子质量及质量比
标出已知量、未知量
练习1.实验室里用加热氯酸钾和二氧化锰的混合物制取氧气,现将氯酸钾和二氧化锰混合物25克加热至气体不再产生,称得剩余固体的质量为15.4克,问:1.产生氧气多少克?2.原混合物中含氯酸钾多少克?
解:氧气的质量为:25克-15.4克=9.6克
设:原混合物中含氯酸钾X。
答:产生氧气9.6克,原混合物中含氯酸钾24.5克。
练习2:实验室里用50克含6.8%的过氧化氢的双氧水溶液在二氧化锰作催化剂条件下制取氧气。问:1.可制得氧气多少克? 2.若氧气的密度是1.43克/升,求制得的氧气体积是多少升?(H:1 O:16)
解:过氧化氢的质量为:50克×6.8%=3.4克
答:产生氧气1.6克,合体积1.12升。
∴ V = m/ρ =1.6g÷1.43g/L = 1.12L
练习3.把一定质量的碳放在一定质量的氧气中燃烧。实验数据如下表:1.这三次实验,从数据看,哪几次符合质量守恒定律?2.第二次实验为什么不生成28克CO2?哪种物质有剩余?余下多少克?3.第三次实验为什么不生成30克CO2 ?哪种物质有剩余?余下多少克?
方程要配平,纯量代方程;对应列比例 ,单位不能忘;6步骤需完整。
化学方程式计算中应注意的几个问题:
1.解题格式一定要规范和程序化。2.化学方程式一定要正确,一定要配平,否则违背客观事实和质量守恒定律。3.各物质之间的质量比一定要计算准确,不能马虎,更不能张冠李戴。4.化学方程式计算依据的是“质量守恒定律”,因此题中如给的条件是体积先要换算成单位。5.化学方程式中各量都是纯物质之间的质量关系,计算时一定要把杂质去掉才行。
例2.实验室用过氧化氢制取氧气,现欲制氧气2.24升(氧气在常温下的密度为1.429克/升)。问:需过氧化氢多少克?
2H2O2 2H2O + O2↑
68 32
解: m = ρv = = 3.2g
设需过氧化氢的质量为X
例3.如图所示,实验室用过氧化氢制取氧气,烧瓶内的物质的质量在完全反应前后如下右图所示,问:实验前加入过氧化氢多少克?
68 32
解:氧气质量=100 – 96.8 = 3.2g
例4.实验室用100克过氧化氢溶液制取氧气,完全反应后生成氧气3.2克?问:原氧化氢溶液的质量分数是多少?
68 32
1.在化学反应A+B=C+D中,40克A和1克B恰好完全反应,生成20克C,则生成D的质量是 ( ) A.20克 B.21克 C.41克 D.59克
2. a g与b g的氯酸钾和二氧化锰混合后,充分加热,得剩余固体cg,则生成氧气的质量为 g, KCl的质量为______ g 。
3.在A+2B===C+2D的反应中,若 A、B、C的相对分子质量依次为16、32、44,则D的相对分子质量为 ( )A.4 B.36 C.18 D.无法确定
4.将镁条点燃后,伸入到装有二氧化碳的集气瓶中,发现镁条仍能继续燃烧,生成了白色的氧化镁和黑色的碳粉。该过程用化学方程式表示为: 。我们可以知道,可燃物燃烧时不一定都与 反应。
CO2+Mg 点燃 MgO+C
由干燥的氯酸钾和二氧化锰组成的混合物的质量为9.9g。把该固体混合物放到大试管中加热,反应完全后,冷却到反应前的温度,称得试管中固体物质的质量为7.2g。 (1)求原混合物中氯酸钾的质量。 (2)反应后试管中固体物质是什么?它们的质量各是多少?
解:根据质量守恒定律,生成氧气为9.9g-7.2g=2.7g 设原混合物中含氯酸钾质量为x
96
x 2.7g
245 : 96 = x : 2.7g
则MnO2的质量为9.9g - 6.9g = 3g
剩余固体中KCl的质量为7.2g - 3g = 4.2g
例5:用多少克含杂质为10%的氯酸钾反应,可制得2克氧气?
解:设需含杂质10%的氯酸钾X克
245 96
X90% 2克
答:用5.7克含杂质为10%的氯酸钾反应,可制得2克氧气。
取氯酸钾和二氧化锰的混合物15.5克,放入一大试管中加热,反应完全后冷却到反应前温度,称残余固体质量为10.7克。求生成氧气多少克?生成氯化钾多少克?
解:根据题意,生成氧气的质量为: 15.5克- 10.7克=4.8克。设生成的氯化钾的质量为x
149∶96 = x∶4.8克
x 4.8克
答:生成氧气4.8克,生成氯化钾7.45克。
149 96
化学方程式计算中几个常用公式
华师大版九年级上册第7章 内能综合与测试复习课件ppt: 这是一份华师大版九年级上册第7章 内能综合与测试复习课件ppt,共56页。PPT课件主要包含了第1节物体的内能,第2节比热容,WFs等内容,欢迎下载使用。
初中科学华师大版九年级上册第6章 电能综合与测试复习课件ppt: 这是一份初中科学华师大版九年级上册第6章 电能综合与测试复习课件ppt,共21页。PPT课件主要包含了机械能,化学能,其他形式的能,光能和其他形式的能,电功率电功,电能转化的多少,电能的量度,电磁感应发电机,电磁铁,奥斯特实验等内容,欢迎下载使用。
2021学年第5章 功和简单机械综合与测试复习ppt课件: 这是一份2021学年第5章 功和简单机械综合与测试复习ppt课件,共55页。PPT课件主要包含了知识网络,斜面可省力,WFS,机械效率公式,探究杠杆的平衡条件,研究杠杆平衡的条件,杠杆的平衡条件是,省力费距离,生活中的省力杠杆,费力省距离等内容,欢迎下载使用。













