




还剩12页未读,
继续阅读
高中化学人教版 (2019)必修 第一册第二节 氯及其化合物说课课件ppt
展开
这是一份高中化学人教版 (2019)必修 第一册第二节 氯及其化合物说课课件ppt,共20页。PPT课件主要包含了水溶性,熔沸点,黄绿色,有刺激性气味,密度比空气大,氧化性,H2O,只有酸性等内容,欢迎下载使用。
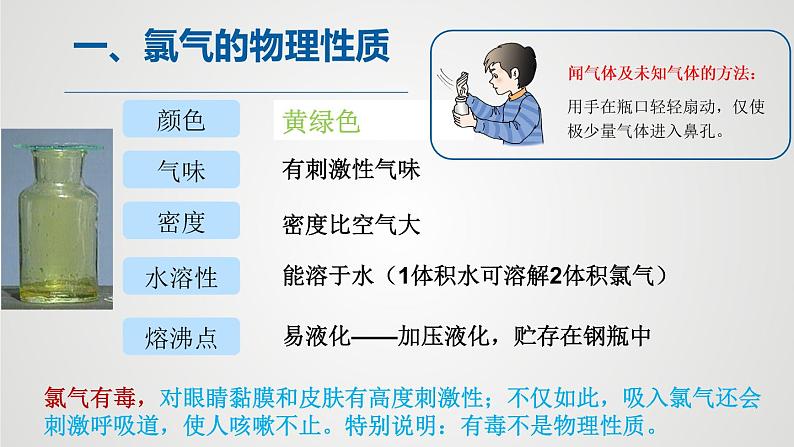
从材料中体现了氯气哪些物理性质?
京沪高速公路淮安路段液氯的泄漏2005年3月29日,京沪高速公路淮安路段一辆满载液氯的液罐车和对面来车相撞 ,大量液氯外泄。据目击者描述 : “一股黄绿色的气体 ‘唰’地射向空中,并有刺鼻的味道,眼睛也熏得睁不开 。”事发后消防队员不断地用水枪喷射,但还是造成350人中毒进医院救治, 28人中毒死亡,附近居民采取应急措施,疏散到高坡上。
能溶于水(1体积水可溶解2体积氯气)
易液化——加压液化,贮存在钢瓶中
氯气有毒,对眼睛黏膜和皮肤有高度刺激性;不仅如此,吸入氯气还会刺激呼吸道,使人咳嗽不止。特别说明:有毒不是物理性质。
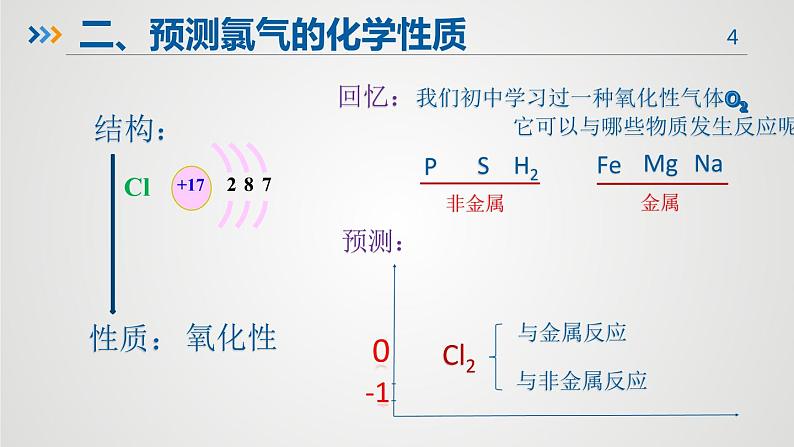
二、预测氯气的化学性质
回忆:我们初中学习过一种氧化性气体O2 它可以与哪些物质发生反应呢?
现象:黄色火焰,产生大量白烟
产生大量棕红色烟,产物的水溶液呈棕黄色
氯气与变价金属反应生成高价态吗?
产生大量棕黄色烟,水溶液呈蓝绿色
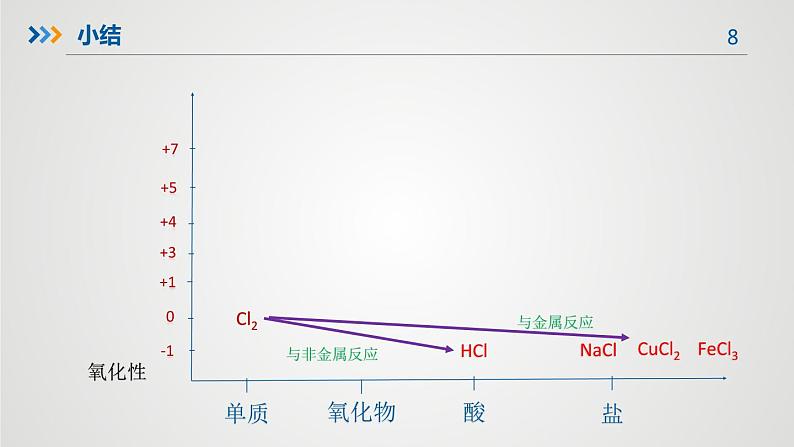
反应规律:氯气和变价金属反应时生成高价金属氯化物
三、氯气的化学性质
(2) 与非金属H2反应
实验现象:氢气在氯气中安静燃烧发出苍白色火焰瓶口有白雾出现
思考:燃烧是否一定需要氧气参加,燃烧的本质是什么?
燃烧的本质是氧化还原反应,所有发光发热的剧烈的化学反应都称为燃烧。
(3) 氯气溶于水?是简单的溶解还是发生了化学反应?
预测1:Cl2、H2O根据原子守恒,可能会生成Cl-、H+
结论:氯气溶于水发生了化学反应,生成了HCl
硝酸酸化的硝酸银产生白色沉淀
试纸变红色,之后又褪色
溶液呈现黄绿色说明存在Cl2分子。如果反应,可能会生成什么产物呢?
设计实验进行验证(演示实验):
预测2: 使试纸褪色的难道是Cl2?氯气具有漂白性吗?
实验结论:1干燥的氯气不具有漂白性,湿润的氯气具有漂白性
干燥的红色纸条放入氯气瓶中
湿润的红色纸条放入氯气瓶中
有色的鲜花放入氯气瓶中
2氯水中一定产生了一种新的漂白性物质
查阅资料:这几种物质中只有次氯酸具有漂白性
结论:Cl2 + H2O = HCl + HClO(这个反应不完全,有氯分子)
①强氧化性 (可用于漂白和杀菌消毒)②一元弱酸 (酸性HClO次氯酸(HClO)的性质
为什么氯水放久了会变质?
分析新制氯水和久置氯水的成分及性质:
Cl2 HClO H2O
H+ Cl- ClO- OH-
H+ Cl- OH-
有酸性,强氧化性,漂白性
新制氯水:三分子四离子久置氯水:相当于稀盐酸
1.下列说法中正确的是( )A.用鼻子对着盛有氯气的瓶口闻氯气的气味B.实验室里可以用排水法收集氯气C.贮氯罐意外泄漏,应沿逆风方向疏散群众D.氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域
2.下列化合物中,不能通过单质间化合直接制取的是( )A.FeCl3 B.CuCl2 C.HCl D.FeCl2
3.下列关于氯水的叙述中正确的是( )A.新制氯水中的微粒只含Cl2和H2OB.新制氯水可使蓝色石蕊试纸先变红后褪色C.光照新制氯水有气泡逸出,该气体是Cl2D.新制氯水在密闭无色玻璃瓶中放置数天后酸性将减弱
4.下列说法中,不正确的是( )A.燃烧一定伴有发光现象 B.燃烧一定是氧化还原反应C.燃烧一定要有氧气参与D.燃烧一定会放出热量
5.氯水中含有多种成分,因而具有多重性质。根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是________ (填“a”“b”“c”或“d”)(2)c过程中的现象是__________________(3)b过程中的离子方程式为________________(4)a过程中发生的反应为__________________
5 (1) d (2) 产生白色沉淀 (3) CO32- + 2H+ = CO2 + H2O (4) 2FeCl2 + Cl2 = 2FeCl3
谢谢大家! 请多指教!
从材料中体现了氯气哪些物理性质?
京沪高速公路淮安路段液氯的泄漏2005年3月29日,京沪高速公路淮安路段一辆满载液氯的液罐车和对面来车相撞 ,大量液氯外泄。据目击者描述 : “一股黄绿色的气体 ‘唰’地射向空中,并有刺鼻的味道,眼睛也熏得睁不开 。”事发后消防队员不断地用水枪喷射,但还是造成350人中毒进医院救治, 28人中毒死亡,附近居民采取应急措施,疏散到高坡上。
能溶于水(1体积水可溶解2体积氯气)
易液化——加压液化,贮存在钢瓶中
氯气有毒,对眼睛黏膜和皮肤有高度刺激性;不仅如此,吸入氯气还会刺激呼吸道,使人咳嗽不止。特别说明:有毒不是物理性质。
二、预测氯气的化学性质
回忆:我们初中学习过一种氧化性气体O2 它可以与哪些物质发生反应呢?
现象:黄色火焰,产生大量白烟
产生大量棕红色烟,产物的水溶液呈棕黄色
氯气与变价金属反应生成高价态吗?
产生大量棕黄色烟,水溶液呈蓝绿色
反应规律:氯气和变价金属反应时生成高价金属氯化物
三、氯气的化学性质
(2) 与非金属H2反应
实验现象:氢气在氯气中安静燃烧发出苍白色火焰瓶口有白雾出现
思考:燃烧是否一定需要氧气参加,燃烧的本质是什么?
燃烧的本质是氧化还原反应,所有发光发热的剧烈的化学反应都称为燃烧。
(3) 氯气溶于水?是简单的溶解还是发生了化学反应?
预测1:Cl2、H2O根据原子守恒,可能会生成Cl-、H+
结论:氯气溶于水发生了化学反应,生成了HCl
硝酸酸化的硝酸银产生白色沉淀
试纸变红色,之后又褪色
溶液呈现黄绿色说明存在Cl2分子。如果反应,可能会生成什么产物呢?
设计实验进行验证(演示实验):
预测2: 使试纸褪色的难道是Cl2?氯气具有漂白性吗?
实验结论:1干燥的氯气不具有漂白性,湿润的氯气具有漂白性
干燥的红色纸条放入氯气瓶中
湿润的红色纸条放入氯气瓶中
有色的鲜花放入氯气瓶中
2氯水中一定产生了一种新的漂白性物质
查阅资料:这几种物质中只有次氯酸具有漂白性
结论:Cl2 + H2O = HCl + HClO(这个反应不完全,有氯分子)
①强氧化性 (可用于漂白和杀菌消毒)②一元弱酸 (酸性HClO
为什么氯水放久了会变质?
分析新制氯水和久置氯水的成分及性质:
Cl2 HClO H2O
H+ Cl- ClO- OH-
H+ Cl- OH-
有酸性,强氧化性,漂白性
新制氯水:三分子四离子久置氯水:相当于稀盐酸
1.下列说法中正确的是( )A.用鼻子对着盛有氯气的瓶口闻氯气的气味B.实验室里可以用排水法收集氯气C.贮氯罐意外泄漏,应沿逆风方向疏散群众D.氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域
2.下列化合物中,不能通过单质间化合直接制取的是( )A.FeCl3 B.CuCl2 C.HCl D.FeCl2
3.下列关于氯水的叙述中正确的是( )A.新制氯水中的微粒只含Cl2和H2OB.新制氯水可使蓝色石蕊试纸先变红后褪色C.光照新制氯水有气泡逸出,该气体是Cl2D.新制氯水在密闭无色玻璃瓶中放置数天后酸性将减弱
4.下列说法中,不正确的是( )A.燃烧一定伴有发光现象 B.燃烧一定是氧化还原反应C.燃烧一定要有氧气参与D.燃烧一定会放出热量
5.氯水中含有多种成分,因而具有多重性质。根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是________ (填“a”“b”“c”或“d”)(2)c过程中的现象是__________________(3)b过程中的离子方程式为________________(4)a过程中发生的反应为__________________
5 (1) d (2) 产生白色沉淀 (3) CO32- + 2H+ = CO2 + H2O (4) 2FeCl2 + Cl2 = 2FeCl3
谢谢大家! 请多指教!













