
安徽省蚌埠市中市区2023届高三(上)摸底检测化学试题(word版,含答案)
展开安徽省蚌埠市中市区2023届高三(上)摸底检测
理科综合(化学试题)
注意事项:
1.答题前,考生务必将自己的学校、姓名、班级、准考证号填写在答题卡上相应的位置。
2.全部答案在答题卡上完成,答在本试卷上无效。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用0.5毫米及以上黑色笔迹签字笔写在答题卡上。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 S-32 Cl-35.5 Ti-48 Zn-65
第Ⅰ卷(选择题 共42分)
一、选择题(本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项符合题目要求.)
1. 化学与科学、技术、社会与环境发展息息相关。下列说法错误的是
A. 中国科学家实现了二氧化碳人工合成淀粉,该成果有利于碳中和
B. 北京冬奥会颁奖礼服内添加了石墨烯发热材料,石墨烯和C60是同位素
C. “世界铜像之王”三星堆青铜大立人属于合金,其深埋于地下生锈是发生了吸氧腐蚀
D. 北京冬奥会火炬在出火口格栅喷涂碱金属,目的是利用焰色反应让火焰可视化
2. 我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列相关说法不正确的是
A. 黄芩素的分子式为C15H12O5
B. 黄芩素分子中所有碳原子可能共平面
C. 黄芩素分子中有易被氧化的官能团,应密闭贮存
D. 27g黄芩素与氢氧化钠溶液完全反应最多消耗0.3molNaOH
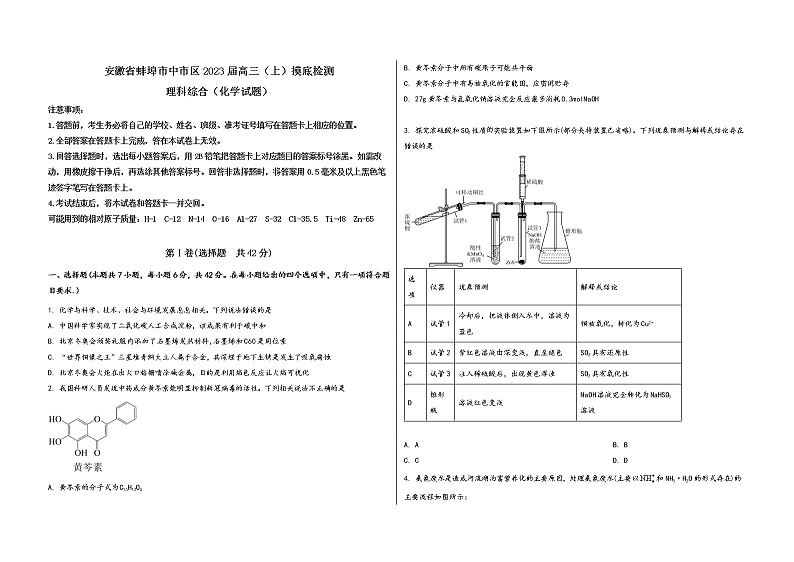
3. 探究浓硫酸和SO2性质实验装置如下图所示(部分夹持装置已省略)。下列现象预测与解释或结论存在错误的是
选项 | 仪器 | 现象预测 | 解释或结论 |
A | 试管1 | 冷却后,把液体倒入水中,溶液为蓝色 | 铜被氧化,转化为Cu2+ |
B | 试管2 | 紫红色溶液由深变浅,直至褪色 | SO2具有还原性 |
C | 试管3 | 注入稀硫酸后,出现黄色浑浊 | SO2具有氧化性 |
D | 锥形瓶 | 溶液红色变浅 | NaOH溶液完全转化为NaHSO3溶液 |
A. A B. B
C. C D. D
4. 氨氮废水是造成河流湖泊富营养化的主要原因,处理氨氮废水(主要以和NH3·H2O的形式存在)的主要流程如图所示:
下列说法不正确的是
A. 过程I降低氮元素浓度的方法:加入NaOH溶液,调节pH为碱性,升高温度,再通入空气,赶出氨气
B. 过程II是在碱性条件下通入氧气实现:→→转化,被氧气氧微生物化为 ,总反应的离子方程式: +2O2 +H2O+2H+
C. 过程III中甲醇的作用是作还原剂,将还原为N2
D. 过程III的转化过程为→→N2,每生成1molN2转移10mol电子
5. 我国科学家开发出一种离子液体(EMIES),该物质由原子序数依次增大的短周期元素X、Y、Z、R、W组成,结构如图所示,只有Y、Z、R位于同一周期,R、W原子的最外层电子数相等。下列说法正确的是
A. 原子半径:Y>Z>R>W>X
B. W的氧化物对应的水化物一定是强酸
C. EMIES中,Z、Y原子的最外层都达到8电子结构
D. 由X、Z、R三种元素组成化合物只有两种
6. 如图为一种酶生物电池,可将葡萄糖(C6H12O6)转化为葡萄糖内酯(C6H10O6),两个碳纳米管电极材料由石墨烯片层卷曲而成。下列说法正确的是
A. 图中离子交换膜为阴离子交换膜
B. 负极区发生的电极反应主要为H2-2e-=2H+
C. 碳纳米管有良好导电性能,且能高效吸附气体
D. 理论上消耗标况下2.24LO2,可生成葡萄糖内酯0.2mol
7. ROH是一元弱碱,难溶盐RA、RB的两饱和溶液中c(A-)或c(B- )随c(OH-)而变化,A-、B-不发生水解。实验发现,298 K时c2(A- )与c(OH- )或c2(B- )与c(OH- )的关系如图所示,甲表示c2(A- )与c(OH- )关系。下列叙述错误的是
A. RA饱和溶液在pH=6时,c(A- )≈1.73 ×10-5mol·L-1
B. RB的溶度积Ksp(RB)的数值为5×10-11
C. ROH的电离平衡常数Kb(ROH)的数值为2×10-6
D. 当RB的饱和溶液pH=7时,c(R+ )+c(H+ )<c(B- )+c(OH-)
第Ⅱ卷(非选择题)
二、非选择题(本题包括必考题和选考题两部分,共58分。第8题~第10题为必考题,每个试题考生都必须作答,第11题~第12题为选考题,考生根据要求作答)
(一)必考题
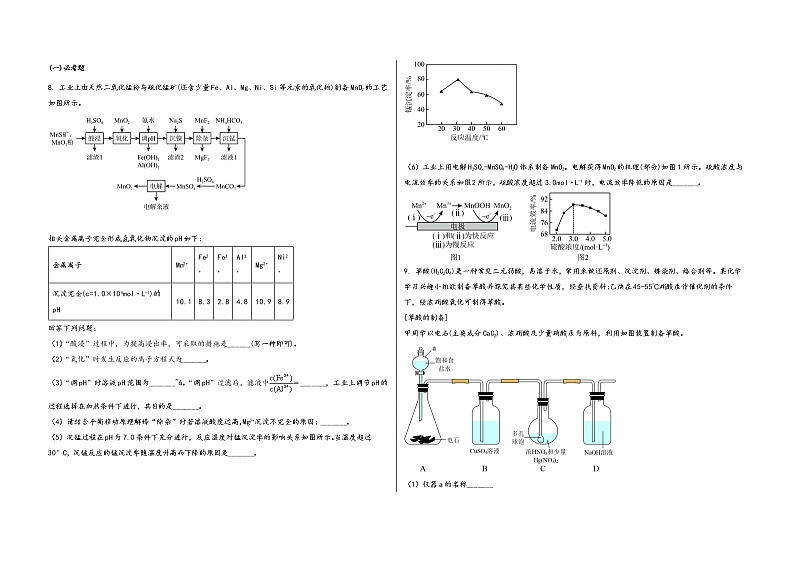
8. 工业上由天然二氧化锰粉与硫化锰矿(还含少量Fe、Al、Mg、Ni、Si等元素的氧化物)制备MnO2的工艺如图所示。
相关金属离子完全形成氢氧化物沉淀的pH如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Ni2+ |
沉淀完全(c=1.0×10-5mol·L-1)的pH | 10.1 | 8.3 | 2.8 | 4.8 | 10.9 | 8.9 |
回答下列问题:
(1)“酸浸”过程中,为提高浸出率,可采取的措施是_______(写一种即可)。
(2)“氧化”时发生反应的离子方程式为_______。
(3)“调pH”时溶液pH范围为_______~6。“调pH”过滤后,滤液中_______,工业上调节pH的过程选择在加热条件下进行,其目的是_______。
(4)请结合平衡移动原理解释“除杂”时若溶液酸度过高,Mg2+沉淀不完全的原因:_______。
(5)沉锰过程在pH为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。当温度超过30°C,沉锰反应的锰沉淀率随温度升高而下降的原因是_______。
(6)工业上用电解H2SOx-MnSO4-H2O体系制备MnO2。电解获得MnO2的机理(部分)如图1所示。硫酸浓度与电流效率的关系如图2所示,硫酸浓度超过3.0mol·L-1时,电流效率降低的原因是_______。
9. 草酸(H2C2O4)是一种常见二元弱酸,易溶于水,常用来做还原剂、沉淀剂、媒染剂、络合剂等。某化学学习兴趣小组欲制备草酸并探究其某些化学性质,经查找资料:乙炔在45-55℃硝酸汞作催化剂的条件下,经浓硝酸氧化可制得草酸。
[草酸的制备]
甲同学以电石(主要成分CaC2)、浓硝酸及少量硝酸汞为原料,利用如图装置制备草酸。
(1)仪器a的名称_______
(2)实验室制乙炔时用饱和食盐水代替水的目的是。_______。反应时C中产生大量红棕色气体,请写出C中发生化学反应方程式_______。
[产品中草酸晶体(H2C2O4·2H2O)质量分数的测定]
乙同学准确称取ag产品,配成100mL水溶液,取20mL所配制的溶液置于锥形瓶内,用cmol·L-1酸性KMnO4标准溶液滴定至终点,平行实验三次,平均消耗标准溶液vmL。试回答:
(3)上述滴定实验中发生的离子反应方程式_______,判断到达滴定终点的现象是_______。
(4)产品中草酸晶体(H2C2O4·2H2O)的质量分数为_______(用a、v表示)
[草酸的性质]
(5)上述酸性高锰酸钾与草酸反应,体现了草酸_______(填酸性、氧化性或还原性)
(6)室温下已知:Ka1(H2C2O4)=5.6×10-2,Ka2(H2C2O4)=1.5×104,通过下列实验探究草酸的性质。[1g2=0.3,lg3=0.5]。向10mL0.1mol/LH2C2O4溶液中逐滴加入VmL0.1mol/LNaOH溶液,当V从0逐渐增大至20时,测得混合溶液的pH逐渐增大,下列说法正确是_______(填字母)
A. 当V=10时,溶液中离子浓度关系:c(Na+)>c(HC2O)>c(C2O)>c(H+)>c(OH-)
B. 当溶液中c(C2O)=c(HC2O)时,混合溶液的pH约为3.8
C. 当溶液中c(C2O)+c(HC2O)=c(Na+)时,混合溶液的pH=7
D. 当溶液中c(Na+)=2c(C2O)+2c(HC2O)+2c(H2C2O4)时,混合溶液的pH>7
10. “液态阳光”是指利用太阳能等可再生能源产生的电力电解水生产“绿色”氢能并将二氧化碳加氢转化为“绿色”甲醇等液体燃料。利用加氢制甲醇等清洁燃料。是实现减排较为可行的方法。
(1)一定条件下,由和制备甲醇的反应历程如图所示:
步骤1:
步骤2:
由和制备甲醇的热化学方程式为:________,其总反应的反应速率由________决定(填“步骤1”或“步骤2”)。
(2)研究发现和制备甲醇也可以不通过CO的中间状态,我国学者在加氢制甲醇反应机理方面取得重要进展(标注“*”表示在催化剂表面吸附的物质):
上述反应历程中,合成甲醇步骤的反应方程式为:___________。
(3)和制备甲醇还存在副反应——逆水煤气变换反应。通过实验测定523K,时不同总压对甲醇产率的影响如图所示;
图中压强增大甲醇产率增大的原因是:___________。
(4)在温度为T,压强为2.8MPa的恒压密闭容。器中,通入1mol、1molCO和2mol同时发生反应1:,反应2:。达到平衡时,容器中(g)为0.8mol,CO(g)为0.6mol,此时的平衡转化率_______,反应2的压强平衡常数_____(分压=总压×物质的量分数,结果保留三位有效数字)。
(5)我国科研团队利用非贵金属催化剂,以相当低电耗在水性电解质中将和甲醇都转化为附加值产品甲酸。请写出阴极的电极反应:___________。
(二)选考题(.请考生从给出的2道题任选一题作答,并用2B铅笔在答题卡上把所选题目题号后的方框涂黑。注意所做题目的题号必修与所涂题目的题号一致,并且在解答过程中写清每问的小题号,在答题卡指定位置答题。如果多做,则每学科按所做的第一题计分。
【化学--选修3:物质结构与性质】
11. 我国硒含量居世界首位,含硒化合物与材料被广泛应用于合成化学、催化化学医学研究、环境保护、农业化学品等方面。
(1)硒原子核外电子排布式为_______
(2)人体代谢甲硒醇(CH3SeH)后可增加抗癌活性,甲硒醇分子中碳原子和硒原子的杂化类型分别是_______、_______。下表中有机物沸点不同的原因是_______。
有机物 | 甲醇 | 甲硫醇 | 甲硒醇 |
沸点/℃ | 64.7 | 5.95 | 25.05 |
(3)NaHSe可用于合成聚硒醚,NaHSe晶体类型为_______,得到NaHSe过程中生成的化学键类型为_______。聚硒醚能清除水中的铅污染,其原因是_______。
(4)硒酸是一种强酸,根据价层电子对互斥理论的推测,其阴离子空间构型是_______
(5)Na2Se的晶体结构如下图所示,其晶胞参数为anm,阿伏伽德罗常数值为NA.则Na2Se的晶胞密度为_______g·cm-3(列出计算式)。
【化学--选修5:有机化学基础】
12. 美乐托宁(G)具有调节昼夜节律、抗氧化、抗炎、抑制肿瘤生长、提高记忆和延缓衰老等作用。它的一种合成路线如下:
已知:①DMF结构简式为;②-NO2-NH2
(1)A的名称是_______。B中含有的含氧官能团的名称为_______。
(2)C到D的反应分两步进行,第一步的反应类型是_______。E的结构简式为_______。
(3)F到G反应化学方程式为_______。
(4)A的同分异构体种类较多,其中满足下列条件的同分异构体有_______种。
①分子中苯环上只有两个取代基②含有羟基③与氢氧化钠溶液反应,其中核磁共振氢谱有5组峰,峰面积之比为2:2:2:2:1的同分异构体的结构简式:_______。
(5)4-甲氧基乙酰苯胺()是重要的精细化工中间体,写出由苯甲醚()制备4-甲氧基乙酰苯胺的合成路线:_______(其他试剂任选)。
参考答案
一.选择题
1. B 2. A 3. D 4. B 5. C 6. C 7. C
二. 非选择题
8. (1)将矿物粉碎以增大接触面积、适当升高温度或适当增大硫酸浓度等
(2)2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O
(3) ①. 4.8 ②. 106:1 ③. 提高反应速率
(4)酸度过高,氟离子与氢离子结合生成弱电解质HF,氟离子浓度减小,导致镁离子沉淀不完全
(5)温度升高,NH4HCO3受热分解
(6)前两步快反应:Mn2+-e-+2H2O=MnOOH+3H+,慢反应:MnOOH-e-=MnO2+H+,从电极反应来看,H+浓度太大,不利于电极反应正向进行,MnOOH直接与H+反应,故当硫酸浓度大于3mol/L时,电流效率降低
9. (1)分液漏斗
(2)①. 减缓反应速率 ②. C2H2+8HNO3 (浓) H2C2O4+8NO2+4H2O
(3)①. 2MnO+6 H++5H2C2O4=2Mn2++10CO2↑+ 8H2O ②. 当滴入最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液由无色变为浅红色,且半分钟内不褪色
(4)1575cv/a% (1.575cv/a)
(5)还原性
(6)BD
10. (1)①. △H=-49kJ/mol ②. 步骤1
(2)
(3)相同条件下,由于反应为气体分子数减小的反应,加压有利于平衡正向移动;而副反应为气体分子数不变的反应,压强不影响平衡的移动,故增大压强,甲醇的产率升高;
(4)①. 70% ②. 2.78
(5)CO2+2e-+2H+=HCOOH
11. (1)1s22s22p63s23p63d104s24p4
(2)①. sp3 ②. sp3 ③. 三种物质都是分子晶体,结构相似,相对分子质量越大,沸点越高,甲醇分子间存在氢键所以沸点最高
(3)①. 离子晶体 ②. 离子键、共价键 ③. Se含有孤电子对,易与铅以配位键相结合
(4)正四面体
(5)
12. (1)①. 对氨基苯甲醚 ②. 醚键
(2) ①. 加成反应 ②.
(3) (4) ①. 6 ②.
(5)
安徽省和县2023届高三(上)摸底检测化学试题(word版,含答案): 这是一份安徽省和县2023届高三(上)摸底检测化学试题(word版,含答案),共7页。试卷主要包含了5 Ti-48 Zn-65等内容,欢迎下载使用。
安徽省歙县2023届高三(上)摸底检测化学试题(word版,含答案): 这是一份安徽省歙县2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65等内容,欢迎下载使用。
安徽省萧县2023届高三(上)摸底检测化学试题(word版,含答案): 这是一份安徽省萧县2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65,5%左右,其成分中含有蛋白质,5NA等内容,欢迎下载使用。












