安徽省合肥市郊区2023届高三(上)摸底检测化学试题(word版,含答案)
展开安徽省合肥市郊区2023届高三(上)摸底检测
理科综合(化学试题)
注意事项:
1.答题前,考生务必将自己的学校、姓名、班级、准考证号填写在答题卡上相应的位置。
2.全部答案在答题卡上完成,答在本试卷上无效。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用0.5毫米及以上黑色笔迹签字笔写在答题卡上。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 S-32 Cl-35.5 Ti-48 Zn-65
第Ⅰ卷(选择题 共42分)
一、选择题(本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项符合题目要求.)
1. 化学与人类生活、生产、社会可持续发展密切相关,下列有关化学知识的说法正确的是
A. 我国科学家首次利用CO2和H2人工合成淀粉 ,分子式为(C6H10O5)n,是纯净物
B. 我国火星探测器“天问一号”使用的新型SiC增强铝基复合材料是一种新型硅酸盐材料
C. 海水淡化可以缓解淡水供应危机,海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等
D. 第24届冬季奥林匹克运动会,上使用的滑雪板,其复合层用玻璃纤维制作,玻璃纤维属于天然有机高分子材料
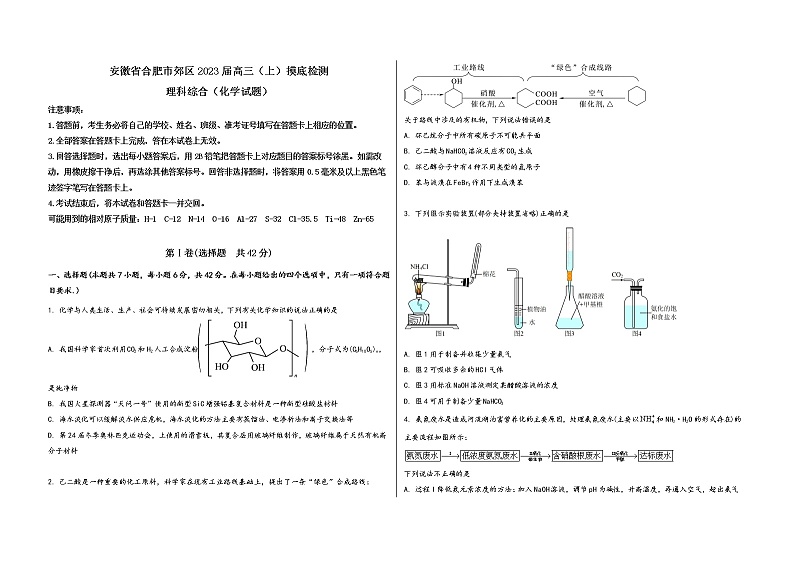
2. 己二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一条“绿色”合成路线:
关于路线中涉及的有机物,下列说法错误的是
A. 环己烷分子中所有碳原子不可能共平面
B. 己二酸与NaHCO3溶液反应有CO2生成
C. 环己醇分子中有4种不同类型的氢原子
D. 苯与液溴在FeBr3作用下生成溴苯
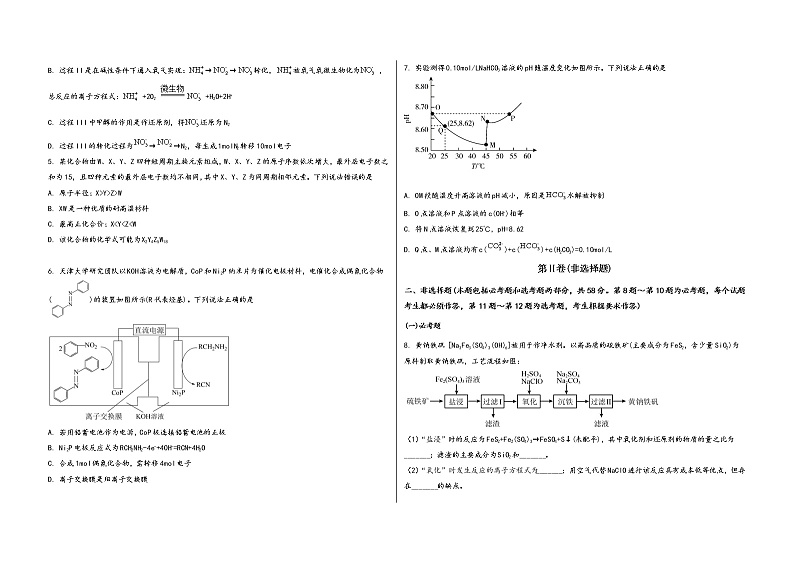
3. 下列图示实验装置(部分夹持装置省略)正确的是
A. 图1用于制备并收集少量氨气
B. 图2可吸收多余的HCl气体
C. 图3用标准NaOH溶液测定某醋酸溶液的浓度
D. 图4可用于制备少量NaHCO3
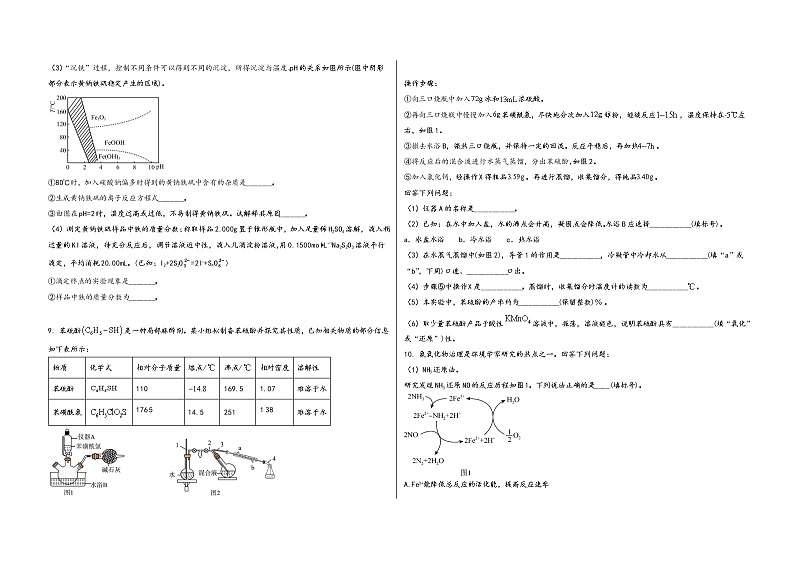
4. 氨氮废水是造成河流湖泊富营养化的主要原因,处理氨氮废水(主要以和NH3·H2O的形式存在)的主要流程如图所示:
下列说法不正确的是
A. 过程I降低氮元素浓度的方法:加入NaOH溶液,调节pH为碱性,升高温度,再通入空气,赶出氨气
B. 过程II是在碱性条件下通入氧气实现:→→转化,被氧气氧微生物化为 ,总反应的离子方程式: +2O2 +H2O+2H+
C. 过程III中甲醇的作用是作还原剂,将还原为N2
D. 过程III的转化过程为→→N2,每生成1molN2转移10mol电子
5. 某化合物由W、X、Y、Z四种短周期主族元素组成,W、X、Y、Z的原子序数依次增大,最外层电子数之和为15,且四种元素的最外层电子数均不相同,其中X、Y、Z为同周期相邻元素。下列说法错误的是
A. 原子半径:X>Y>Z>W
B. XW是一种优质的耐高温材料
C. 最高正化合价:X<Y<Z<W
D. 该化合物的化学式可能为X2Y4Z5W18
6. 天津大学研究团队以KOH溶液为电解质,CoP和Ni2P纳米片为催化电极材料,电催化合成偶氮化合物()的装置如图所示(R代表烃基)。下列说法正确的是
A. 若用铅蓄电池作为电源,CoP极连接铅蓄电池的正极
B. Ni2P电极反应式为RCH2NH2-4e-+4OH-=RCN+4H2O
C. 合成1mol偶氮化合物,需转移4mol电子
D. 离子交换膜是阳离子交换膜
7. 实验测得0.10mol/LNaHCO3溶液的pH随温度变化如图所示。下列说法正确的是
A. OM段随温度升高溶液的pH减小,原因是水解被抑制
B. O点溶液和P点溶液的c(OH-)相等
C. 将N点溶液恢复到25℃,pH=8.62
D. Q点、M点溶液均有c()+c()+c(H2CO3)=0.10mol/L
第Ⅱ卷(非选择题)
二、非选择题(本题包括必考题和选考题两部分,共58分。第8题~第10题为必考题,每个试题考生都必须作答,第11题~第12题为选考题,考生根据要求作答)
(一)必考题
8. 黄钠铁矾[Na3Fe3(SO4)3(OH)6]被用于作净水剂。以高品质的硫铁矿(主要成分为FeS2,含少量SiO2)为原料制取黄钠铁矾,工艺流程如图:
(1)“盐浸”时的反应为FeS2+Fe2(SO4)3→FeSO4+S↓(未配平),其中氧化剂和还原剂的物质的量之比为_______;滤渣的主要成分为SiO2和_______。
(2)“氧化”时发生反应的离子方程式为_______;用空气代替NaClO进行该反应具有成本低等优点,但存在_______的缺点。
(3)“沉铁”过程,控制不同条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图中阴影部分表示黄钠铁矾稳定产生的区域)。
①80℃时,加入碳酸钠偏多时得到的黄钠铁矾中含有的杂质是_______。
②生成黄钠铁矾的离子反应方程式_______。
③由图在pH=2时,温度过高或过低,不易制得黄钠铁矾。试解释其原因_______。
(4)测定黄钠铁矾样品中铁的质量分数:称取样品2.000g置于锥形瓶中,加入足量稀H2SO4溶解,滴入稍过量的KI溶液,待充分反应后,调节溶液近中性,滴入几滴淀粉溶液,用0.1500mol•L-1Na2S2O3溶液平行滴定,平均消耗20.00mL。(已知:I2+2S2O=2I-+S4O)
①滴定终点的实验现象是_______。
②样品中铁的质量分数为_______。
9. 苯硫酚是一种局部麻醉剂。某小组拟制备苯硫酚并探究其性质,已知相关物质的部分信息如下表所示:
物质 | 化学式 | 相对分子质量 | 熔点/ | 沸点/ | 相对密度 | 溶解性 |
苯硫酚 | 110 | 169.5 | 1.07 | 难溶于水 | ||
苯磺酰氯 | 1765 | 14.5 | 251 | 138 | 难溶于水 |
操作步骤:
①向三口烧瓶中加入冰和浓硫酸。
②再向三口烧瓶中慢慢加入苯磺酰氯,尽快地分次加入锌粉,继续反应,温度保持在左右,如图1。
③撤去水浴B,微热三口烧瓶,并保持一定的回流。反应平稳后,再加热。
④将反应后的混合液进行水蒸气蒸馏,分出苯硫酚,如图2。
⑤加入氯化钙,经操作X得粗品。再进行蒸馏,收集馏分,得纯品。
回答下列问题:
(1)仪器A的名称是___________。
(2)已知:在水中加入盐,水的沸点会升高,凝固点会降低。水浴B应选择___________(填标号)。
a.冰盐水浴 b.冷水浴 c.热水浴
(3)在水蒸气蒸馏中(如图2),导管1的作用是___________,冷凝管中冷却水从___________(填“a”或“b”,下同)口进、___________口出。
(4)步骤⑤中操作X是___________。蒸馏时,收集馏分时温度计的读数为___________。
(5)本实验中,苯硫酚的产率约为___________(保留整数)。
(6)取少量苯硫酚产品于酸性溶液中,振荡,溶液褪色,说明苯硫酚具有___________(填“氧化”或“还原”)性。
10. 氮氧化物治理是环境学家研究的热点之一。回答下列问题:
(1)NH3还原法。
研究发现NH3还原NO的反应历程如图1。下列说法正确的是____(填标号)。
A.Fe3+能降低总反应的活化能,提高反应速率
B.总反应为6NO+4NH3=5N2+6H2O
C.该反应历程中形成了非极性键和极性键
(2)已知有关反应如下:
①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②CO2(g)+C(s)=2CO(g) ΔH2=+172.5kJ·mol-1
③NO和CO反应的能量变化如图2所示。
2NO(g)=N2(g)+O2(g) ΔH=____kJ·mol-1。
(3)H2还原法。
已知催化剂Rh表面H2催化还原NO的反应机理如表所示,其他条件一定时,决定H2的催化还原NO反应速率的基元反应为____(填序号)。
序号 | 基元反应 | 活化能Ea/(kJ·mol-1) |
① | H2(g)+Rh(s)+Rh(s)=H(s)+H(s) | 12.6 |
② | 2NO(g)+Rh(s)=2NO(s) | 0.0 |
③ | NO(s)+Rh(s)=N(s)+O(s) | 97.5 |
④ | H(s)+O(s)=OH(s)+Rh(s) | 83.7 |
⑤ | HO(s)+H(s)=H2O(s)+Rh(s) | 33.5 |
⑥ | H2O(s)=H2O(g)+Rh(s) | 45.0 |
⑦ | N(s)+N(s)=N2(s)+Rh(s)+Rh(s) | 120.9 |
注明:N2(s)表示N2被吸附在Rh表面上。
(4)CO还原法。
一定温度下,在刚性密闭容器中充入1molNO(g)和1molCO(g)发生反应:2NO(g)+2CO(g)N2(g)+2CO2(g)。达到平衡后,再充入amolNO(g)和amolCO(g),NO的平衡转化率____(“增大”、“减小”或“不变”,下同),气体总压强____。
(5)甲烷还原法。
一定温度下,在2.0L刚性密闭容器中充入1molCH4和2molNO2,发生反应:CH4(g)+2NO2(g)CO2(g)+N2(g)+2H2O(g)。测得反应时间(t)与容器内气体总压强(p)的变化如表所示。
反应时间(t)/min | 0 | 2 | 4 | 6 | 8 | 10 |
p/(100kPa) | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
达到平衡时,NO2的转化率为____。若起始时加入3molCH4和2molNO2,则在该温度下的压强平衡常数Kp=____(以分压表示的平衡常数为Kp,分压=总压×物质的量分数)kPa。
(6)电解氧化吸收法。电解0.1mol·L-1的NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图3。当电流强度为4A时,吸收NO的主要反应的离子方程式为____(NO最终转化为NO)
(二)选考题(.请考生从给出的2道题任选一题作答,并用2B铅笔在答题卡上把所选题目题号后的方框涂黑。注意所做题目的题号必修与所涂题目的题号一致,并且在解答过程中写清每问的小题号,在答题卡指定位置答题。如果多做,则每学科按所做的第一题计分。
【化学--选修3:物质结构与性质】
11. 中国传统绘画颜料迄今已有七千多年的历史。古代艺术作品色彩艳丽,璀璨夺目,与所使用矿物颜料有很大关系。回答下列问题:
(1)石青,又名蓝矿石,化学式为Cu3(CO3)2(OH)2,基态Cu2+核外电子的空间运动状态有_______种。原子轨道中电子有两种相反的自旋状态,分别用+ 和-表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为_______。中C原子的杂化方式为_______。
(2)亚铁氰化钾,化学式为K4[Fe(CN)6],呈黄色结晶性粉末。[Fe(CN)6]4-中配体CN-的配位原子是_______(填元素符号),[Fe(CN)6]4-中。σ键和π键的数目之比为_______。
(3)宜德时期青花瓷使用的颜料“苏勃泥青”是从一种钴矿[主要成分为(FeCo)x AsS]中提取出来的。无水CoCl2的熔点是735℃ ,沸点1049℃ ,CoCl2属于_______晶体;砷酸根离子( )的空间构型为_______。
(4)ZnS可用于制白色颜料等。ZnS的晶胞如图所示。
①图中S2-的坐标有(0,0,0)、(0,,),与(0,0,0)距离最近的S2-还有_______(填坐标)。
②Zn2+占据_______ (填“八面体”或“四面体”)空隙,空隙利用率为_______%。
③ZnS的密度为_______g·cm-3(设NA为阿伏加德罗常数的值)。
【化学--选修5:有机化学基础】
12. 以芳香族化合物A为原料制备某药物中间体G的路线如图:
已知:①同一碳原子上连两个羟基时不稳定,易发生反应:RCH(OH)2→RCHO+H2O。
②R1CHO+R2CH2COOHR1CH=CHR2+CO2↑+H2O。
③
请回答下列问题:
(1)G中含氧官能团的名称为____。
(2)C→D的反应类型是____,C的分子式为____。
(3)E的结构简式为____。
(4)F→G的化学方程式为____。
(5)H是D的同分异构体,同时满足下列条件的H有____种(不包括立体异构)。
①遇氯化铁溶液发生显色反应;
②能发生水解反应;
③苯环上只有两个取代基。
其中,核磁共振氢谱显示4组峰,且峰的面积之比为3:2:2:1的结构简式为____(写一种即可)。
(6)根据上述路线中的相关知识,设计以 和乙酸为原料制备 的合成路线____。(无机试剂任选)
参考答案
一.选择题
1. C 2. C 3. D 4. B 5. C 6. B 7. D
二. 非选择题
8. (1) ①. 1:1 ②. S
(2)①. 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O ②. 空气氧化速率小
(3)①. FeOOH ②. 3Fe3++3Na++3SO+3CO+3H2O=Na3Fe3(SO4)3(OH)6↓+3CO2↑ ③. 温度过高,Fe3+水解程度增大并分解为Fe2O3导致产率低;温度过低,Fe3+水解程度小,不易生成黄钠铁矾
(4)①. 滴入最后一滴Na2S2O3溶液,溶液由蓝色变为无色,且30s内颜色不复原 ②. 8.400%
9. (1)恒压滴液漏斗
(2)a
(3)①. 平衡气压,避免烧瓶内气压过大,发生危险 ②. b ③. a
(4)①. 过滤 ②. 169.5
(5)91
(6)还原
10. (1)AC
(2)-180.5
(3)⑦
(4)①. 增大 ②. 增大
(5) ①. 75% ②. 3240
(6)2NO+3ClO-+2OH-=2NO+3Cl-+H2O
11. (1) ①. 14 ②. +或- ③. sp2
(2)①. C ②. 1:1
(3)①. 离子 ②. 正四面体形
(4)①. (,0,)和(,,0) ②. 四面体 ③. 50 ④.
12. (1)(酚)羟基、酯基
(2) ①. 取代反应 ②. C7H5BrO2
(3)
(4) ++H2O
(5)①. 9 ②. (或)
(6)
山西省阳泉市郊区2023届高三(上)摸底检测化学试题(word版,含答案): 这是一份山西省阳泉市郊区2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65, 苯硫酚是一种局部麻醉剂等内容,欢迎下载使用。
安徽省合肥市东市区2023届高三(上)摸底检测化学试题(word版,含答案): 这是一份安徽省合肥市东市区2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65,5%左右,其成分中含有蛋白质,5NA等内容,欢迎下载使用。
安徽省合肥市西市区2023届高三(上)摸底检测化学试题(word版,含答案): 这是一份安徽省合肥市西市区2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65, 2+O22+2H2O等内容,欢迎下载使用。












