
山西省高平市2023届高三(上)摸底检测化学试题(word版,含答案)
展开
这是一份山西省高平市2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65, 实验测得0,62,10ml/L等内容,欢迎下载使用。
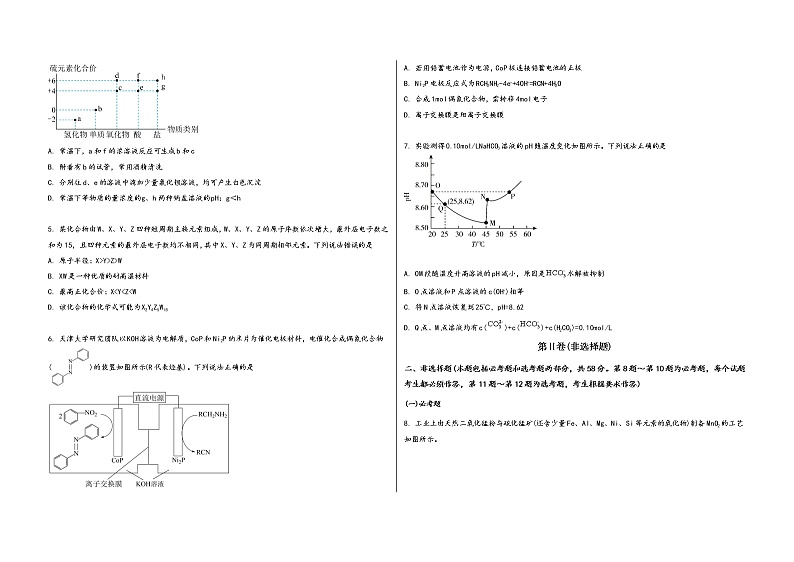
山西省高平市2023届高三(上)摸底检测理科综合(化学试题)注意事项:1.答题前,考生务必将自己的学校、姓名、班级、准考证号填写在答题卡上相应的位置。2.全部答案在答题卡上完成,答在本试卷上无效。3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用0.5毫米及以上黑色笔迹签字笔写在答题卡上。4.考试结束后,将本试卷和答题卡一并交回。可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 S-32 Cl-35.5 Ti-48 Zn-65 第Ⅰ卷(选择题 共42分)一、选择题(本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项符合题目要求.)1. 2022年北京冬奥会被誉为科技奥运绿色奥运,从清洁能源到环保材料,化学高科技所起的作用功不可没。下列有关说法错误的是A. 二氧化碳跨临界直冷制冰技术环保节能安全无毒B. 颁奖礼服内胆添加的石墨烯发热材料为有机高分子材料C. 滑雪服采用的剪切增稠流体材料可有效减小空气阻力D. 冬奥火炬“飞扬”外壳采用的是碳纤维与高性能树脂制成的新型复合材料2. 20世纪40年代,传统法合成己二酸工艺就已成熟,一直沿用至今。2020年我国科学家利用8种酶采用“一锅催化法”高效绿色合成了己二酸,其流程如图:下列说法错误的是A. 温度越高,上述2种方法合成己二酸的速率越快B. 传统法合成己二酸会产生大气污染物,原子利用率低C. “一锅催化法”属于绿色化学工艺D. 1mol己二酸与足量NaHCO3反应生成88gCO23. 根据下列实验操作和现象所得到的结论正确的是选项实验操作和现象结论 A向鸡蛋清溶液中加入几滴醋酸铅溶液,产生白色沉淀发生了蛋白质的盐析B室温下,向0.1mol/LCH3COOH溶液中加入少量镁粉,产生大量气泡,且测得溶液的温度升高反应体系的焓减小C向2mL0.1mol/LNaOH溶液中滴加5滴0.1mol/LMgSO4溶液,振荡试管,再向其中滴加10滴0.1mol/LCuSO4溶液,出现蓝色沉淀该温度下,Ksp[Cu(OH)2]<Ksp[Mg(OH)2]D在试管中加入0.5g淀粉和4mL2mol/LH2SO4溶液,加热,待溶液冷却后向其中加入NaOH溶液至碱性,再滴加少量新制Cu(OH)2,未观察到砖红色沉淀生成淀粉未发生水解 A. A B. B C. C D. D 4. 物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的价态-类别图。下列说法正确的是A. 常温下,a和f的浓溶液反应可生成b和cB. 附着有b的试管,常用酒精清洗C. 分别往d、e的溶液中滴加少量氯化钡溶液,均可产生白色沉淀D. 常温下等物质的量浓度的g、h两种钠盐溶液的pH:g<h 5. 某化合物由W、X、Y、Z四种短周期主族元素组成,W、X、Y、Z的原子序数依次增大,最外层电子数之和为15,且四种元素的最外层电子数均不相同,其中X、Y、Z为同周期相邻元素。下列说法错误的是A. 原子半径:X>Y>Z>W B. XW是一种优质的耐高温材料C. 最高正化合价:X<Y<Z<W D. 该化合物的化学式可能为X2Y4Z5W18 6. 天津大学研究团队以KOH溶液为电解质,CoP和Ni2P纳米片为催化电极材料,电催化合成偶氮化合物()的装置如图所示(R代表烃基)。下列说法正确的是A. 若用铅蓄电池作为电源,CoP极连接铅蓄电池的正极B. Ni2P电极反应式为RCH2NH2-4e-+4OH-=RCN+4H2OC. 合成1mol偶氮化合物,需转移4mol电子D. 离子交换膜是阳离子交换膜 7. 实验测得0.10mol/LNaHCO3溶液的pH随温度变化如图所示。下列说法正确的是
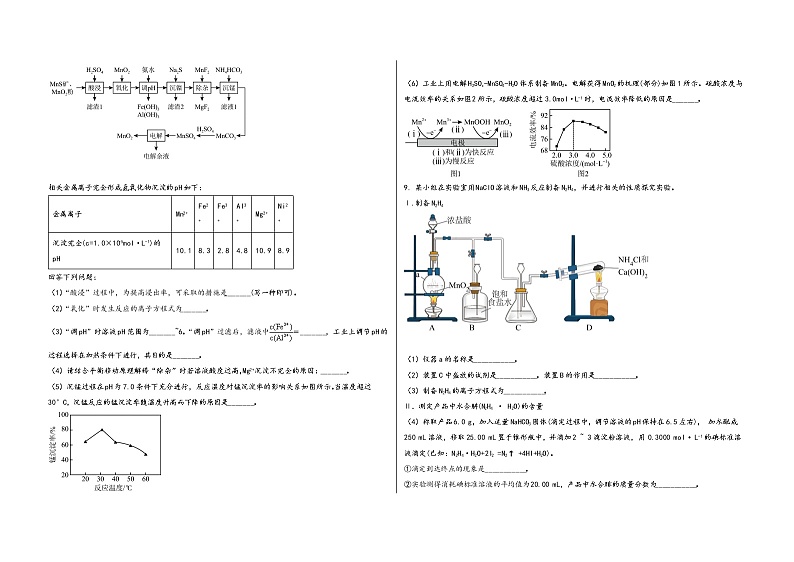
A. OM段随温度升高溶液的pH减小,原因是水解被抑制B. O点溶液和P点溶液的c(OH-)相等C. 将N点溶液恢复到25℃,pH=8.62D. Q点、M点溶液均有c()+c()+c(H2CO3)=0.10mol/L第Ⅱ卷(非选择题)二、非选择题(本题包括必考题和选考题两部分,共58分。第8题~第10题为必考题,每个试题考生都必须作答,第11题~第12题为选考题,考生根据要求作答)(一)必考题8. 工业上由天然二氧化锰粉与硫化锰矿(还含少量Fe、Al、Mg、Ni、Si等元素的氧化物)制备MnO2的工艺如图所示。
相关金属离子完全形成氢氧化物沉淀的pH如下:金属离子Mn2+Fe2+Fe3+Al3+Mg2+Ni2+沉淀完全(c=1.0×10-5mol·L-1)的pH10.18.32.84.810.98.9回答下列问题:(1)“酸浸”过程中,为提高浸出率,可采取的措施是_______(写一种即可)。(2)“氧化”时发生反应的离子方程式为_______。(3)“调pH”时溶液pH范围为_______~6。“调pH”过滤后,滤液中_______,工业上调节pH的过程选择在加热条件下进行,其目的是_______。(4)请结合平衡移动原理解释“除杂”时若溶液酸度过高,Mg2+沉淀不完全的原因:_______。(5)沉锰过程在pH为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。当温度超过30°C,沉锰反应的锰沉淀率随温度升高而下降的原因是_______。
(6)工业上用电解H2SOx-MnSO4-H2O体系制备MnO2。电解获得MnO2的机理(部分)如图1所示。硫酸浓度与电流效率的关系如图2所示,硫酸浓度超过3.0mol·L-1时,电流效率降低的原因是_______。9. 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。Ⅰ.制备N2H4
(1)仪器a的名称是___________。(2)装置C中盛放的试剂是___________。装置B的作用是___________。(3)制备N2H4的离子方程式为___________。Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。①滴定到达终点的现象是___________。②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为___________。Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。 【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。【实验验证】设计如下方案,进行实验。操作现象实验结论i.取少量黑色固体于试管中,加入适量①_________黑色固体部分溶解黑色固体有Ag2Oii.取少量黑色固体于试管中加入足量稀硝酸,振荡②_________黑色固体是Ag和Ag2O(5)请完成表中的空白部分:①___________;②___________。(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:___________。10. 研究CO2的回收及充分利用,对减少碳排放和缓解能源危机具有重要的意义。(1)在一定温度下,向1L恒容密闭容器中通入2molCO2和6molH2,在催化剂作用下可发生如下反应:2CO2(g) + 6H2(g)CH3CH2OH(g) +3H2O(g) ∆H①已知H2、CH3CH2OH(g)的燃烧热分别为285. 8KJ/mol、1366.8KJ/mol,H2O(l) =H2O(g) ∆H1=+44kJ/mol,则∆H=_______。②下列表示该反应达到平衡状态的是_______。A.混合气体的平均摩尔质量保持不变B.有6molH—H断裂同时有6molO-H断裂C.混合气体的密度不再改变D.CO2的物质的量浓度保持不变E.容器的压强保持不变③当反应经过20min达到平衡时,容器中n(CO2)与n(H2O)相等,此时H2的转化率为_______,用CH3CH2OH表示20min内该反应的反应速率为_______(2)一定温度下,以Ni/Ce为催化剂,在某恒容密闭容器中,发生反应CO2(g) +C(s)2CO(g) ,已知CO2、CO的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(CO2)=k1·P(CO2),v(CO)=k2·P2 (CO),一定温度下,k1、k2与平衡常数Kp(用平衡分压代替平衡浓度计算平衡常数)的关系是Kp=_______;v(CO2)、v(CO)与温度关系如图所示,则表示反应达到平衡状态的是_______(填TA、TB或TC)
(3)用NaOH浓溶液吸收CO2,得到Na2CO3溶液,Na2CO3溶液中各离子浓度大小关系为_______;已知:Ksp(CaCO3)=2.8×10-9,向VmL 0.001mol/LNa2CO3溶液中加入等体积CaCl2溶液,欲使CO沉淀完全,则起始CaCl2物质的量浓度至少为_______(当离子浓度小于10-5mol/L可认为沉淀完全)(二)选考题(.请考生从给出的2道题任选一题作答,并用2B铅笔在答题卡上把所选题目题号后的方框涂黑。注意所做题目的题号必修与所涂题目的题号一致,并且在解答过程中写清每问的小题号,在答题卡指定位置答题。如果多做,则每学科按所做的第一题计分。【化学--选修3:物质结构与性质】11. 目前已经确认了16种元素是植物生长所必需的,其中硼、铁、铜、钼等7种元素为必需的微量元素。回答下列问题:(1)钼位于第5周期与Cr同族,试写出钼的基态价电子排布式_______,钼位于周期表第_______纵行。(2)铁元素能与多种分子或离子形成配位键,如[FeCl2(H2O)4]+、Fe(CO)5。①[FeCl2(H2O)4]+中每个H2O的O周围σ键电子对有_______对,游离态的水中H-O-H的键角比该配离子中H-O-H的键角小,其原因是_______。②CO分子中C原子和O原子,上均存在孤电子对,在Fe(CO)5中_______(填元素符号)更容易Fe提供孤电子对。(3)硼氢化钠(NaBH4)具有很强的还原性,常用于有机合成,的VSEPR模型为_______与其互为等电子体的阳离子有_______(写一种)。(4)一种铜的溴化物立方晶胞如图所示。该化合物的化学式为_______,在晶体中与Br紧邻的Br有_______个,若Cu原子与最近的Br原子的核间距为apm,则该晶体的密度计算表达式为_______g·cm-3(用NA表示阿伏加德罗常数的值)。【化学--选修5:有机化学基础】12. 以芳香族化合物A为原料制备某药物中间体G的路线如图:
已知:①同一碳原子上连两个羟基时不稳定,易发生反应:RCH(OH)2→RCHO+H2O。②R1CHO+R2CH2COOHR1CH=CHR2+CO2↑+H2O。③请回答下列问题:(1)G中含氧官能团的名称为____。(2)C→D的反应类型是____,C的分子式为____。(3)E的结构简式为____。(4)F→G的化学方程式为____。(5)H是D的同分异构体,同时满足下列条件的H有____种(不包括立体异构)。①遇氯化铁溶液发生显色反应;②能发生水解反应;③苯环上只有两个取代基。其中,核磁共振氢谱显示4组峰,且峰的面积之比为3:2:2:1的结构简式为____(写一种即可)。(6)根据上述路线中的相关知识,设计以 和乙酸为原料制备 的合成路线____。(无机试剂任选)
参考答案一.选择题 1. B 2. A 3. B 4. A 5. C 6. B 7. D 二. 非选择题8. (1)将矿物粉碎以增大接触面积、适当升高温度或适当增大硫酸浓度等 (2)2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O (3) ①. 4.8 ②. 106:1 ③. 提高反应速率 (4)酸度过高,氟离子与氢离子结合生成弱电解质HF,氟离子浓度减小,导致镁离子沉淀不完全 (5)温度升高,NH4HCO3受热分解 (6)前两步快反应:Mn2+-e-+2H2O=MnOOH+3H+,慢反应:MnOOH-e-=MnO2+H+,从电极反应来看,H+浓度太大,不利于电极反应正向进行,MnOOH直接与H+反应,故当硫酸浓度大于3mol/L时,电流效率降低 9. (1)圆底烧瓶 (2)①. NaOH溶液 ②. 平衡气压,收集多余氯气 (3)2NH3+ClO-=N2H4+Cl-+H2O (4)①. 当加入最后一滴(或半滴)碘标准溶液时,溶液恰好变为蓝色,且半分钟内不褪色 ②. 25% (5)①. 加入足量氨水 ②. 黑色固体溶解,并有气体产生 (6)肼具有还原性将Ag+还原为Ag,肼具有碱性,与Ag+反应生成AgOH,AgOH分解生成黑色的Ag2O 10. (1)①. -216 kJ/mol ②. ABDE ③. 40% ④. (2)①. ②. TC (3) ①. c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+) ②. 5.6×10-4mol/L11. (1)①. 4d55s1 ②. 6 (2)①. 3 ②. 游离态的水分子中O原子孤电子对对σ键的斥力比该配离子水分子中O原子的σ键之间的斥力大,造成H—O—H键角减小 ③. C (3)①. 正四面体 ②. (4)①. CuBr ②. 12 ③. 12. (1)(酚)羟基、酯基 (2) ①. 取代反应 ②. C7H5BrO2 (3) (4) ++H2O (5)①. 9 ②. (或) (6)
相关试卷
这是一份山西省隰县2023届高三(上)摸底检测化学试题(word版,含答案),共7页。试卷主要包含了5 Ti-48 Zn-65, 苯硫酚是一种局部麻醉剂等内容,欢迎下载使用。
这是一份山西省盂县2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65, 实验测得0,62,10ml/L等内容,欢迎下载使用。
这是一份山西省兴县2023届高三(上)摸底检测化学试题(word版,含答案),共6页。试卷主要包含了5 Ti-48 Zn-65等内容,欢迎下载使用。








