





所属成套资源:人教版高中化学必修一同步PPT课件+教案
- 2.2《碳酸钠和碳酸氢钠》教案+课件 课件 41 次下载
- 2.3《碱金属性质及焰色试验》课件+教案 课件 36 次下载
- 2.5《氯气的实验室制备》课件+教案 课件 47 次下载
- 2.6《物质的量、阿伏伽德罗常数》课件+教案 课件 53 次下载
- 2.7《摩尔质量》课件+教案 课件 43 次下载
人教版 (2019)必修 第一册第二节 氯及其化合物评课ppt课件
展开
这是一份人教版 (2019)必修 第一册第二节 氯及其化合物评课ppt课件,文件包含24《氯气的性质》pptx、24《氯气的性质》docx等2份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
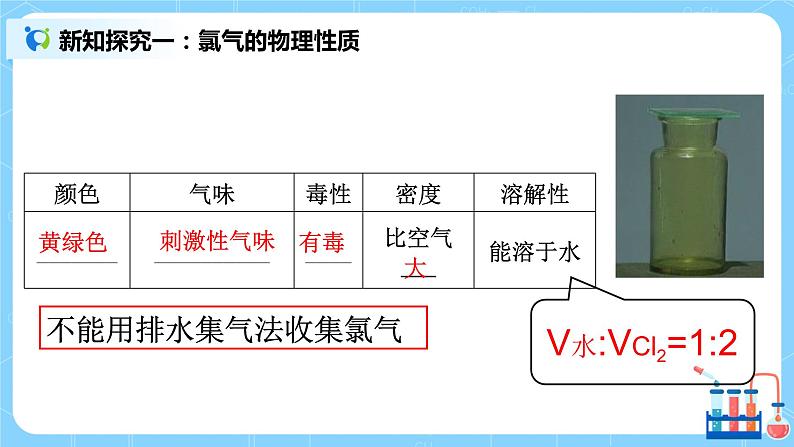
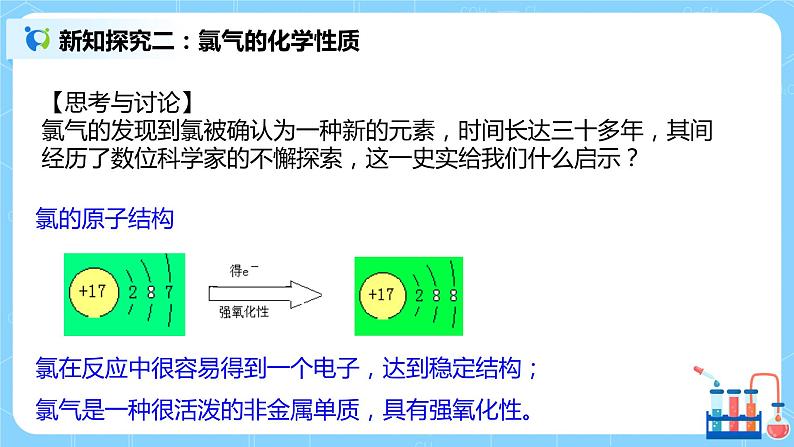
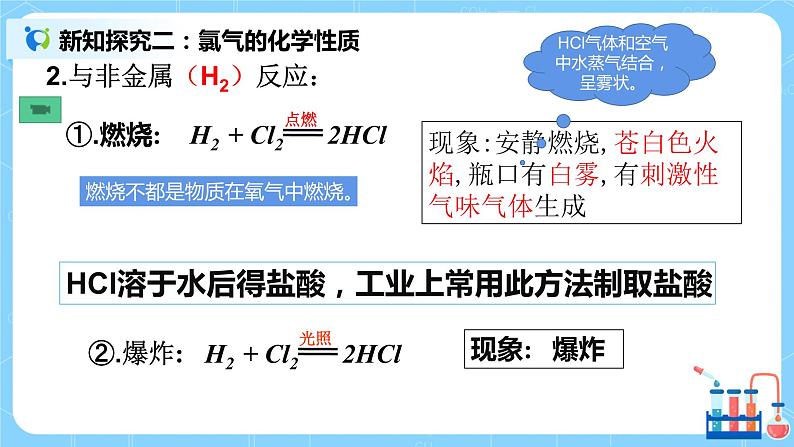
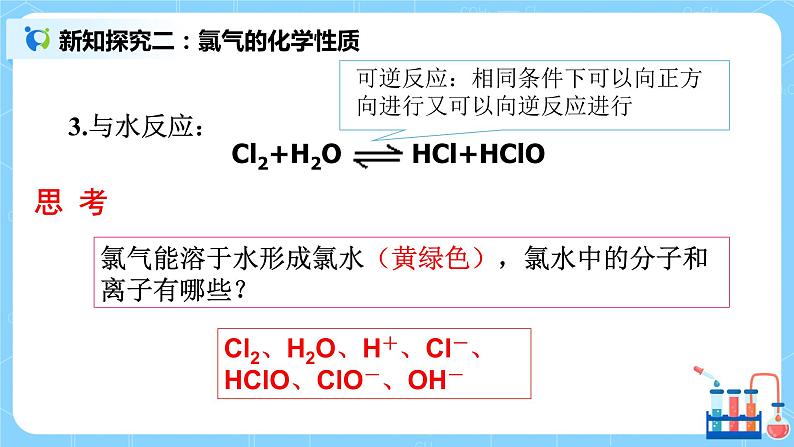
人教版化学科高一年必修一《氯气的性质》教学设计课题氯气的性质课型新授课教学目标1掌握氯气的物理性质和化学性质。 2掌握次氯酸的性质,以及氯水的制备和保存。3通过物质的学习,了解其在生活中的应用。教学重难点重点:氯气的化学性质难点:氯气的化学性质、次氯酸的性质教学环节教学过程课堂导入【新课导入】展示图片氯的单质是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、染料和药品。但氯气也是一种剧毒物质,对人的危害特别严重。某工厂发生氯气泄漏事件,消防官兵迅速出动,经过紧张奋战,终于封堵泄露点,解除危险。那么,消防官兵为什么用喷水的方法治理氯气泄漏?氯气有哪些物理性质和化学性质? 课程学习 一、 氯气的物理性质 1.通常情况下,氯气是一种黄绿色、有刺激性气味的有毒气体。 2.氯气的密度比空气大,氯气易液化――液氯――纯净物。3.氯气能溶于水,常温下,1体积水约能溶解2体积氯气。4.氯气不能用排水法收集。 二、氯气的化学性质1.【思考与讨论】氯气的发现到氯被确认为一种新的元素,时间长达三十多年,其间经历了数位科学家的不懈探索,这一史实给我们什么启示?氯原子结构:【结论】氯在反应中很容易得到一个电子,达到稳定结构;氯气是一种很活泼的非金属单质,具有强氧化性。2.化学性质(1)Cl2与金属反应——生成高价金属氯化物。 ①.与钠反应:2Na+Cl2 ===2NaCl②.与铁反应:2Fe+3Cl2 === 2FeCl3③.与铜反应:Cu + Cl2 ===CuCl2(2)Cl2与非金属反应,与H2的反应。 ①.燃烧: H2 + Cl2 ===2HCl现象:安静燃烧,苍白色火焰,瓶口有白雾,有刺激性气味气体生成【思考】燃烧的条件:燃烧不都是物质在氧气中燃烧 ②.爆炸: H2 + Cl2 ===2HCl【用途】HCl溶于水后得盐酸,工业上常用此方法制取盐酸(3)氯气与水反应。Cl2+H2O HCl+HClO a、次氯酸(HClO)的性质(1)不稳定性:2HClO === 2HCl+O2↑(2)强氧化性(漂白性)应用:能使染料和某些有机色素褪色、杀菌、消毒(净水)(3)弱酸性:HClO酸性比H2CO3 弱b、氯水(浅黄绿色、混合物)成分为: Cl2 (主), H2O, HClO, H+, Cl-, ClO-, OH-(极少c、氯水的保存:棕色试剂瓶,密封避光保存(4)Cl2与碱反应①Cl2+2NaOH = NaCl+NaClO+H2O漂白液的主要成分:NaCl、NaClO;有效成分:NaClO②2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O工业制漂白粉的原理原料:Cl2与石灰乳漂白粉的主要成分:CaCl2、Ca(ClO)2;有效成分:Ca(ClO)2漂白原理 Ca(ClO)2+H2O+CO2 = CaCO3↓+2HClO漂白粉需密封保存,放在阴凉干燥处 ; 三、课堂练习1.下列氯化物中,不能由金属和氯气直接反应制得的是( )A.CuCl2 B.FeCl2C.MgCl2 D.KCl2.用自来水养金鱼时,将水注入鱼缸以前需在阳光下曝晒一段时间,目的是( )A.使水的温度升高 B.使水中的HClO分解C.起到杀菌作用 D.增加水中含氧量3.下列说法中,正确的是( )A.液氯和氯水都含有氯离子B.氯气和液氯都能使干燥的有色布条褪色C.盐酸和氯水都含有氯离子D.盐酸和氯水都能使湿润的有色布条褪色4.下列关于氯水的叙述中正确的是(双选)( )A.新制氯水中只含Cl2和H2O分子B.新制氯水可使蓝色石蕊试纸先变红后褪色C.光照氯水有气泡逸出,该气体是Cl2D.氯水放置数天后pH将变小 课堂小结一、氯气的物理性质二、氯气的化学性质板书设计氯气的性质一、氯气的物理性质二、氯气的化学性质氯气的性质小结:与金属、与非金属、与水、与碱次氯酸的性质小结:弱酸性、强氧化性、漂白性、不稳定性教学反思情景建设导入可以极大程度吸引学生的注意力,其次演示实验将课堂氛围推向了高潮,教学过程中,注重将生活实际与教材内容联系起来,这样不仅能带动学生的学习兴趣,还能提高学生的科学文化素养。











