




人教版 (2019)必修 第一册第三节 氧化还原反应评课课件ppt
展开目录 CONTENT
一、不同角度认识氧化还原反应
二、氧化还原反应的基本概念和实质
认识有化合价变化的反应是氧化还原反应
了解氧化还原反应的本质是电子的转移
通过氧化还原反应实现含有不同价态同种元素的物质的相互转化
认识物质是运动和变化的
认识化学变化的本质是有新物质生成
从宏观和微观相结合的视角分析与解决实际问题
同学们根据初中学过的氧化反应和还原反应相应的知识,分析以下反应。
小组讨论:氧化反应和还原反应是分别独立进行的吗?
结论1:在同一个反应中:氧化反应和还原反应是同时发生的。这一类反应统称为——氧化还原反应。
请标出下列反应化合价,比较反应前后化合价的变化
+2 -2 0 0 +4-2
+3 -2 +2 -2 0 +4-2
分析上述2个反应中各种元素的化合价在反应前后有无变化,讨论氧化还原反应与元素化合价的升降有什么关系。
结论2:物质所含元素化合价升高的反应是氧化反应物质所含元素化合价降低的反应是还原反应
1.从得氧、失氧的角度认识
一、从不同角度认识氧化还原反应
①氧化铜_________氧,发生_________反应,被碳_________。②碳_________氧,发生___________反应,被氧化铜_____________。
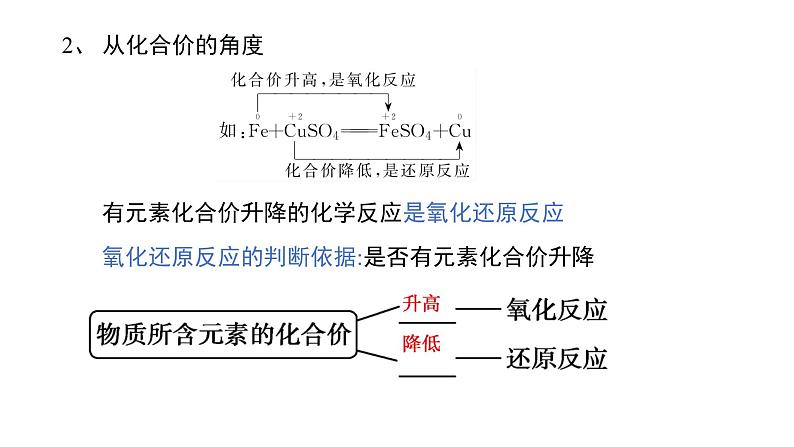
有元素化合价升降的化学反应是氧化还原反应
氧化还原反应的判断依据:是否有元素化合价升降
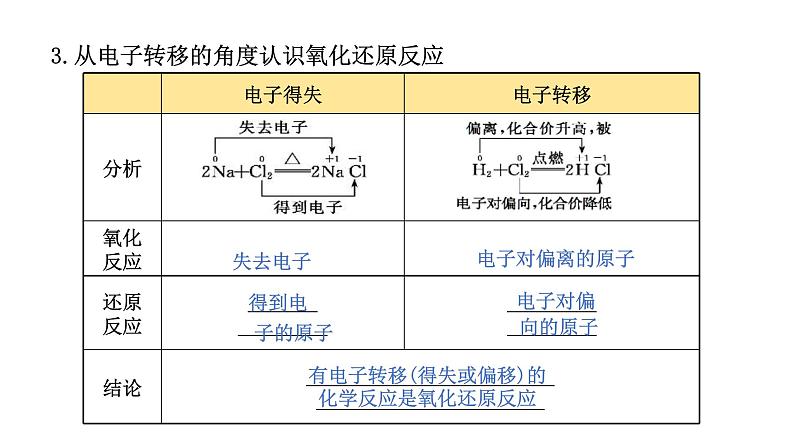
3.从电子转移的角度认识氧化还原反应
有电子转移(得失或偏移)的
化学反应是氧化还原反应
化合价降低,发生还原反应
化合价升高,发生氧化反应
化合价升高,发生氧化反应
1、并不是所有的氧化还原反应发生氧的得失,但一定会有元素化合价变化
2、元素化合价升降是氧化还原反应的重要特征,也是判断反应是否氧化还原反应的依据
下列两个反应是否属于氧化还原反应,如果是,请说明理由,并说一说你对氧化还原反应有什么新的认识?
【总结】 氧化还原反应 、化合价、电子的关系
氧化还原反应的特征: 。氧化还原反应的实质: 。
升、失、氧化降、得、还原
特征:元素化合价有升降变化;实质:电子的转移。
氧化还原反应的特征和实质是什么?
(2)实质:电子的转移(即电子的得失或偏移)。(3)特征:元素化合价发生变化。
1.基本概念和实质(1)基本概念:
2.反应中概念间的联系Fe+CuSO4===F化合价升高,被氧化eSO4+C化合价降低,被还原 (1)氧化剂在反应中化合价_____→具有_____性→被_____→生成_____产物。(2)还原剂在反应中化合价_____→具有_____性→被_____→生成_____产物。判断一个反应是否是氧化还原反应的依据是看反应中是否有元素化合价的变化。
氧化还原反应与四种基本反应类型的关系
(1)置换反应一定是氧化还原反应。(2)复分解反应一定不是氧化还原反应。(3)有单质参加的化合反应是氧化还原反应。(4)有单质生成的分解反应是氧化还原反应。
1.氧化还原反应中粒子间转化关系
氧化还原反应中的“不一定”(1)一种元素被氧化,不一定有另一种元素被还原。(2)某元素由化合态转化为游离态不一定被还原,也可能被氧化,如H2O转化为O2,氧元素被氧化,CuO转化为Cu,铜元素被还原。
氧化还原反应概念的发展:
电子转移(电子得失或共用电子对偏移)
电子的转移(电子的得失或共用电子对的偏移)
电子转移、化合价升降、反应类型的关系:
得电子→化合价降低→还原反应(得降还)
失电子→化合价升高→氧化反应(失升氧)
1.下列说法正确的是( )A.氧化还原反应的本质是元素化合价的升降B.氧化还原反应一定有氧元素参加C.氧化反应一定先于还原反应发生D.发生氧化反应的物质也可能同时发生还原反应
2.下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )A.Fe+CuSO4===FeSO4+CuB.AgNO3+NaCl===AgCl↓+NaNO3C.Fe2O3+3CO2Fe+3CO2D.2KMnO4K2MnO4+MnO2+O2↑
3.有以下5个反应(反应条件略):A.Na2O+CO2====Na2CO3B.CH4+2O2 ==== CO2+2H2OC.2KClO3 ==== 2KCl+3O2↑D.2Na+2H2O====2NaOH+H2↑E.CaCO3+2HCl====CaCl2+H2O+CO2↑
属于化合反应的有________(填字母,下同),属于分解反应的有________,属于置换反应的有________,属于复分解反应的有________________,属于氧化还原反应的有________,属于离子反应的有________。
4、在K2Cr2O7 + 14 HCl == 2KCl + 2CrCl3+ 3Cl2↑ + 7H2O反应中, 元素得电子,化合价 , 是氧化剂; 元素失电子,化合价 , 是还原剂; 被氧化, 被还原。
5、某元素在化学反应中由化合态(化合物)变为游离态(单质),则该元素( )A.一定被氧化 B.一定被还原C.可能被氧化,也可能被还原 D.以上都不是
人教版 (2019)必修 第一册第三节 氧化还原反应教案配套ppt课件: 这是一份人教版 (2019)必修 第一册第三节 氧化还原反应教案配套ppt课件,共26页。PPT课件主要包含了+1-1等内容,欢迎下载使用。
人教版 (2019)第三节 氧化还原反应精品ppt课件: 这是一份人教版 (2019)第三节 氧化还原反应精品ppt课件,共27页。PPT课件主要包含了双线桥法表示电子转移,本节重点,本节难点,氧化反应,Fe2O3,还原反应,得氧失氧,思考与讨论,发生了氧化反应,发生了还原反应等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第三节 氧化还原反应教学演示ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第三节 氧化还原反应教学演示ppt课件,共26页。PPT课件主要包含了课程导入,思考与讨论,化合价升降,共用电子对偏移,化合反应,分解反应,置换反应,复分解反应,①④⑤⑥,氧化还原反应等内容,欢迎下载使用。













