






人教版九年级化学第三单元《物质构成的奥秘》复习(共18张PPT)
展开1、构成物质的粒子有:分子、原子、离子。2、分子:保持物质化学性质的最小粒子。3、原子:化学变化中最小的粒子。4、离子:带电的原子或原子团。5、元素:具有相同质子数(核电荷数)的一类原子的总称。
1、物质是由________、________、________等微粒构成的。2、分子是保持物质______________的最小粒子;原子是_______________中最小的粒子。分子与分原子的本质区别是:在 变化中 可再分, 不可再分;3、离子是带电的________________________。4、写出下列粒子表示的意义或符号 甲 3O2-表示_________ 氮原子_____ 氯离子_____ 3个水分子_____ 2个硫原子_____5、甲元素的原子结构示意图如右: ⑴甲原子核内质子数为____,最外电子层有 个电子,这种原子容易 ________电子,形成____(填“阴”或“阳”)离子。
分子 原子 离子
1.构成物质的粒子:分子、原子、离子及它们的定义理解。2.能正确书写常用的化学用语。理解化学用语的涵义并能正确应用。
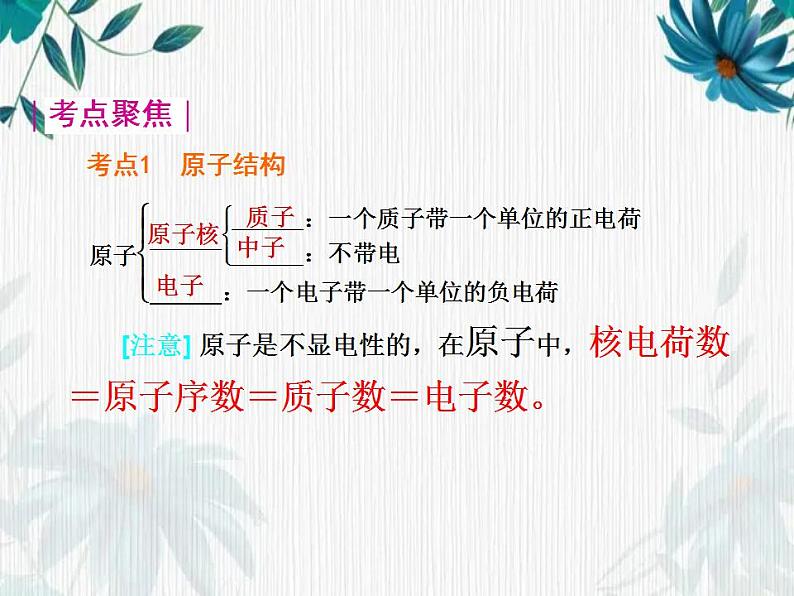
[注意] 原子是不显电性的,在原子中,核电荷数=原子序数=质子数=电子数。
第10课时┃ 考点聚焦
考点2 核外电子的分层排布
考点3 相对原子质量
[注意] ①电子质量很小,因此原子质量主要集中在原子核上。 ②相对原子质量≈质子数+中子数。
元 素
原子核(+)核外电子(-)
质子(+)中子(不带电)
相对原子质量=质子数+中子数
[例2].科学研究证明,物质是由微粒构成的。请用原子、分子或离子填空: (1)应用最广泛的铁是由铁 构成的;(2)保持氮气化学性质的是氮 ;(3)调味用的氯化钠是由钠 和氯 构成的。
[例3]. 我国在2007年发射一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3原子核是由一个中子和两个质子构成的,其原子核外电子数为( )A.1 B.2 C.3 D.6
各元素在地壳中的含量;1.地壳中各元素的质量分数由多到少排列正确的是 ( ) A.氧、铝、硅、铁 B.硅、氧、铁、铝 C.铁、铝、氧、硅 D.氧、硅、铝、铁 2.地壳中的含量最多的金属元素是 ,最多的非金属元素是 ;
元素符号的书写及其意义离子符号的书写及其意义原子(离子)结构示意图
一个离子所带的正负电荷值
一个分子中所含原子的个数
[例1]、下列微粒结构示意图表示阳离子的( )
[例2]、元素符号周围的数字有不同的含义,下列符号中只表示“2个氢原子”的是( )A、2H2 B、H2 C、 2H D、2H+
【例3】下列关于"2"的含义的解释中,正确的是( ) A.Zn2+中的"2+"表示锌粒带有2个单位的正电荷 B.2NO中的"2"表示2个一氧化氮分子 C.如H20中的“2”表示一个水分子中含有二个氢元素 D.Al2( SO4)3中化学式上方的"-2"表示3个硫酸根的化合价为-2价
1.一个原子转变为离子,发生的变化是 ( ) A.失去一定数目的电子 B.得到 一定数目的电子 C.不得电子也不失电子 D.可能得到电子也可能失去电子
2.有符号①2O ②N2 ③2Cl2 ④H3PO4 ⑤2Fe3+ ⑥SO42-,其中数字“2”表示的含义不同。则“2”用来表示原子个数的是 (填序号,下同);“2”用来表示离子个数的是 ;“2”用来表示分子个数的是 ;“2”用来表示分子构成的是 ;“2”用来表示离子所带电荷的是 ;
人教版九年级化学上册第三单元《物质构成的奥秘》期末复习PPT课件: 这是一份人教版九年级化学上册第三单元《物质构成的奥秘》期末复习PPT课件,共32页。PPT课件主要包含了构成物质的微粒,化学变化,不显电性,带正电或负电,可以再分,不可再分,原子团有时可分,化学式,元素符号,离子符号等内容,欢迎下载使用。
人教版九年级化学上册 第三单元 物质构成的奥秘复习 (共13张PPT): 这是一份人教版九年级化学上册 第三单元 物质构成的奥秘复习 (共13张PPT),共13页。PPT课件主要包含了构成的微粒,原子离子,氦原子,氮气分子,水分子,过氧化氢分子,铁原子,一原子,电子层,最外层电子数等内容,欢迎下载使用。
人教版九年级化学上第三单元 物质构成的奥秘复习课教学课件 (共29张PPT): 这是一份人教版九年级化学上第三单元 物质构成的奥秘复习课教学课件 (共29张PPT),共29页。PPT课件主要包含了考点聚焦,知识梳理,概念锦囊,第一站物质分类,小组讨论,练一练,感知中考,谢谢大家,祝愿你们梦想成真等内容,欢迎下载使用。













