




还剩23页未读,
继续阅读
高中化学人教版 (2019)选择性必修3第三章 烃的衍生物第一节 卤代烃背景图课件ppt
展开
这是一份高中化学人教版 (2019)选择性必修3第三章 烃的衍生物第一节 卤代烃背景图课件ppt,共31页。PPT课件主要包含了新课导入,醇和酚,基本概念,物理性质,化学性质,酯化反应,氧化反应,取代反应,实验3-2,试剂的作用等内容,欢迎下载使用。
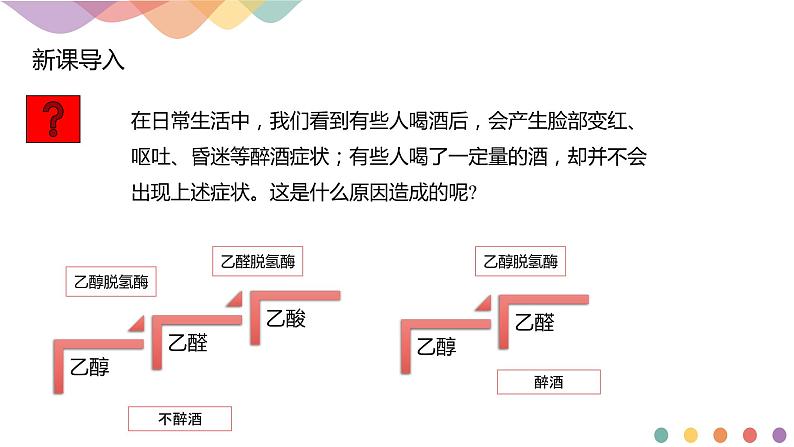
在日常生活中,我们看到有些人喝酒后,会产生脸部变红、呕吐、昏迷等醉酒症状;有些人喝了一定量的酒,却并不会出现上述症状。这是什么原因造成的呢?
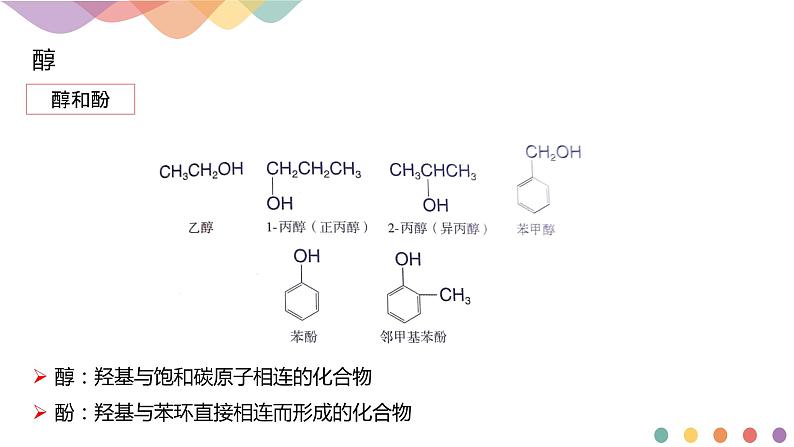
醇:羟基与饱和碳原子相连的化合物 酚:羟基与苯环直接相连而形成的化合物
概念:羟基与烃基或苯环侧链上的碳原子相连的化合物 官能团:羟基 —OH 一元醇:分子中只含有一个羟基的饱和一元醇:由烷烃所衍生的一元醇,如甲醇、乙醇;饱和一元醇的通式为CnH2n+1OH
甲醇(CH3OH)是无色、具有挥发性的液体,易溶于水,沸点为65℃。甲醇有毒,误服会损伤视神经,甚至致人死亡。甲醇广泛应用于化工生产,也可作为车用燃料。乙二醇和丙三醇都是无色、黏稠的液体,都易溶于水和乙醇,是重要的化工原料。
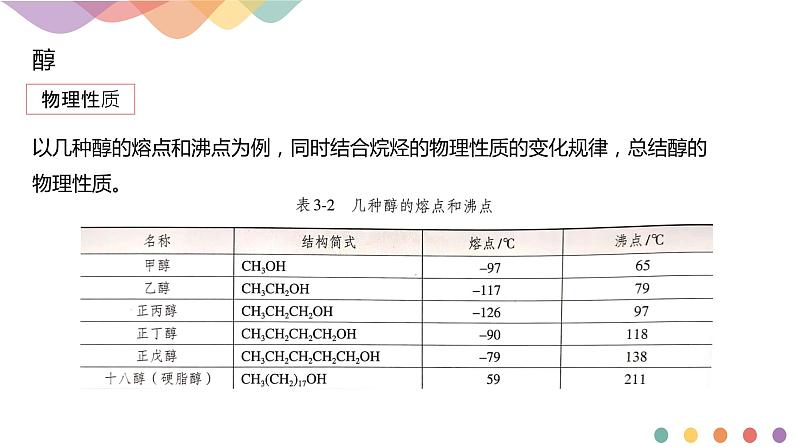
以几种醇的熔点和沸点为例,同时结合烷烃的物理性质的变化规律,总结醇的物理性质。
沸点①饱和一元醇,随分子中碳原子个数的增加,醇的沸点升高。②碳原子数相同时,羟基个数越多,醇的沸点越高。 溶解性:甲醇、乙醇、丙醇、乙二醇、丙三醇等低级醇可与水以任意比例混溶。密度:醇的密度比水的密度小。
表3-3列举了几种相对分子质量相近的醇与烷经的沸点。请仔细阅读并对比表格中的数据,你能得出什么结论?
相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃的沸点。醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着氢键。甲醇、乙醇和丙醇均可与水互溶,这也是因为醇分子与水分子之间形成了氢键。
反应方程式:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ Na与醇的反应比Na与水的反应平缓,说明水分子中—OH活性比醇中—OH的大。醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着氢键。
与活泼金属(如Na)发生反应
醇的化学性质主要由羟基官能团所决定。在醇分子中,由于氧原子吸引电子的能力比氢原子和碳原子的强,使O—H和C—O的电子都向氧原子偏移。因此,醇在发生反应时,O—H容易断裂,使羟基中的氢原子被取代,同样,C—O也易断裂,使羟基被取代或脱去,从而发生取代反应或消去反应。
醇可以与氢卤酸发生取代反应生成卤代烃和水。反应时醇分子中的C—O断裂,卤素原子取代了羟基而生成卤代烃。
乙醇与浓氢溴酸混合加热后发生取代反应,生成溴乙烷,这是制备溴乙烷的方法之一。
乙醇和浓硫酸的混合物的温度控制在140℃左右,乙醇将以另一种方式脱水,即每两个乙醇分子间会脱去一个水分子而生成乙醚。
乙醚是一种无色、易挥发的液体,沸点34.5℃,有特殊气味,具有麻醉作用 乙醚微溶于水,易溶于有机溶剂 乙醚本身是一种优良溶剂,能溶解多种有机物
醚:由两个烃基通过一个氧原子连接起来的化合物醚的官能团:
醚的结构可用R—O—R'来表示,R和R'都是烃基,可以相同,也可以不同。
在圆底烧瓶中加入乙醇和液硫酸(体积比约为1:3)的混合液20 mL,放入几片碎瓷片,以避免混合液在受热时暴沸。加热混合液,使液体温度迅速升到170℃,将生成的气体先通入氢氧化钠溶液除去杂质,再通入酸性高锰酸钾溶液和溴的四氯化碳溶液中,观察实验现象。
实验现象:酸性高锰酸钾溶液退的,溴的四氯化碳溶液褪色。 实验结论:乙醇在浓硫酸的作用下,加热到170 ℃时生成乙烯。
无水酒精和浓硫酸混合物在170 ℃的温度下主要生成乙烯和水,而在140 ℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚,故需迅速升温至170 ℃。温度计水银球要置于反应物的中央位置因为需要测量的是反应物的温度,而且不能与烧瓶接触。
吸收二氧化硫和乙醇(都与酸性高锰酸钾溶液反应,SO2能与溴的CCl4溶液反应)
浓硫酸与乙醇作用生成碳单质
乙烯与溴单质发生加成反应
乙烯被酸性高锰酸钾氧化
醇分子中,连有—OH的碳原子的相邻碳原子上连有氢原子时,才能发生消去反应而形成不饱和键。若醇分子中与—OH相连的碳原子无相邻碳原子或其相邻碳原子上无氢原子,则不能发生消去反应。如CH3OH、(CH3)3CCH2OH不能发生消去反应生成烯烃。
溴乙烷与乙醇都能发生消去反应,二者的反应有什么异同?
NaOH乙醇溶液 加热
CH2=CH2 NaBr H2O
浓硫酸,加热至170 ℃
CH2=CH2 H2O
请写出分子式为C3H8O的有机化合物的同分异构体的结构简式
CH3CH2CH2OH
CH3CH(CH3)OH
实验方案:在试管中加入酸性重铬酸钾溶液,然后滴加乙醇,充分振荡,观察实验现象。实验现象:溶液由橙红色变为绿色实验结论:乙醇能被酸性重铬酸钾溶液氧化,其氧化过程可分为两个阶段:
氧化反应:有机化合物分子中失去氢原子或加入氧原子的反应还原反应:有机化合物分子中加入氢原子或失去氧原子的反应
醇能否被氧化以及被氧化的产物的类别,取决于与羟基相连的碳原子上的氢原子的个数
总结乙醇发生化学反应时的断键位置规律
在日常生活中,我们看到有些人喝酒后,会产生脸部变红、呕吐、昏迷等醉酒症状;有些人喝了一定量的酒,却并不会出现上述症状。这是什么原因造成的呢?
醇:羟基与饱和碳原子相连的化合物 酚:羟基与苯环直接相连而形成的化合物
概念:羟基与烃基或苯环侧链上的碳原子相连的化合物 官能团:羟基 —OH 一元醇:分子中只含有一个羟基的饱和一元醇:由烷烃所衍生的一元醇,如甲醇、乙醇;饱和一元醇的通式为CnH2n+1OH
甲醇(CH3OH)是无色、具有挥发性的液体,易溶于水,沸点为65℃。甲醇有毒,误服会损伤视神经,甚至致人死亡。甲醇广泛应用于化工生产,也可作为车用燃料。乙二醇和丙三醇都是无色、黏稠的液体,都易溶于水和乙醇,是重要的化工原料。
以几种醇的熔点和沸点为例,同时结合烷烃的物理性质的变化规律,总结醇的物理性质。
沸点①饱和一元醇,随分子中碳原子个数的增加,醇的沸点升高。②碳原子数相同时,羟基个数越多,醇的沸点越高。 溶解性:甲醇、乙醇、丙醇、乙二醇、丙三醇等低级醇可与水以任意比例混溶。密度:醇的密度比水的密度小。
表3-3列举了几种相对分子质量相近的醇与烷经的沸点。请仔细阅读并对比表格中的数据,你能得出什么结论?
相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃的沸点。醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着氢键。甲醇、乙醇和丙醇均可与水互溶,这也是因为醇分子与水分子之间形成了氢键。
反应方程式:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ Na与醇的反应比Na与水的反应平缓,说明水分子中—OH活性比醇中—OH的大。醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着氢键。
与活泼金属(如Na)发生反应
醇的化学性质主要由羟基官能团所决定。在醇分子中,由于氧原子吸引电子的能力比氢原子和碳原子的强,使O—H和C—O的电子都向氧原子偏移。因此,醇在发生反应时,O—H容易断裂,使羟基中的氢原子被取代,同样,C—O也易断裂,使羟基被取代或脱去,从而发生取代反应或消去反应。
醇可以与氢卤酸发生取代反应生成卤代烃和水。反应时醇分子中的C—O断裂,卤素原子取代了羟基而生成卤代烃。
乙醇与浓氢溴酸混合加热后发生取代反应,生成溴乙烷,这是制备溴乙烷的方法之一。
乙醇和浓硫酸的混合物的温度控制在140℃左右,乙醇将以另一种方式脱水,即每两个乙醇分子间会脱去一个水分子而生成乙醚。
乙醚是一种无色、易挥发的液体,沸点34.5℃,有特殊气味,具有麻醉作用 乙醚微溶于水,易溶于有机溶剂 乙醚本身是一种优良溶剂,能溶解多种有机物
醚:由两个烃基通过一个氧原子连接起来的化合物醚的官能团:
醚的结构可用R—O—R'来表示,R和R'都是烃基,可以相同,也可以不同。
在圆底烧瓶中加入乙醇和液硫酸(体积比约为1:3)的混合液20 mL,放入几片碎瓷片,以避免混合液在受热时暴沸。加热混合液,使液体温度迅速升到170℃,将生成的气体先通入氢氧化钠溶液除去杂质,再通入酸性高锰酸钾溶液和溴的四氯化碳溶液中,观察实验现象。
实验现象:酸性高锰酸钾溶液退的,溴的四氯化碳溶液褪色。 实验结论:乙醇在浓硫酸的作用下,加热到170 ℃时生成乙烯。
无水酒精和浓硫酸混合物在170 ℃的温度下主要生成乙烯和水,而在140 ℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚,故需迅速升温至170 ℃。温度计水银球要置于反应物的中央位置因为需要测量的是反应物的温度,而且不能与烧瓶接触。
吸收二氧化硫和乙醇(都与酸性高锰酸钾溶液反应,SO2能与溴的CCl4溶液反应)
浓硫酸与乙醇作用生成碳单质
乙烯与溴单质发生加成反应
乙烯被酸性高锰酸钾氧化
醇分子中,连有—OH的碳原子的相邻碳原子上连有氢原子时,才能发生消去反应而形成不饱和键。若醇分子中与—OH相连的碳原子无相邻碳原子或其相邻碳原子上无氢原子,则不能发生消去反应。如CH3OH、(CH3)3CCH2OH不能发生消去反应生成烯烃。
溴乙烷与乙醇都能发生消去反应,二者的反应有什么异同?
NaOH乙醇溶液 加热
CH2=CH2 NaBr H2O
浓硫酸,加热至170 ℃
CH2=CH2 H2O
请写出分子式为C3H8O的有机化合物的同分异构体的结构简式
CH3CH2CH2OH
CH3CH(CH3)OH
实验方案:在试管中加入酸性重铬酸钾溶液,然后滴加乙醇,充分振荡,观察实验现象。实验现象:溶液由橙红色变为绿色实验结论:乙醇能被酸性重铬酸钾溶液氧化,其氧化过程可分为两个阶段:
氧化反应:有机化合物分子中失去氢原子或加入氧原子的反应还原反应:有机化合物分子中加入氢原子或失去氧原子的反应
醇能否被氧化以及被氧化的产物的类别,取决于与羟基相连的碳原子上的氢原子的个数
总结乙醇发生化学反应时的断键位置规律












