

初中科学浙教版九年级上册第6节 几种重要的盐第1课时课堂检测
展开第6节 几种重要的盐
第1课时 什么是盐 几种盐的性质
请判断下列说法的正误(正确的在括号内画“√”,错误的画“×”):
(1)盐是由金属离子和酸根离子组成的化合物。( )
(2)盐溶液都是显中性的。( )
(3)食盐属于盐,盐就是指食盐。( )
(4)某固体物质与稀盐酸反应产生无色无味的气体,说明此固体物质是碳酸盐。( )
(5)碳酸钠溶液显碱性,故属于碱类物质。( )
(6)碳酸钙俗称大理石或石灰石。( )
[核心知识] 盐是由金属离子(或铵根离子)与酸根离子结合形成的化合物。
[易错点拨] 常见物质的名称、俗名与化学式:
碳酸氢钠—小苏打—NaHCO3;
氢氧化钙—熟石灰—Ca(OH)2;
氢氧化钠—火碱、烧碱、苛性钠—NaOH;
氧化钙—生石灰—CaO。
1.我国化学家侯德榜创立的“侯氏制碱法”誉满全球,其中的“碱”指纯碱,也就是下列物质中的( )
A. 氢氧化钠 B.碳酸氢钠
C.碳酸钠 D.氯化钠
2.人的汗液中含有盐分,法医做指纹实验,常用某溶液喷洒指纹,你认为该溶液是( )
A. 酒精 B.碘酒
C.AgNO3溶液 D.BaCl2溶液
3.下列关于盐的用途中,叙述错误的是( )
4.Na2CO3这种盐的溶液能使无色酚酞试液变红,某同学想探究是Na+还是CO32-的作用使酚酞变红,于是设计了下列实验,其中能证明是CO32-的作用而不是Na+的作用使酚酞变红的是( )
A. 向NaOH溶液中滴入酚酞试液,观察溶液是否变红
B.向K2CO3溶液中滴入酚酞试液,观察溶液是否变红
C.向Na2CO3溶液中滴入酚酞试液后,再加入适量的盐酸,观察红色是否消失
D.向Na2CO3溶液中滴入酚酞试液,再加入适量的Ca(OH)2,观察红色是否消失
5.某溶液中可能含有碳酸钾、硫酸钾中的一种或两种溶质,为测定其成分,进行如下实验:取一定量溶液置于烧杯中,先加入过量氯化钡溶液,再加入稀硝酸,反应过程中产生沉淀的质量与所加溶液质量的关系如所示。下列说法中正确的个数有( )
①该溶液中一定含有碳酸钾和硫酸钾
②反应进行到a点时,溶液中只含有一种溶质
③bc段上的任意一点 (c点除外) 都存在两种沉淀
④反应进行到c点时,溶液中只含有两种溶质
A. 1个 B.2个 C.3个 D.4个
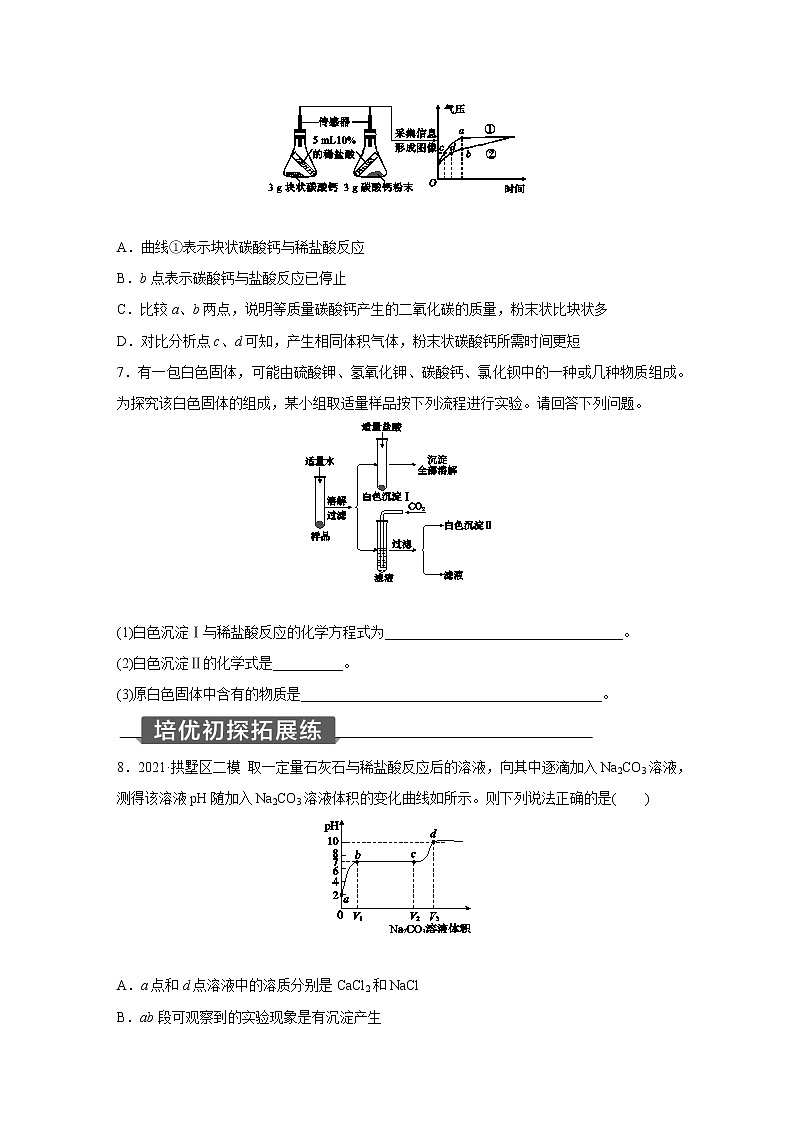
6.2021·萧山区模拟 利用数字化实验可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶使试管内的稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。有关说法正确的是( )
A.曲线①表示块状碳酸钙与稀盐酸反应
B.b点表示碳酸钙与盐酸反应已停止
C.比较a、b两点,说明等质量碳酸钙产生的二氧化碳的质量,粉末状比块状多
D.对比分析点c、d可知,产生相同体积气体,粉末状碳酸钙所需时间更短
7.有一包白色固体,可能由硫酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成。为探究该白色固体的组成,某小组取适量样品按下列流程进行实验。请回答下列问题。
(1)白色沉淀Ⅰ与稀盐酸反应的化学方程式为__________________________________。
(2)白色沉淀Ⅱ的化学式是__________。
(3)原白色固体中含有的物质是___________________________________________。
8.2021·拱墅区二模 取一定量石灰石与稀盐酸反应后的溶液,向其中逐滴加入Na2CO3溶液,测得该溶液pH随加入Na2CO3溶液体积的变化曲线如所示。则下列说法正确的是( )
A.a点和d点溶液中的溶质分别是CaCl2和NaCl
B.ab段可观察到的实验现象是有沉淀产生
C.bc段可观察到的实验现象是有气泡产生
D.cd段pH增大的原因是Na2CO3溶液过量
9.向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0% 的 Na2CO3溶液。反应过程中产生沉淀或气体的质量与加入Na2CO3溶液的质量关系如所示。下列说法正确的是( )
A. 图中Oa段表示生成沉淀的过程
B.b点溶液中溶质有两种
C.c点溶液的pH=7
D.x值为106.0
10.小江和小南同学发现实验室有两瓶标签模糊的白色粉末状药品,经询问老师,得知它们分别是K2CO3和Na2CO3,他们想通过所学知识把两种药品区分出来,在老师的指导下,设计了如甲所示的实验装置。其主要步骤如下:
①按图甲组装仪器,称量5 g样品1放入锥形瓶中,加入足量稀盐酸;
②测量一定时间内干燥管内物质增加的质量;
③再称量5 g样品2,重复以上实验。
[实验结果] 以曲线图呈现,如图乙。
[实验结论] 两位同学通过简单计算,认为样品1是________,理由是________________________________________________________________________。
[反思与拓展] 两位同学的称量无误,但在两次实验中,干燥管内物质的增重均________(填“大于”或“小于”)理论值,请你帮助他们找出一个可能的原因:________________________________________________________________________。
答案
核心·易错
(1)× 盐是由金属离子(或者铵根离子)和酸根离子组成的化合物。
(2)× 盐溶液不一定显中性,如碳酸钠溶液显碱性。
(3)× 食盐是盐中的一种,盐不仅有食盐,还包含很多其他的盐。
(4)× 能与稀盐酸反应产生无色无味气体的固体物质还有活泼金属。
(5)×
(6)× 大理石或石灰石的主要成分是碳酸钙。
能力提升拔尖练
1.C
2.C 已知“人的汗液中含有盐分”,其盐分的主要成分为氯化钠,则“法医做指纹实验,常用某溶液喷洒指纹”,可以选择含有银离子的物质,因为银离子与氯离子反应生成氯化银白色沉淀。
3.A 工业盐中含有亚硝酸钠,亚硝酸钠是有毒的物质,对人体有害,不能用工业盐制香肠;碳酸氢钠是发酵粉的主要成分;碳酸钙含有钙元素,能用于作补钙剂;氯化钠可用来配制生理盐水。
4.C 氢氧化钠中含有氢氧根离子,会有氢氧根离子的干扰;碳酸钾溶液中含有钾离子,不能排除钠、钾离子使酚酞变红;碳酸钠可以和稀盐酸反应生成二氧化碳,随着加入稀盐酸的质量的增加,碳酸根离子被反应掉,而钠离子仍然存在,至不再产生气泡时溶液的红色消失,从而可以判断是碳酸根离子使酚酞变红,而不是钠离子;氢氧化钙和碳酸钠反应会生成氢氧化钠,而氢氧化钠能够使酚酞变红。
要想证明碳酸钠溶液中能使无色酚酞试液变红的是钠离子还是碳酸根离子,则选择试剂时要加入含有钠离子且阴离子不产生干扰的物质,或者加入含有碳酸根离子且阳离子不产生干扰的物质,或者加入试剂消耗掉碳酸根离子。
5.C 分析图像,加入氯化钡溶液有沉淀生成,加稀硝酸沉淀部分溶解,说明原溶液含有碳酸钾和硫酸钾;a点时,沉淀最多,说明加入的氯化钡与碳酸钾和硫酸钾恰好完全反应,此时溶液中溶质只含有氯化钾;加入稀硝酸时,碳酸钡开始溶解,未到c点时,两种沉淀都有,到c点时沉淀只有硫酸钡,溶质有氯化钾、氯化钡和硝酸钡。
6.D 对比分析a、b点可知,曲线①单位时间内气压大,说明单位时间内产生的气体多,反应速率快,曲线①表示粉末状碳酸钙与稀盐酸反应。b点之后气压继续增大,b点表示碳酸钙与盐酸反应没有停止。对比分析a、b点可知,曲线①单位时间内气压大,说明单位时间内产生的气体多,反应速率快,即相同的时间内,粉末状的碳酸钙产生的二氧化碳多。对比分析c、d点可知,产生相同体积气体,粉末状所需时间更短。
7.(1)CaCO3+2HCl===CaCl2+H2O+CO2↑
(2)BaCO3
(3)CaCO3、BaCl2和KOH
由样品加水溶解所得的沉淀Ⅰ遇盐酸全部溶解可知,该沉淀是碳酸钙沉淀,而不是硫酸钡沉淀,所以样品中一定存在碳酸钙,且只含有硫酸钾和氯化钡中的一种。由“向第一步的滤液中通入CO2后产生白色沉淀”可知,样品中一定含有氢氧化钾和氯化钡(氢氧化钾与CO2反应生成碳酸钾,碳酸钾与氯化钡反应生成碳酸钡沉淀),同时可确定样品中一定不含硫酸钾。
培优初探拓展练
8.D a点是加入碳酸钠溶液前,此处溶液中的溶质是反应生成的氯化钙和过量的氯化氢;ab段是碳酸钠和稀盐酸反应,生成二氧化碳气体,因此可观察到的实验现象是有气泡产生;bc段是碳酸钠和氯化钙反应生成碳酸钙和氯化钠,有沉淀生成;碳酸钠溶液显碱性,cd段pH上升的原因是碳酸钠过量。
9.D 图中Oa段表示生成气体的质量;b点表示碳酸钠恰好完全反应,溶液中只含有NaCl一种溶质;c点的溶液中含有Na2CO3、NaCl两种溶质,由于Na2CO3显碱性,NaCl显中性,所以c点溶液的pH>7;根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成二氧化碳气体2.2 g,碳酸钠与氯化钙反应生成碳酸钙沉淀5.0 g。设生成2.2 g二氧化碳所需Na2CO3的质量为y,生成5.0 g碳酸钙所需Na2CO3的质量为z。则:
Na2CO3~CO2
106 44
y 2.2 g
= y=5.3 g
Na2CO3~CaCO3
106 100
z 5.0 g
= z=5.3 g
所以x==106.0。
10.[实验结论] Na2CO3 等质量的Na2CO3和K2CO3与足量的稀盐酸反应,Na2CO3所产生的CO2质量大于K2CO3所产生的CO2质量
[反思与拓展] 小于 稀盐酸滴入过快,CO2没有被完全吸收(合理即可)
[实验结论] Na2CO3~CO2
106 44
K2CO3~CO2
138 44
可知等质量的Na2CO3和K2CO3与足量的稀盐酸反应,Na2CO3所产生的CO2质量大于K2CO3,所以样品1是碳酸钠。[反思与拓展] 两位同学的称量无误,但在两次实验中,干燥管内物质的增重小于理论值,出现这种现象的可能的原因很多,如稀盐酸滴入过快,CO2没有被完全吸收等。
初中科学第1节 食物与营养第1课时同步练习题: 这是一份初中科学第1节 食物与营养第1课时同步练习题,共7页。
科学九年级上册第2节 机械能第1课时课后练习题: 这是一份科学九年级上册第2节 机械能第1课时课后练习题,共8页。试卷主要包含了请判断下列说法的正误,有下列物体,中属于势能逐渐变大的一组是,如所示为农用扬场机的示意图等内容,欢迎下载使用。
浙教版九年级上册第5节 物质的转化第1课时练习: 这是一份浙教版九年级上册第5节 物质的转化第1课时练习,共7页。













