
初中化学沪教版九年级上册第3节 金属防护和废金属回收教学设计
展开1.知道钢铁的锈蚀条件。
2.掌握防止金属锈蚀的简单方法。
3.了解废弃金属对环境的污染,认识回收废金属的重要性。
4.提高资源意识和环保意识。
【重点和难点】
铁生锈的条件探究
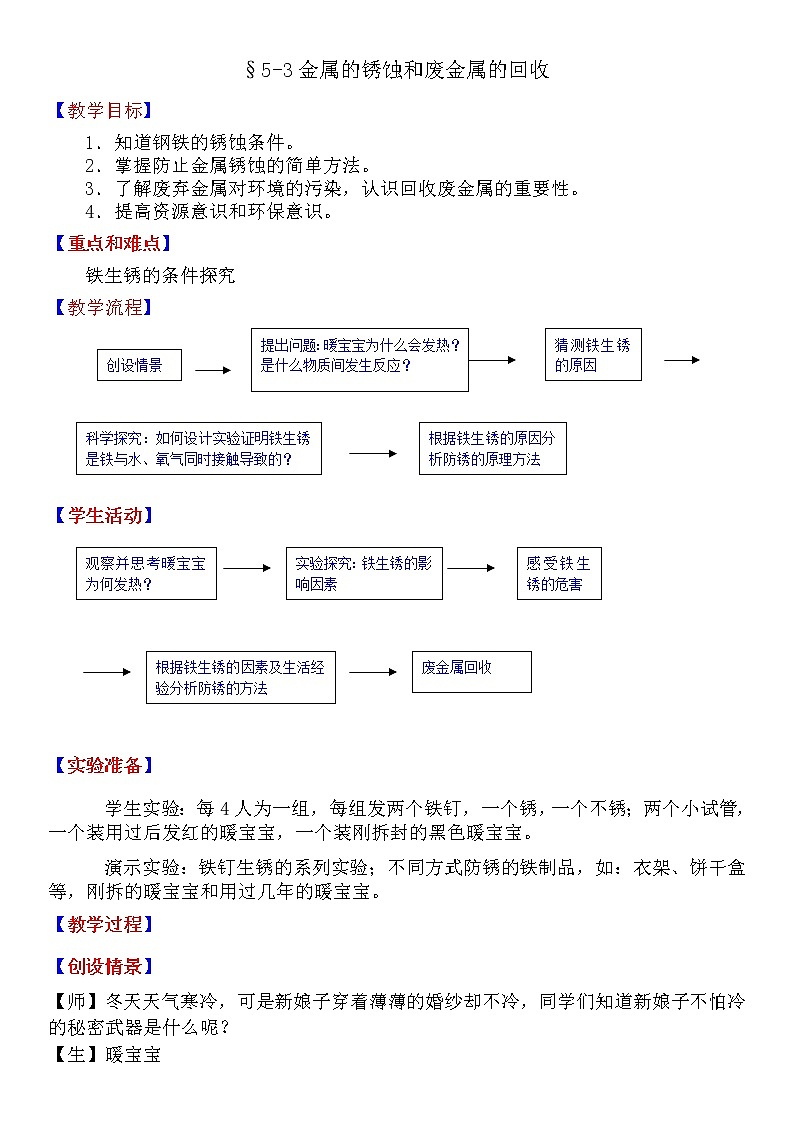
【教学流程】
猜测铁生锈的原因
创设情景
提出问题:暖宝宝为什么会发热?是什么物质间发生反应?
根据铁生锈的原因分析防锈的原理方法
科学探究:如何设计实验证明铁生锈是铁与水、氧气同时接触导致的?
【学生活动】
感受铁生锈的危害
实验探究:铁生锈的影响因素
观察并思考暖宝宝为何发热?
废金属回收
根据铁生锈的因素及生活经验分析防锈的方法
【实验准备】
学生实验:每4人为一组,每组发两个铁钉,一个锈,一个不锈;两个小试管,一个装用过后发红的暖宝宝,一个装刚拆封的黑色暖宝宝。
演示实验:铁钉生锈的系列实验;不同方式防锈的铁制品,如:衣架、饼干盒等,刚拆的暖宝宝和用过几年的暖宝宝。
【教学过程】
【创设情景】
【师】冬天天气寒冷,可是新娘子穿着薄薄的婚纱却不冷,同学们知道新娘子不怕冷的秘密武器是什么呢?
【生】暖宝宝
【师】同学们用过暖宝宝吗?为啥暖宝宝能发热呢?
【生】因为正在发生化学反应,而这个反应是放热的。
【师】究竟是什么物质在反应呢?我们来看看他的成分?
【多媒体投影】:暖宝宝的成分有:铁、氯化钠、水等
【师】暖宝宝中的铁是粉末状的,简称为铁粉。同学们观察一下刚拆封的暖宝宝内固体的颜色状态是怎么样的?
【生】黑色固体。
【师】能否用简单的物理方法检测一下铁粉的存在?
【生】用磁铁吸。
【师演示实验】用磁铁吸引刚开封的暖宝宝,固体能被吸引。
【师】实验也证明了暖宝宝中有铁粉。
【师】为什么塑料袋不打开暖宝宝就不热?
【生】塑料袋打开后空气可以进去了,可能与空气中成分发生了反应。
【师】你觉得空气中什么成分可能参与反应了呢?
【生】氧气
【师】为什么不是氮气呢?
【生】氧气的化学性质比较活泼,而氮气的化学性质比较稳定。
【师】暖宝宝发热就是在发生化学变化,发生了什么样的化学变化呢?请同学们观察一下纸包里的已经用过的暖宝宝,发现它的颜色有啥变化?
【生】变红色。
【师】再观察一下桌子上的两支铁钉什么颜色?
【生】一支不锈的银白色,一支生锈的红褐色。
【师】看来暖宝宝发热,就是铁粉生锈产生。根据生活经验,接触什么物质会导致铁生锈呢?
【生】氧气、水
【师】是铁单独接触氧气或水就会生锈还是同时接触氧气和水才会生锈呢?
【生】同时接触
【师】你能设计实验证明你的猜测吗?
【生】学生小组讨论方案,学生交流汇报。
【师】我们设计时,看氧气是否是必须的因素,一个试管内只有铁和氧气看是否生锈;分析水是否是必须的因素,我们设计方案时一个试管内只有铁和水看是否生锈;看是否水和氧气同时接触,我们设计实验时一个试管内有铁、水、氧气。这是正向思维。
【师】我们还可以反向思维:看某个因素是否必须,设计时故意缺了它,看铁会不会生锈。如看水这个因素,设计时故意没有水,如果铁也生锈了,说明水不是必须的。
【师】设计了方案,我们用实验来验证。
【展示实验】试管1有氧气无水,不生锈;试管2,有水无氧气,不生锈;
试管3有铁、有水、有氧气,生锈了。
【师】说明铁生锈的必要条件是:铁与水、氧气同时接触。
【师】铁的生锈是个缓慢氧化的过程,该反应放热,所以铁钉生锈的实验往往要几天后才能看到现象,但为什么暖宝宝一般5分钟左右就能感受热,为什么反应这么快呢?是什么加快了这个反应呢?
【师】回顾第一章铁生锈的实验中会什么要加一些食盐水?钢铁大轮在海水中为什么比淡水中容易生锈?刚才暖宝宝的成分中的食盐有啥用途呢?
【生】可能食盐加快了铁生锈。
【师】是的。食盐能加快铁生锈。我们还发现实验室里放酸的仪器的橱柜里的铁器总是特别容易锈掉,又是为什么呢?
【生】酸也加快生锈
【师】是的,氯化钠、酸都能加快铁的生锈。请同学们观察一下铁钉碰到食盐、酸生锈情况。
【展示实验】
【师】通过实验说明食盐、酸溶液能加快铁的生锈。
【师】少量的酸能加快铁生锈,如果铁钉浸在多量的酸中会怎么样呢?
【生】会直接把铁溶解掉,反应生成氢气。
【师】确实如此。铁锈有什么特点呢?请同学们观察发的两个铁钉的颜色状态,用手指分别摸一下,看看手上留下的是什么?
【生】手上留下红色,说明铁锈比较疏松,颜色是红棕色的。
【展示】各种生锈的铁器。
【师】铁锈疏松多孔,水和空气容易进入铁锈中,向内层渗透,持续跟铁反应,直至把铁完全锈蚀,所以俗称锈吃铁。铁锈成分复杂,是混合物,且锈的程度不同,颜色也有所不同,但铁锈的主要成分氧化铁是红棕色的。
【师】铁锈如何除去?
【师】用砂皮打磨,还可以用酸洗,该方法将在下学期第七章学习。
【师】铁生锈,究竟好不好呢?
【生】不好
【师】为什么不好?
【生】买的冰箱很快锈了,会不开心的。生锈会导致铁损失。
【师】是的。钢铁是当今世界用途最广的金属,每年因为生锈而损耗的铁约占产量的十分之一,造成大量的资源的浪费和损失,甚至造成严重的事故。(PPT出示事故报道)铁生锈导致的危害和损失比较大。如果家里买的汽车锈了,刹车锈了坏了,不能用了。都会让我们不开心。
【师】但是铁生锈这个反应是否有帮我们人类提供正能量的方面呢?
【生】暖宝宝。
【师】是的。利用铁生锈放热做成暖宝宝;吸氧剂利用铁生锈吸掉月饼包装袋内氧气,使月饼保存的时间长一点。这些是对我们有利的一面。可见,我们有了知识才能利用化学反应更好的为人类服务。
【师】相对来说,铁生锈对人类造成的损失更大,所以研究如何防止铁生锈就显得非常有必要。
【师】请同学们根据铁生锈的原理讨论一下钢铁防锈的原理和防锈的方法;
【呈现各种防锈的铁器】
【生1】隔绝空气和水
【生2】涂油、刷漆
【生3】镀其他金属、表面包塑料
【师】防锈的原理就是隔绝空气和水;单独隔绝一种很好,如果两种一起隔绝更好。
【师】具体的铁制品防锈方法可以归纳为三招:1、保持铁制品的洁净和干燥,我们形象的称之为注意个人卫生; 2、在钢铁制品表面覆盖保护膜:(1)可以在铁制品表面涂油、油漆或烧制搪瓷、覆盖塑料、镀其他金属,如锌、锡、铬等.;用化学方法使铁制品表面生成一层致密而稳定的氧化膜。第二招我们称为:穿好衣服,做好防护;3.改变钢铁内部结构,做成合金,如不锈钢。第三招我们称为:改善体质,增强抵抗力。
【师】有的锈的实在不行的铁器怎么办?
【生】回收
【师】废金属是放错地方的资源。非金属的回收利用具有很大的意义。请同学们讨论学习废金属回收的意义。
【生】节约资源、保护环境
【小结】
【课外延伸】铜生锈就变成铜绿,即碱式碳酸铜Cu2(OH)2CO3,请同学们分析铜生锈的条件?如何设计实验来证明你的猜测呢?考虑反向思维的设计方法。
【板书设计】
第三节金属防护和废金属回收
一、钢铁的锈蚀及其防护
1.铁生锈的原因: 铁与水、氧气同时接触;
氯化钠、酸溶液等物质加快生锈
2.防止铁生锈的原理:隔绝空气
方法:保持铁制品洁净和干燥
涂保护层
制成不锈钢
二、废金属的回收利用
1.废金属的危害 2.回收利用的意义:节约资源、保护环境
备注:本教案是特级教师后备班培训时的公开课
沪教版九年级上册第3节 金属防护和废金属回收教案: 这是一份沪教版九年级上册第3节 金属防护和废金属回收教案,共6页。教案主要包含了设计思想,教材分析,教法分析,学法分析,教学程序,教后反思等内容,欢迎下载使用。
初中化学北京课改版九年级上册第三节 化合价教案: 这是一份初中化学北京课改版九年级上册第三节 化合价教案,共3页。教案主要包含了创设情境,引入新课,学生活动,练习提升,规律总结,学生回顾、自主总结,当堂检测,能力提升等内容,欢迎下载使用。
2021学年第5章 化学元素与物质组成的表示综合与测试教案: 这是一份2021学年第5章 化学元素与物质组成的表示综合与测试教案,共5页。教案主要包含了教学目标,教学重点,教学难点,教学媒体,教学过程等内容,欢迎下载使用。













