





所属成套资源:新人教版化学选择性必修1课件PPT全套
- 专题18 原电池 (3)- 名校同步2022-2023学年高二化学疑难点突破实用课件(人教版2019选择性必修1) 课件 2 次下载
- 专题19 电解池 (1)- 名校同步2022-2023学年高二化学疑难点突破实用课件(人教版2019选择性必修1) 课件 2 次下载
- 专题20 电解池 (2)- 名校同步2022-2023学年高二化学疑难点突破实用课件(人教版2019选择性必修1) 课件 1 次下载
- 专题21 电解池 (3)- 名校同步2022-2023学年高二化学疑难点突破实用课件(人教版2019选择性必修1) 课件 1 次下载
- 专题23 金属的腐蚀与防护(2)- 名校同步2022-2023学年高二化学疑难点突破实用课件(人教版2019选择性必修1) 课件 1 次下载
高中化学人教版 (2019)选择性必修1第三节 金属的腐蚀与防护完美版课件ppt
展开
这是一份高中化学人教版 (2019)选择性必修1第三节 金属的腐蚀与防护完美版课件ppt,共15页。PPT课件主要包含了铜器生锈,M-ne-Mn+,化学腐蚀,电化学腐蚀,金属的腐蚀,1化学腐蚀,Fe2O3·xH2O,2电化学腐蚀,无电流产生,有微弱电流产生等内容,欢迎下载使用。
金属的腐蚀在生活中非常普遍
主要成分:Fe2O3 · xH2O
铜绿的主要成分:Cu2(OH)2CO3
【资料】——金属的腐蚀的危害
面对这样惊人的数据和金属腐蚀危害事实,大家有没有想过,铁怎么会被腐蚀?怎样防腐?
我国每年因为金属腐蚀所造成的经济损失约占国民生产总值的5%,全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4,超过每年各项大灾(火灾、风灾及地震等)损失的总和。
1、什么是金属的腐蚀? 2、金属腐蚀的实质是什么? 3、一般金属的腐蚀可分为几种?各有什么特点?
【自主学习-P107】
是指金属或合金跟接触的气体或液体发生氧化还原反应而腐蚀损耗的过程。
金属或合金跟接触的气体或液体发生氧化还原反应而腐蚀损耗的过程。
其本质是金属原子失去电子被氧化的过程。
M-ne- = Mn+
金属跟接触到的干燥气体(如O2、Cl2、SO2等)或非电解质液体(如石油)等直接发生化学反应而引起的腐蚀。
输送原油的钢管在无水、无氧的情况下被腐蚀而漏油
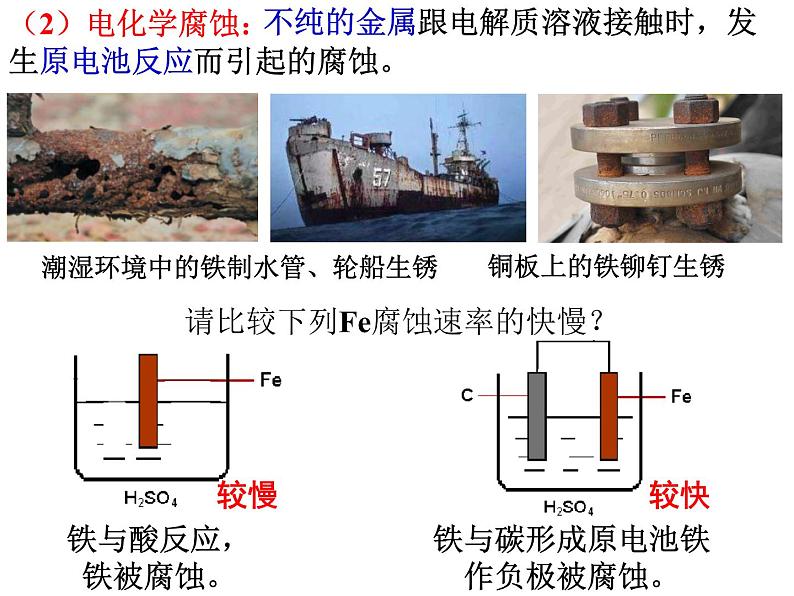
不纯的金属跟电解质溶液接触时,发生原电池反应而引起的腐蚀。
请比较下列Fe腐蚀速率的快慢?
铁与酸反应,铁被腐蚀。
铁与碳形成原电池铁作负极被腐蚀。
较慢 较快
潮湿环境中的铁制水管、轮船生锈
化学腐蚀与电化学腐蚀的比较
金属与氧化性物质直接接触
不纯金属与电解质溶液及氧化剂接触
通常情况下,两者同时存在,以电化学腐蚀为主
【探究1】潮湿环境中钢铁生锈原理探究
装置中铁、碳和盐酸构成原电池,铁钉发生析氢腐蚀腐蚀
导管中有水柱下降,铁钉表面有铁锈生成
正极: 2H++ 2e- =H2 ↑
负极: Fe - 2e- = Fe2+
总反应:Fe + 2H+ =Fe2+ + H2 ↑
装置中铁、碳和饱和食盐水构成原电池,铁钉发生吸氧腐蚀腐蚀
导管中有水柱上升,铁钉表面有铁锈生成
【实验4-3】潮湿环境中钢铁生锈原理探究
负极:2Fe - 4e- = 2Fe2+
正极:O2 + 2H2O + 4e-= 4OH-
总反应: 2Fe+ O2+2H2O =2Fe(OH)2
条件:弱酸性或中性或碱性
或2Fe- 4e- +4OH- =2Fe(OH)2
装置中进一步反应: 4Fe(OH)2 +O2 + 2H2O =4 Fe(OH)3 2Fe(OH)3=Fe2O3·xH2O+(3-x) H2O
2H+ + 2e− = H2↑
想一想:为什么钢铁吸附的水膜呈现不同性质的时候,正极的电极反应不同?
pH=2.0、3.0、3.5:
O2 + 4e− + 4H+ = 2H2O
写出pH=2.0~3.5和4.0时发生的主要正极反应。
【创新实验】不同pH下,试管中气体压强随时间变化情况
水膜呈弱酸性或中性或碱性
Fe-2e-=Fe2+
2Fe- 4e- = 2Fe2+或
O2+2H2O+4e- =4OH-
2H++2e-=H2↑
2H++Fe=Fe2++H2 ↑
2Fe+2H2O+O2=2Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
金属的腐蚀以电化学腐蚀为主,电化学腐蚀又以吸氧腐蚀为主。
钢铁的析氢腐蚀和吸氧腐蚀比较
2Fe(OH)3=Fe2O3·xH2O+(3-x) H2O
2Fe- 4e-+4OH- =2Fe(OH)2
1、下列关于金属腐蚀的说法正确的是 ( ) A.合金都比纯金属易被腐蚀 B.金属化学腐蚀的实质是:M-ne-=Mn+,电子直接转移给氧化剂 C.金属的电化学腐蚀必须在酸性条件下进行 D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀 E.镀锌铁皮的镀层损坏后,铁更容易被腐蚀
探究一:镀锌铁皮和镀锡铁皮哪个更易被腐蚀?为什么?探究二:纯锌和粗锌哪个更易和酸反应?如果向溶液中再加入硫酸铜又会什么现象?
2.某学生为研究金属腐蚀的条件,用金属丝把三根大小相同的铁钉分别固定在如图所示的三个装置中,放置一星期后观察现象,下列描述错误的是 ( ) A.装置Ⅰ的U形管铁钉一侧的液面一定会上升 B.装置Ⅱ中的铁钉腐蚀最严重 C.比较U形管铁钉一侧的液面:装置Ⅰ比装置Ⅱ的低 D.装置Ⅲ中的铁钉几乎没有被腐蚀
相关课件
这是一份高中化学人教版 (2019)选择性必修1实验活动2 强酸与强域的中和滴定教课课件ppt,共27页。PPT课件主要包含了酸碱中和滴定,溶液的pH,酸碱中和滴定曲线,VNaOH,甲基橙,无→粉红,橙→黄,粉红→无,黄→橙,突变范围等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修1实验活动1 探究影响化学平衡移动的因素图片ppt课件,共21页。PPT课件主要包含了硫酸铜晶体的变化,溶解成离子,结合成沉淀,保持不变,溶解平衡的建立,沉淀溶解平衡,电离平衡,BaSO4s,不等于零,发生移动等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修1第三节 金属的腐蚀与防护精品课件ppt,共18页。PPT课件主要包含了不锈钢,金属的防护,电化学保护法,船身上装锌块,实验4-4,锌片逐渐溶解,铁电极上有气泡冒出,H++2eH2↑,实验现象,其他方法等内容,欢迎下载使用。










