


化学选择性必修1第一单元 弱电解质的电离平衡课前预习ppt课件
展开1.理解电离平衡的概念和特征。2.掌握影响电离平衡的因素。3.能用化学平衡移动原理分析电离平衡的移动。
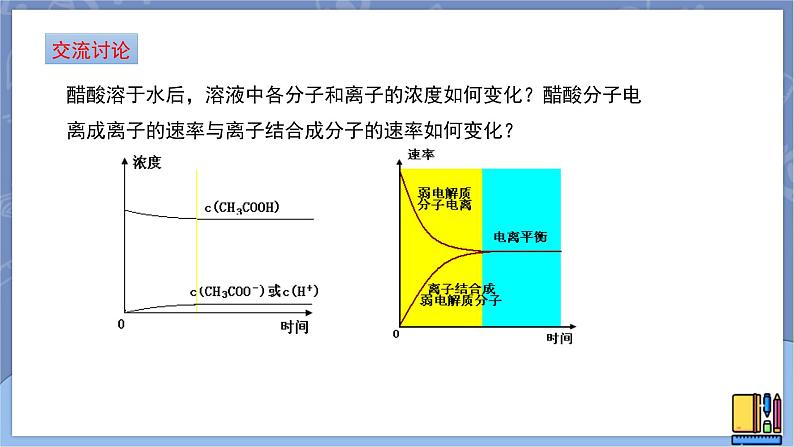
醋酸溶于水后,溶液中各分子和离子的浓度如何变化?醋酸分子电离成离子的速率与离子结合成分子的速率如何变化?
醋酸在水溶液中的电离方程式
一定温度下,弱电解质在水溶液中电离达到最大程度时,弱电解质分子电离成离子的速率和离子结合成电解质分子的速率相等,溶液中各分子和离子的浓度不再发生变化,弱电解质的电离达到了电离平衡状态。
电离平衡的特征(1)弱电解质的电离平衡是一种动态平衡,弱电解质的电离是可逆的。(2)弱电解质分子电离成离子速率和离子结合成弱电解质分子速率相等。(3)溶液中各分子和离子的浓度都保持不变。(4)外界条件发生变化,电离平衡发生移动。
电离平衡与化学平衡相同,因此也遵循化学平衡的规律。
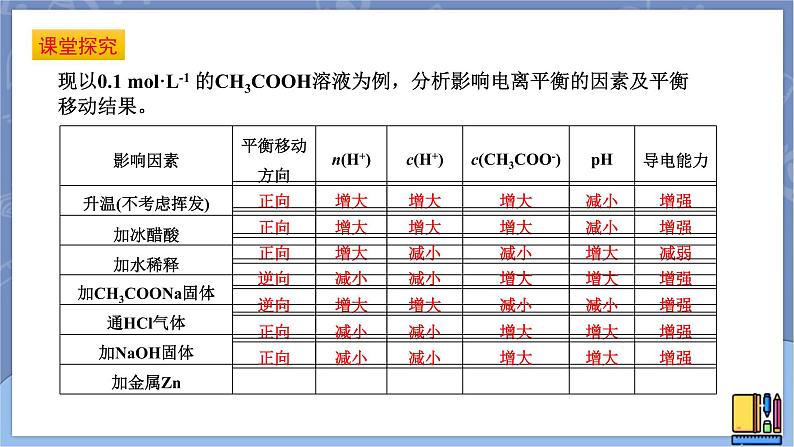
现以0.1 ml·L-1 的CH3COOH溶液为例,分析影响电离平衡的因素及平衡移动结果。
影响电离平衡的外界因素(以醋酸在水溶液中的电离为例)
(1)溶液的浓度 浓度越大,电离程度越小;浓度越小,电离程度越大。(2)溶液的酸碱度 c(H+)增大,电离平衡逆向移动;c(OH-)增大,电离平衡正向移动。(3)同离子效应 加入相同的离子,抑制电离平衡进行。(4)化学反应 加入与溶液中离子发生化学反应的物质,电离平衡正向进行。(5)温度 弱电解质的电离是吸热过程,升高温度,电离程度增大
NH3·H2O的电离方程式为NH3·H2O NH4++OH-。一定温度下,在一定浓度的氨水中改变条件,氨的电离平衡及平衡时物质的浓度有何变化?请填写下表。
减小 增大 减小 增大 正向增大 减小 减小 减小 逆向增大 增大 增大 减小 逆向减小 减小 减小 增大 正向
1.下列有关弱电解质的电离平衡的叙述正确的是( ) A.达到电离平衡时,弱电解质分子浓度和离子浓度相等B.达到电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是动态平衡C.电离平衡是相对的、暂时的,外界条件改变时,平衡就可能发生移动D.达到电离平衡后,溶液中不存在分子,只存在离子
2.下列说法正确的是( )A.根据溶液中有CH3COOH、CH3COO-和H+即可证明CH3COOH达到电离平衡状态B.根据溶液中CH3COO-和H+的物质的量浓度相等即可证明CH3COOH达到电离平衡状态C.当NH3·H2O达到电离平衡时,溶液中NH3·H2O、NH和OH-的浓度相等D.H2CO3是分步电离的,电离程度依次减弱
高中化学苏教版 (2019)必修 第一册专题3 从海水中获得的化学物质第一单元 氯气及氯的化合物精品课件ppt: 这是一份高中化学苏教版 (2019)必修 第一册专题3 从海水中获得的化学物质第一单元 氯气及氯的化合物精品课件ppt,共16页。PPT课件主要包含了氯气泄漏事件,颜色黄绿色,密度比空气大,味道刺激性气味,物理性质,毒性有毒,状态气体,易得e-,强氧化性,Cl2等内容,欢迎下载使用。
高中化学苏教版 (2019)选择性必修1第二单元 溶液的酸碱性图文课件ppt: 这是一份高中化学苏教版 (2019)选择性必修1第二单元 溶液的酸碱性图文课件ppt,共14页。PPT课件主要包含了学习目标,实验探究,课堂探究,交流讨论,无影响,课堂练习,在半分钟内不变色等内容,欢迎下载使用。
化学第二单元 溶液的酸碱性教学演示课件ppt: 这是一份化学第二单元 溶液的酸碱性教学演示课件ppt,共12页。PPT课件主要包含了学习目标,交流讨论,归纳小结,课堂探究,课堂练习等内容,欢迎下载使用。













