










人教版九年级下册第九单元 溶液课题3 溶液的浓度多媒体教学ppt课件
展开第2课时 溶质质量分数的综合计算
【学习目标】
1.知识与技能:掌握溶质质量分数的计算。
2.过程与方法:学会分析问题、解决问题,提高解题能力,能找准各量的关系。
3.情感态度与价值观:培养具体问题具体分析的能力。
【学习重点】
有关溶质质量分数的计算。
【学习难点】
与化学反应有关且含杂质的溶质质量分数的计算。
一、情景导入 生成问题
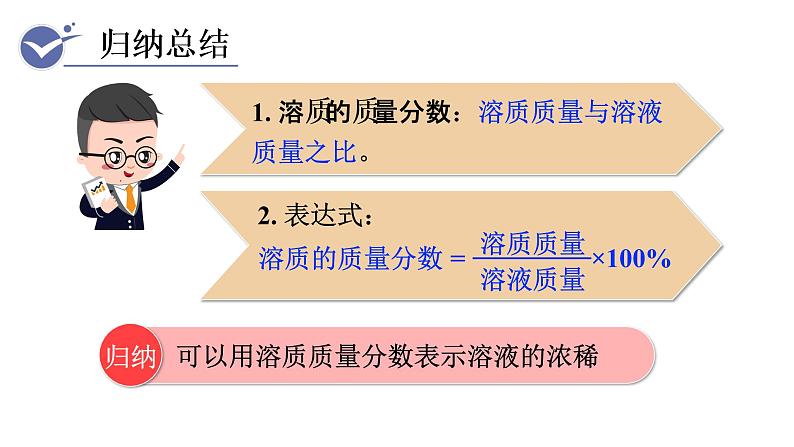
1.写出溶质质量分数的公式及其变形,你能用公式或公式变形来解决实际问题吗?
2.出示学习目标,由学生对学习目标进行解读。
二、自学互研 生成能力
1.阅读教科书P43例题1:题目略。
思考:(1)本题已知量是什么?待求量是什么?
(2)计算的依据是什么?
(3)计算的步骤是怎样的?
【交流】写出解题步骤和过程。
略。
2.配制500 mL质量分数为10%的氢氧化钠溶液(密度为1.1 g/cm3),需要氢氧化钠和水各多少克?
【讨论】与例题1相比,两题的不同之处是什么?该如何来解决这个问题呢?
解:500 mL氢氧化钠溶液质量为:500 mL×1.1 g/cm3=550 g,
(1)需要氢氧化钠质量:550×10%=55 g;
(2)需要水的质量:550 g-55 g=495 g。
教科书P44例题2改编:把50 g质量分数为98%的浓硫酸稀释成质量分数为20%的硫酸溶液,需要多少克水?
解:浓硫酸中溶质的质量为50 g×98%=49 g,
质量分数为20%的稀硫酸溶液的质量为=245 g,
需要水的质量为245 g-50 g=195 g。
答:需要水195 g。
【讨论】解这道题的关键是什么?
【分析】抓住关键:溶液稀释前的溶质质量=稀释后的溶质质量。
【拓展】如果把50 g换成50 mL那么还需要什么条件才能解题?
【巩固练习】P45课后习题3、4两小题。
方法指导:创景设疑,帮助学生明确本节课的学习目标。
提示:教会学生看书,独学时对于书中的问题一定要认真探究,书写答案。 教会学生落实重点。
提示:收集疑难问题,在交流展示中解决。 |
【例题】100 g某硫酸溶液恰好与13 g锌完全反应。试计算反应后溶液中溶质的质量分数。(结果精确到0.1%)
解:设反应后生成的ZnSO4的质量为x,H2的质量为y。
Zn+H2SO4===ZnSO4+H2↑
65 161 2
13 g x y
= x=32.2 g
= y=0.4 g
反应后溶液中溶质的质量分数为:×100%≈28.6%。
答:反应后溶液中溶质的质量分数约为28.6%。
【分析】这种与化学方程式结合起来的题目,应该怎样来寻找溶质、溶剂以及溶液的量呢?
【小结】对学生的板演进行评价,引导学生归纳计算步骤。
【巩固练习】P45课后习题第6小题。
三、交流展示 生成新知
知识模块一:溶质质量分数的计算
知识模块二:溶液稀释和配制问题的计算
知识模块三:与化学反应有关的溶质质量分数的计算
第2课时 溶质质量分数的综合计算
一、在饱和溶液中:溶质质量分数C%=×100%(C < S)
二、溶液稀释和配制问题的计算
关键:稀释前溶质的质量=稀释后溶质的质量。
三、化学反应中溶质质量分数的计算
教学中,教师要引导学生认真审题,不要盲目地随意计算。这个课题的内容一向是学生理解上的难点,尤其是计算牵涉的变形题目种类较多,学生很容易出现思维混乱,计算中出现张冠李戴的现象。对于溶质质量分数概念的应用和结合化学方程式进行一些有关溶质质量分数的计算,要通过一些典型例题的进一步强化训练,发现学生还存在哪种问题,需要在后续的教学中继续巩固。
提示:针对在自学互研中收集的疑难问题,在交流展示中指导。
及时总结所学知识,养成梳理知识的良好习惯,受益终身。 |
化学九年级下册课题3 溶液的浓度评优课ppt课件: 这是一份化学九年级下册<a href="/hx/tb_c76882_t3/?tag_id=26" target="_blank">课题3 溶液的浓度评优课ppt课件</a>,共28页。PPT课件主要包含了溶液的浓度,20ml水,44%,09%,完全溶解,≈265%等内容,欢迎下载使用。
初中化学人教版九年级下册第九单元 溶液课题3 溶液的浓度备课课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c76882_t3/?tag_id=26" target="_blank">第九单元 溶液课题3 溶液的浓度备课课件ppt</a>,共41页。PPT课件主要包含了%VV,白酒的浓度,白醋的浓度,啤酒的浓度,课前导入,%mV,葡萄糖注射液的浓度,9%mV,PART1,溶质的质量分数等内容,欢迎下载使用。
人教版课题3 溶液的浓度教学演示课件ppt: 这是一份人教版课题3 溶液的浓度教学演示课件ppt,共14页。PPT课件主要包含了实验9-7,飞机喷洒农药,喷洒药水,溶质质量分数,溶质质量,溶液质量,×100%,变一变,实验9-8,计算的依据等内容,欢迎下载使用。













