




- 3.2.1 分子晶体(基础过关A练)-2022-2023学年高二化学课时过关提优AB练(人教版2019选择性必修2) 试卷 2 次下载
- 3.2.2 共价晶体(基础过关A练)-2022-2023学年高二化学课时过关提优AB练(人教版2019选择性必修2) 试卷 3 次下载
- 3.3.1 金属键 金属晶体(基础过关A练)-2022-2023学年高二化学课时过关提优AB练(人教版2019选择性必修2) 试卷 3 次下载
- 3.3.2 离子晶体 过渡晶体与混合型晶体(基础过关A练)-2022-2023学年高二化学课时过关提优AB练(人教版2019选择性必修2) 试卷 1 次下载
- 3.4 配合物与超分子(基础过关A练)-2022-2023学年高二化学课时过关提优AB练(人教版2019选择性必修2) 试卷 2 次下载
高中化学人教版 (2019)选择性必修2第三节 金属晶体与离子晶体精品课后练习题
展开第三章 晶体结构与性质
第三节 金属晶体与离子晶体
(建议时间:30分钟)
1.下列叙述正确的是
A.金属受外力作用时常常发生变形而不易折断,这是由于金属原子之间有较强的作用
B.通常情况下,金属里的自由电子会发生定向移动而形成电流
C.金属是借助自由电子的运动,把能量从温度高的部分传到温度低的部分
D.金属的导电性随温度的升高而减弱
2.下列四种性质的叙述,可能属于金属晶体的是( )
A.由分子间作用力结合而成,熔点低
B.固态时或熔融后易导电,熔点在1 000 ℃左右
C.以共价键结合成三维骨架结构,熔点高
D.固态时不导电,但溶于水或熔融后能导电
3.在金属晶体中,金属原子的价电子数越多,原子半径越小,金属键越强,金属的熔、沸点越高。由此判断下列各组金属熔、沸点高低顺序,其中正确的是
A.Mg>Al>Ca B.Al>Na>Li
C.Al>Mg>Ca D.Mg>Ba>Al
4.要使金属晶体熔化必须破坏其中的金属键。金属晶体熔点的高低和硬度的大小一般取决于金属键的强弱,而金属键的强弱与金属阳离子所带电荷的多少及半径大小有关。由此判断下列说法正确的是
A.金属镁的熔点大于金属铝
B.碱金属的熔点从到是逐渐增大的
C.金属铝的硬度大于金属钠
D.金属钙的硬度小于金属钡
5.下图为某金属的面心立方晶胞,则该金属的一个晶胞中实际拥有的微粒数为( )
A.3 B.4 C.7 D.9
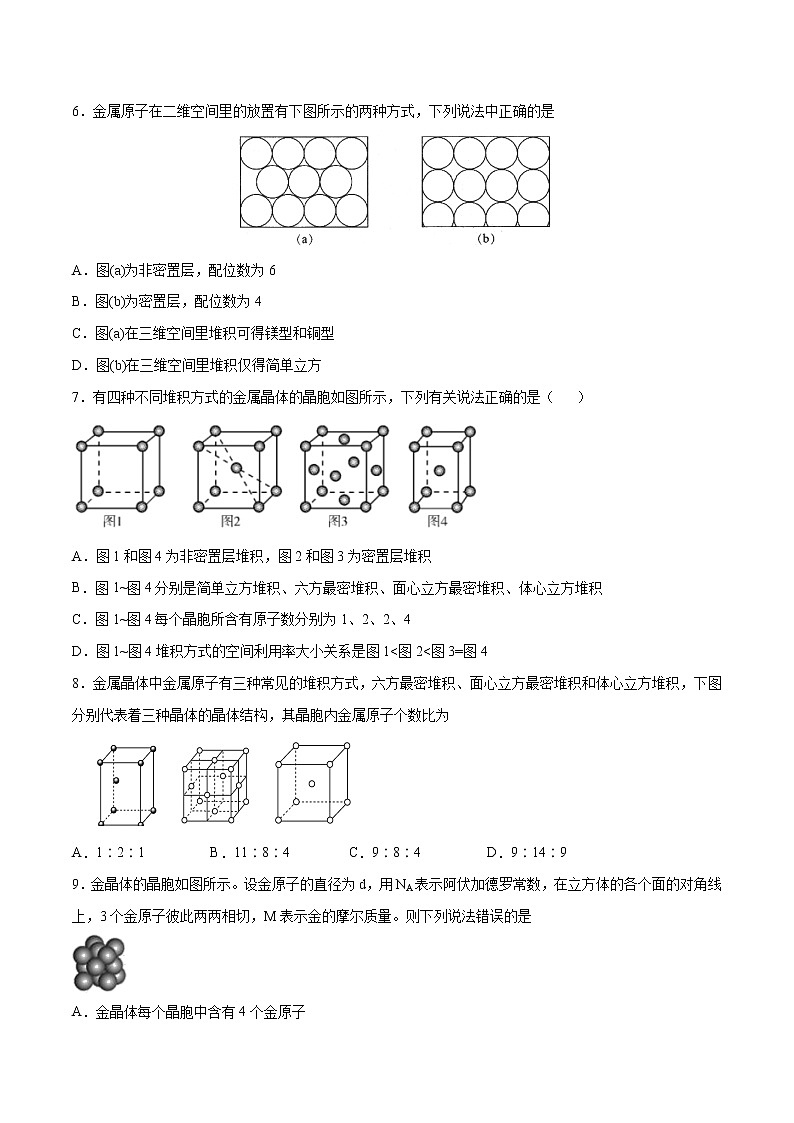
6.金属原子在二维空间里的放置有下图所示的两种方式,下列说法中正确的是
A.图(a)为非密置层,配位数为6
B.图(b)为密置层,配位数为4
C.图(a)在三维空间里堆积可得镁型和铜型
D.图(b)在三维空间里堆积仅得简单立方
7.有四种不同堆积方式的金属晶体的晶胞如图所示,下列有关说法正确的是( )
A.图1和图4为非密置层堆积,图2和图3为密置层堆积
B.图1~图4分别是简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积
C.图1~图4每个晶胞所含有原子数分别为1、2、2、4
D.图1~图4堆积方式的空间利用率大小关系是图1<图2<图3=图4
8.金属晶体中金属原子有三种常见的堆积方式,六方最密堆积、面心立方最密堆积和体心立方堆积,下图分别代表着三种晶体的晶体结构,其晶胞内金属原子个数比为
A.1∶2∶1 B.11∶8∶4 C.9∶8∶4 D.9∶14∶9
9.金晶体的晶胞如图所示。设金原子的直径为d,用NA表示阿伏加德罗常数,在立方体的各个面的对角线上,3个金原子彼此两两相切,M表示金的摩尔质量。则下列说法错误的是
A.金晶体每个晶胞中含有4个金原子
B.金属键无方向性,金属于最密堆积,配位数是12
C.一个晶胞的体积是16d3
D.金晶体的密度是
10.铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法错误的是
A.铁镁合金的化学式可表示为
B.晶胞中有14个铁原子
C.晶体中存在的化学键类型为金属键
D.该晶胞的质量是(表示阿伏加德罗常数的值)
11.金晶体是面心立方最密堆积,已知立方体的每个面上5个金原子紧密堆砌,金原子半径为r cm,则金晶体的空间利用率为
A. B.
C. D.
12.石墨晶体是层状结构(如图)。以下有关石墨晶体的说法正确的一组是( )
①石墨中存在两种作用力;②石墨是混合晶体;③石墨中的C为sp2杂化;④石墨熔点、沸点都比金刚石低;⑤石墨中碳原子数和C—C键数之比为1∶2;⑥石墨和金刚石的硬度相同;⑦石墨层内导电性和层间导电性不同;⑧每个六元环完全占有的碳原子数是2
A.全对 B.除⑤外
C.除①④⑤⑥外 D.除⑥⑦⑧外
13.Al 的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示。
已知 Al的原子半径为 d,NA代表阿伏加德罗常数,Al 的相对原子质量为 M。
(1)晶胞中 Al 原子的配位数为_____,一个晶胞中 Al 原子的数目为_____,该晶胞的空间利用率是_____。
(2)该晶体的密度为_____(用字母表示)。
14.碳元素的单质有多种形式,如图所示,依次是C60、石墨和金刚石的结构图:
回答下列问题:
(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C60属于________晶体,石墨属于________晶体。
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存在________共价键,还有________键。
15.(1)如图为一个金属铜的晶胞,请完成以下各题。
①该晶胞“实际”拥有的铜原子数是_________个。
②该晶胞称为________(填序号)。
A 六方晶胞 B 体心立方晶胞 C 面心立方晶胞 D 简单立方晶胞
③此晶胞立方体的边长为,的摩尔质量为,金属铜的密度为,则阿伏加德罗常数为________(用a、表示)。
(2)洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,如图为氮原子在铁的品面上的单层附着局部示意图(图中小黑色球代表氮原子,大灰色球代表铁原子)。则在图示状况下,铁颗粒表面上的原子数的比值为____________。
(3)硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如图示意的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面各有一个镁原子,6个硼原子位于棱柱内,则该化合物的化学式可表示为_______。
(4)若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的微粒间的相互作用依次是_______。
A 氢键:分子间作用力:非极性键 B 氢键;分子间作用力:极性键
C 氢键;极性键;分子间作用力 D 分子间作用力;氢键:非极性键
16.早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)①铜元素位于周期表中________区。Cu2+的价电子排布图为___________
___________。
②锰、铁、钴三种元素的逐级电离能如下表:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
Mn | 717.3 | 1 509.0 | 3 248 | 4 940 |
Fe | 762.5 | 1 561.9 | 2 957 | 5 290 |
Co | 760.4 | 1 648 | 3 232 | 4 950 |
铁元素的第三电离能明显低于锰元素和钴元素,其原因是 __。
③实验室可用赤血盐K3[Fe(CN)6]检验Fe2+,在赤血盐中铁元素的化合价为________,中心离子的配位数为________。
(2)利用反应:X+C2H2+NH3→Cu2C2+NH4Cl(未配平)可检验乙炔。
①化合物X晶胞结构如图,据此可知X的化学式为________。
②乙炔分子中σ键与π键数目之比为_______,碳原子的杂化方式为_______;N空间构型为 (用文字描述)。
(3)Al单质中原子采取面心立方最密堆积,其晶胞边长为0.405 nm,列式表示Al单质的密度 g·cm-3(不必计算出结果)。
高中化学人教版 (2019)选择性必修3第一节 糖类精品课后复习题: 这是一份高中化学人教版 (2019)选择性必修3第一节 糖类精品课后复习题,文件包含41糖类素养提优B练-2022-2023学年高二化学课时过关提优AB练人教版2019选择性必修3解析版docx、41糖类素养提优B练-2022-2023学年高二化学课时过关提优AB练人教版2019选择性必修3原卷版docx等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
高中人教版 (2019)实验活动3 糖类的性质精品一课一练: 这是一份高中人教版 (2019)实验活动3 糖类的性质精品一课一练,文件包含33醛酮素养提优B练-2022-2023学年高二化学课时过关提优AB练人教版2019选择性必修3解析版docx、33醛酮素养提优B练-2022-2023学年高二化学课时过关提优AB练人教版2019选择性必修3原卷版docx等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。
人教版 (2019)选择性必修3第一节 卤代烃精品同步测试题: 这是一份人教版 (2019)选择性必修3第一节 卤代烃精品同步测试题,文件包含31卤代烃素养提优B练-2022-2023学年高二化学课时过关提优AB练人教版2019选择性必修3解析版docx、31卤代烃素养提优B练-2022-2023学年高二化学课时过关提优AB练人教版2019选择性必修3原卷版docx等2份试卷配套教学资源,其中试卷共22页, 欢迎下载使用。













