




化学九年级上册第一节 质量守恒定律背景图ppt课件
展开课题1 质量守恒定律
物质在发生化学变化时,反应物的质量总和与生成物的质量总和之间存在什么关系呢?
我们的猜想:可能。。。
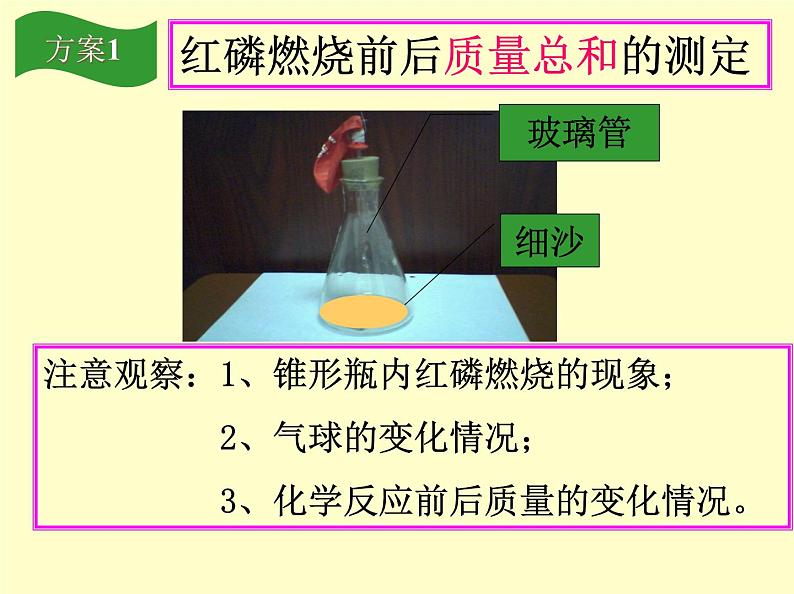
注意观察:1、锥形瓶内红磷燃烧的现象; 2、气球的变化情况; 3、化学反应前后质量的变化情况。
红磷燃烧前后质量总和的测定
剧烈燃烧,产生大量白烟,放出大量热 气球先鼓起后瘪掉,
结论:反应物质量总和 生成物质量总和
m(P)+ m(O2)= m(P2O5)
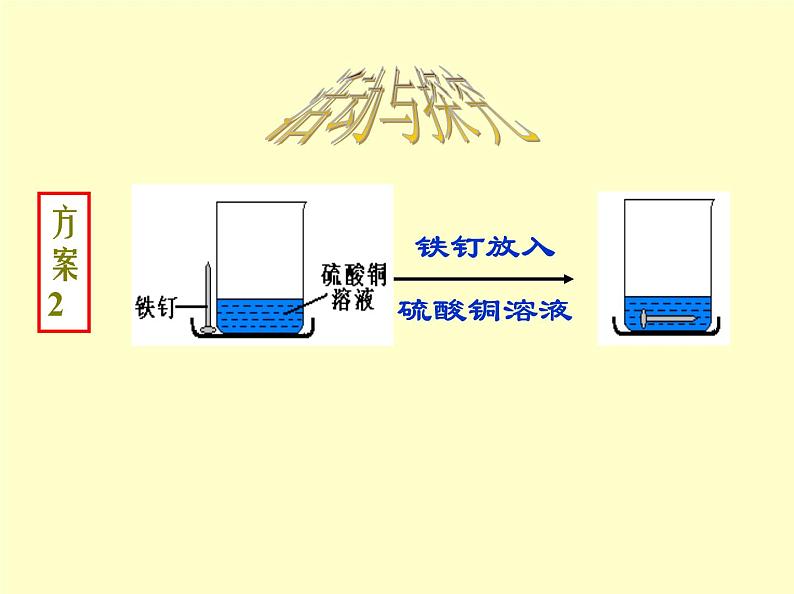
铁钉跟硫酸铜溶液反应前后质量总和的测定
结论:反应物质量总和=生成物质量总和
铁钉表面有红色固体物质析出,溶液由蓝色变成浅绿色。
m(Fe)+ m(CuSO4) = m(FeSO4) + m(Cu)
参加化学反应的各物质的 质量总和
生成的各物质的质量 总和
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和——质量守恒定律
为什么化学反应前后的物质的质量总和相等?
试用分子、原子的观点解释质量守恒的原因。
水 氢气 + 氧气
分析讨论:①化学反应前后,分子种类变了吗?②化学反应前后,原子种类变了吗?③化学反应过程的实质是什么?
H2O H2 + O2
化学反应的实质 :物质是由原子和分子,离子构成的,分子的破裂和原子的重新组合。即在化学变化中分子会破裂,但可重组合成新的分子。
是否存在违背质量守恒定律的化学反应呢?
固体粉末溶解,有大量的气泡产生;
天平指针向右倾斜(变轻)
思考:1、该实验的现象是什么?
发出耀眼的白光、放出大量的热,生成白色固体,同时还有白烟产生
思考:2、该反应的原理是什么?
1、根据上面两个实验,讨论为什么会出现这样的实验结果。2、如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?
之所以会出现这样的结果,是由于反应有气体参加或生成的缘故。
如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会发现天平保持指针向左偏。
小结:若选择有气体参加或有气体生成的化学反应来证明质量守恒定律,则反应一定要在密闭容器内进行。
把握质量守恒定律应注意几点
1、只有化学变化才遵守质量守恒定律,物理变化不用质量守恒定律解释!2、守恒的是“总质量”,即“参加反应的各反应物的总质量”和“生成物的总质量”。 如沉淀、气体等都应考虑进去。3、 “参加”,意味着没有参加反应(剩余)的物质的质量不能算在内。
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
巩固练习:1、现有一反应A+B→C,有10克A和5克B反应,反应结束后还剩余3克A,B无剩余,则生成C的质量为多少克?
参加参加注意是参加反应的质量
巩固练习:2、根据质量守恒定律,2L 氢气和1L氧气反应能生成3L水,这句话对吗?
巩固练习: 3、10克的水受热蒸发变成10克的水蒸气,这一变化符合质量守恒定律。这句话对吗?
在化学反应中有六不变、两改变、一个可能改变
化学反应前后分子的数目
1、下列现象不能用质量守恒定律解释的是 A、蜡烛燃烧时慢慢变短 B、白磷在密闭容器中燃烧质量不变 C、铁钉生锈后质量增加 D、水结冰质量不变
2、请用质量守恒定律解释能否点石成金?
根据质量守恒定律,化学反应前后元素种类不变,石头中没有金元素,所以不能点石成金。
用质量守恒定律解释常见现象
3、对质量守恒定律的正确理解是( ) A、参加反应的各种物质的质量不变B、化学反应前后各物质的质量不变C、化学反应前的各物质质量总和等于反应后生成的各物质的质量总和D、参加化学反应的各物质的质量总和与反应后生成的各物质的质量总和相等
4、下列说法能用质量守恒定律解释的是( ) A m克水受热变成m克水蒸气 B 煤燃烧后留下煤灰比原煤的质量少 C 10克食盐溶于70克水得到80克食盐水 D 湿衣服晾干后,质量变小
蜡烛在空气中燃烧后,生成二氧化碳和水,试推断蜡烛中一定含有_____元素,可能含有___元素。
三、质量守恒的应用1、推断物质的组成元素
环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式为:I2O5 + 5CO =I2 + 5X,根据生成X的多少,可以判断CO的含量,则X的化学式为 。
木炭在氧气中燃烧生成二氧化碳的反应可以用文字表示为:
用化学式来表示化学反应的式子,叫做化学方程式。
(1)宏观读法:碳和氧气在点燃的条件下生成二氧化碳(2)数量读法:每12份质量的碳跟32份质量的氧气反应生成44份质量的二氧化碳(3)微观读法:每1个碳原子和1个氧分子反应生成1个二氧化碳分子
36 4 32
①表示水在通电的条件下反应生成氢气和氧气。
③表示每2个水分子在通电的条件下能反应生成2个氢分子和1个氧分子。
②表示每36份质量的水分解能生成4份质量的氢气和32份质量的氧气。
1、用化学式表示化学反应的式子,叫做化学方程式。2、化学方程式表明了: ①反应物、生成物和反应条件; ②参加反应的各微粒之间的数量关系; ③表示各物质之间的质量关系,即各物质之间的质量比,通过相对分子质量(或相对原子质量)来表示。
从物质种类、质量和反应条件等方面考虑,下列反应的化学方程式能提供给你哪些信息?S+O2 SO2Fe+CuSO4 Cu + FeSO4CuO+H2 Cu+H2O
北京课改版九年级上册第2章 空气之谜第一节 空气多媒体教学课件ppt: 这是一份北京课改版九年级上册第2章 空气之谜第一节 空气多媒体教学课件ppt,共18页。PPT课件主要包含了汞Hg,第一个发现氮气的,氧化汞,--拉瓦锡,药品红磷,原理红磷+氧气,可以用蜡烛代替吗,物质的简单分类,供给呼吸,支持燃烧等内容,欢迎下载使用。
2021学年第3章 构成物质的微粒第三节 分子课文ppt课件: 这是一份2021学年第3章 构成物质的微粒第三节 分子课文ppt课件,共24页。PPT课件主要包含了扫描隧道显微镜,猜猜看,水分子自述,观察与思考,想一想,分子的基本特征,分子间隔比较示意图,我会解释,分子由原子构成,水的蒸发等内容,欢迎下载使用。
2020-2021学年第一节 原子课文课件ppt: 这是一份2020-2021学年第一节 原子课文课件ppt,共18页。PPT课件主要包含了本节课我们要知道,原子结构的发现史,原子的内部运动等内容,欢迎下载使用。













