






高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教学课件ppt
展开
这是一份高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教学课件ppt,共16页。PPT课件主要包含了学习评价,《金版》79问题情境,《金版》P80等内容,欢迎下载使用。
【学习任务一】PH计算
(3)25 ℃时,在0.01 ml/L的盐酸中,溶液中c(H+) 和pH是多少?由水电离产生的H+浓度是多少?
1、单一溶液的PH计算
解题技巧:酸过量,求过量的c(H+)溶液→PH
2、混合溶液的PH计算
解题技巧:碱过量,求过量的c(OH-)溶液→根据Kw求算c(H+)溶液→PH
解题技巧:两强酸混合,求c(H+)混合溶液→PH
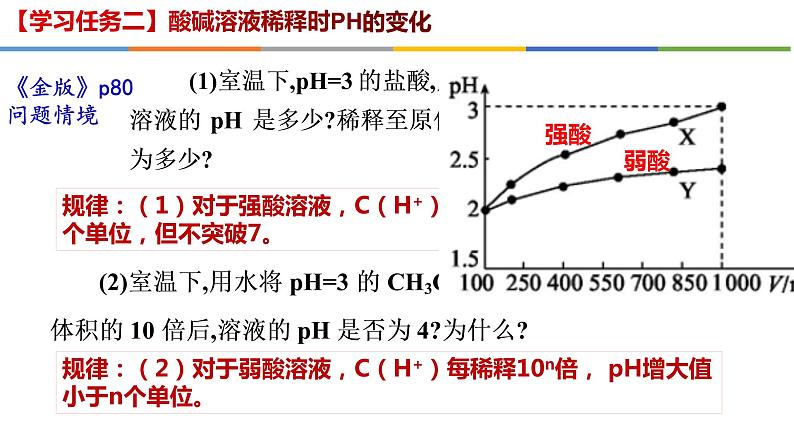
【学习任务二】酸碱溶液稀释时PH的变化
规律:(1)对于强酸溶液,C(H+)每稀释10n倍, pH增大n个单位,但不突破7。
规律:(2)对于弱酸溶液,C(H+)每稀释10n倍, pH增大值小于n个单位。
《金版》p80问题情境
规律:(3)对于强碱溶液,C(OH-)每稀释10n倍, pH减小n个单位,但不突破7。( 4)对于弱碱碱溶液,C(OH-)每稀释10n倍, pH减小值小于n个单位。
补充:如果将上述溶液改为等PH的氨水,稀释10倍后,PH如何变化?
常温下,酸碱溶液无限稀释,pH只能接近于7,酸溶液的pH不可能大于7,碱溶液的pH不可能小于7。
1.pH相等的酸或碱溶液稀释后溶液pH的变化示意图
酸碱溶液稀释时pH的变化图像
2.c相等的酸或碱溶液稀释后溶液pH的变化示意图
无论是c相等还是pH相等,加水稀释相同倍数pH变化大的都是强酸或强碱。
【阅读拓展1】人体某些体液的正常pH范围
【学习任务三】pH测定和调控的意义
【阅读拓展2】 土壤的酸碱性直接影响植物的生长发育。例如浙江的“龙井茶”就只能产于微酸性的土壤中。如果酸性太强就无法正常生长。
相关课件
这是一份2021学年第三章 水溶液中的离子反应与平衡第二节 水的电离和溶液的pH优秀课件ppt,共27页。PPT课件主要包含了思考交流,学习目标,第3课时pH的计算,约为7,当堂练习等内容,欢迎下载使用。
这是一份高中人教版 (2019)第三章 水溶液中的离子反应与平衡第三节 盐类的水解教学ppt课件,共27页。PPT课件主要包含了③②①等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教学ppt课件,共16页。PPT课件主要包含了溶液中存在哪些微粒,问题情境,水的电离,v电离,等动定变,温度越高Kw越大,①中性溶液时,②酸性溶液时,③碱性溶液时,《金版》P76等内容,欢迎下载使用。









