2022中考化学总复习专题突破:实验探究题(酸的性质)(无答案)
展开
这是一份2022中考化学总复习专题突破:实验探究题(酸的性质)(无答案),共9页。试卷主要包含了 硝酸是实验室常见的一种酸等内容,欢迎下载使用。
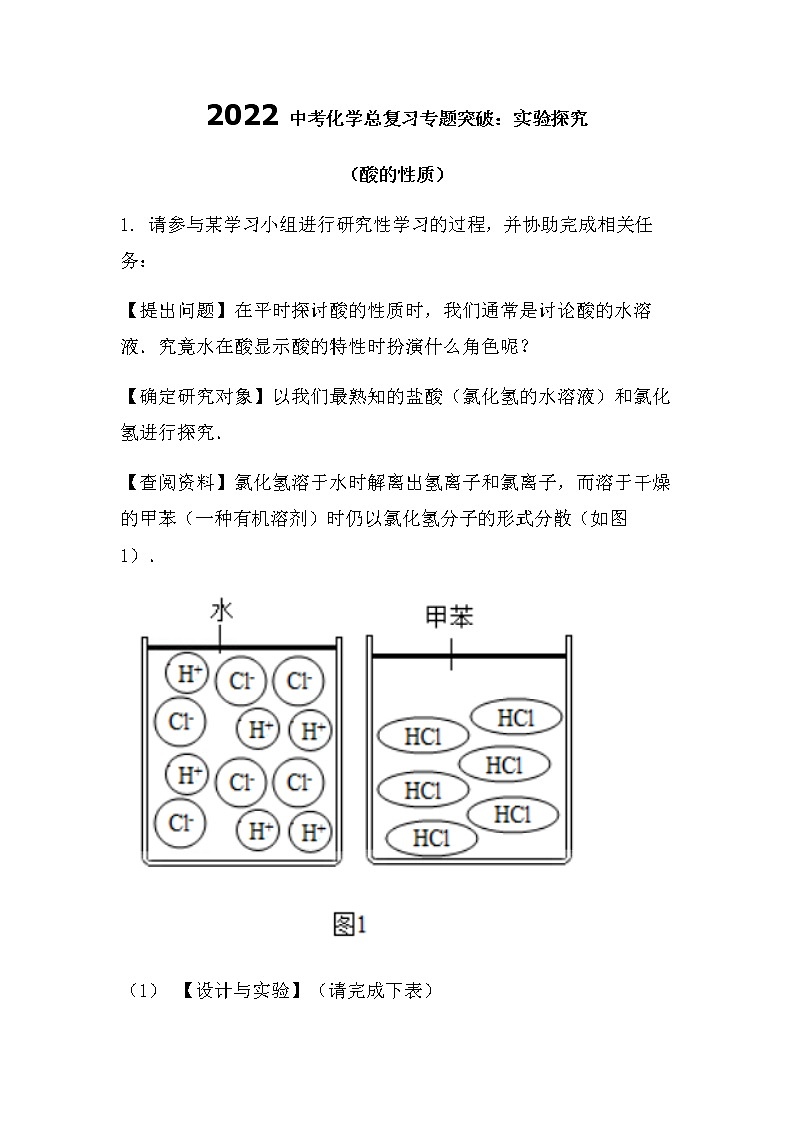
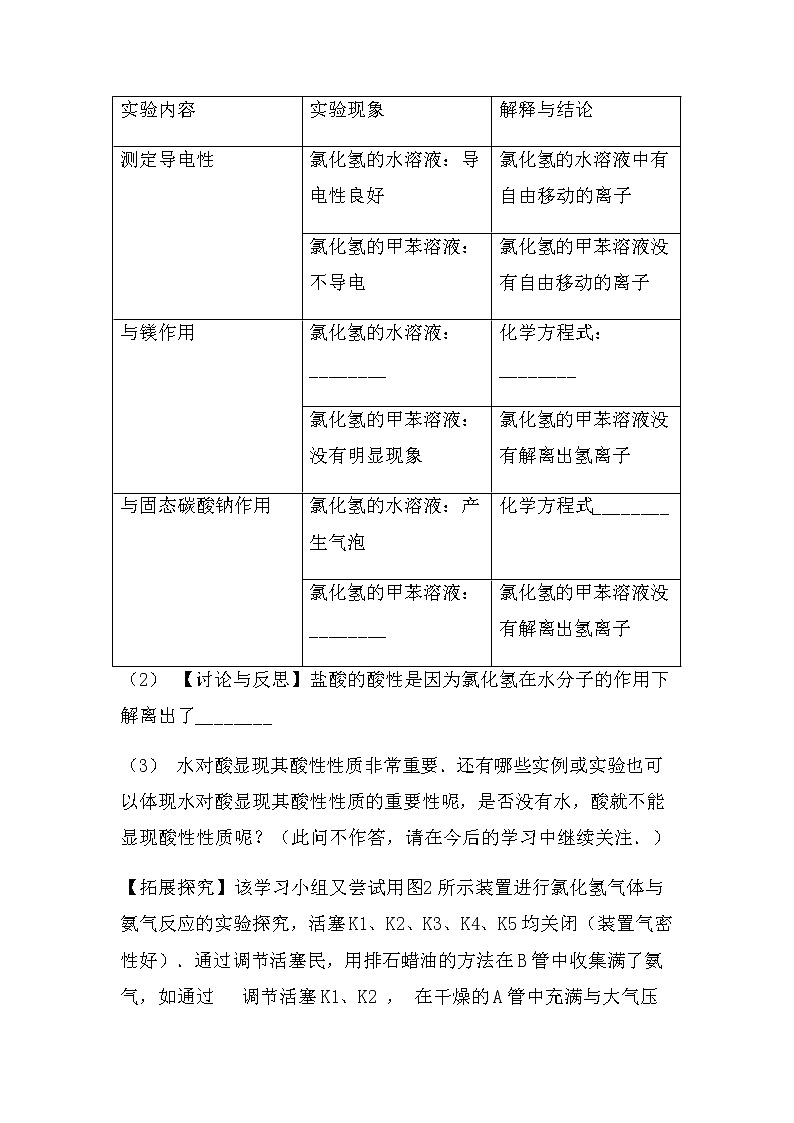
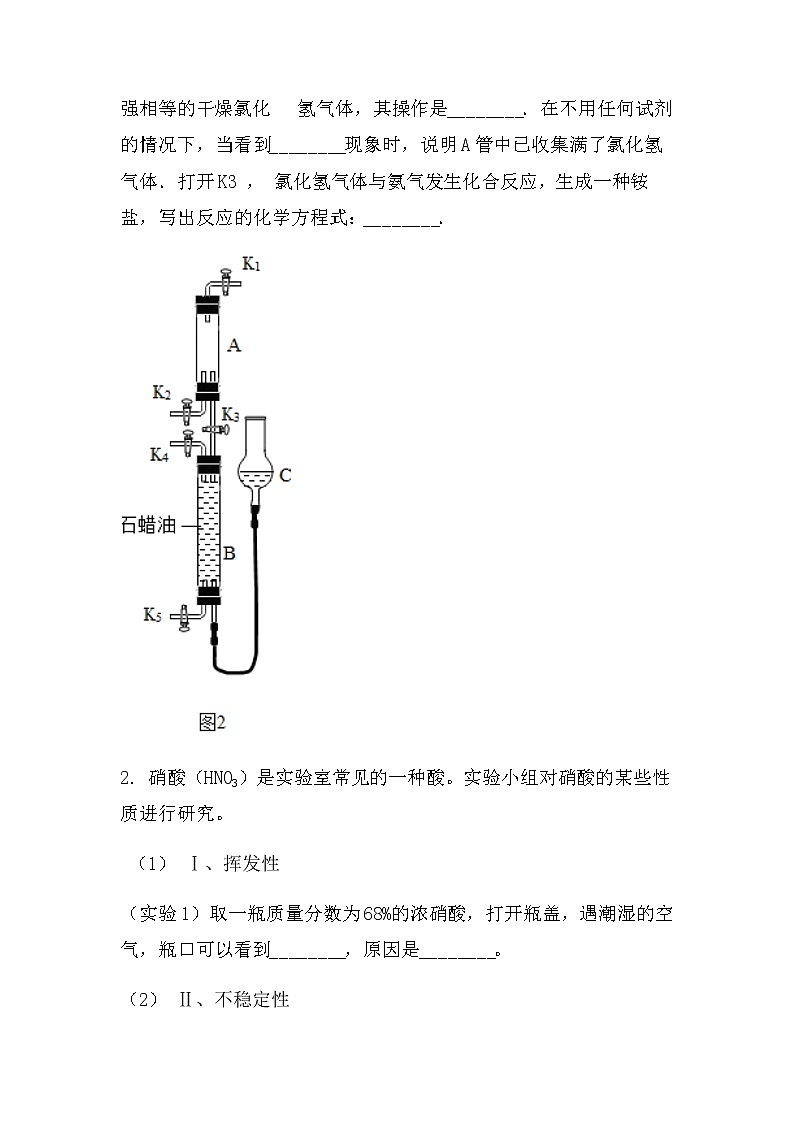
2022中考化学总复习专题突破:实验探究(酸的性质)1. 请参与某学习小组进行研究性学习的过程,并协助完成相关任务: 【提出问题】在平时探讨酸的性质时,我们通常是讨论酸的水溶液.究竟水在酸显示酸的特性时扮演什么角色呢? 【确定研究对象】以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究. 【查阅资料】氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如图1). (1) 【设计与实验】(请完成下表) 实验内容实验现象解释与结论测定导电性 氯化氢的水溶液:导电性良好氯化氢的水溶液中有自由移动的离子氯化氢的甲苯溶液:不导电 氯化氢的甲苯溶液没有自由移动的离子与镁作用氯化氢的水溶液:________ 化学方程式:________ 氯化氢的甲苯溶液:没有明显现象氯化氢的甲苯溶液没有解离出氢离子与固态碳酸钠作用氯化氢的水溶液:产生气泡 化学方程式________氯化氢的甲苯溶液:________氯化氢的甲苯溶液没有解离出氢离子 (2) 【讨论与反思】盐酸的酸性是因为氯化氢在水分子的作用下解离出了________ (3) 水对酸显现其酸性性质非常重要.还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢,是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注.) 【拓展探究】该学习小组又尝试用图2所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好).通过调节活塞民,用排石蜡油的方法在B管中收集满了氨气,如通过 调节活塞K1、K2 , 在干燥的A管中充满与大气压强相等的干燥氯化 氢气体,其操作是________.在不用任何试剂的情况下,当看到________现象时,说明A管中已收集满了氯化氢气体.打开K3 , 氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:________.2. 硝酸(HNO3)是实验室常见的一种酸。实验小组对硝酸的某些性质进行研究。 (1) Ⅰ、挥发性 (实验1)取一瓶质量分数为68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到________,原因是________。 (2) Ⅱ、不稳定性 (查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体、氧气及一种无色液体 硝酸分解的化学方程式为:________。 (3) (实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26℃)。记录溶液上方的气体颜色随时间的变化情况。 实验编号123实验条件实验现象6分钟出现浅红棕色15分钟红棕色比较明显30分钟红棕色非常明显60分钟无明显变化 3分钟出现浅红棕色 6分钟红棕色比较明显 10分钟红棕色非常明显 实验①、②对比是研究________对浓硝酸稳定性的影响。 实验①、③对比可得出的结论是________。 (4) Ⅲ、酸性 (查阅资料2)硝酸能够与金属氧化物反应生成盐和水。 (实验3)向氧化铜粉末中加入硝酸,能够看到的现象是________。 IV、氧化性 (查阅资料3)浓硝酸在加热条件下能与木炭发生反应: C+4HNO3(浓) 加 热 4NO2↑+CO2↑+2H2O。 (实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能是________。3. 实验室开放日,化学小组的同学来到实验室,对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究。 (1) 【实验设计】 ①将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变________色。 ②将Zn片投入稀硝酸中,预计将产生氢气。 (2) 【实验验证】 同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B。 【提出问题】 ①石蕊试液变色后为何会褪色? ②上述产生的无色气体是什么?硝酸具有哪些特性? 【查阅资料】 看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料: ①硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2。 ②含氮元素的某些气态物质的物理性质: NH3 N2NONO2颜色无色 无色 无色红棕色 溶解性极易溶于水不溶于水不溶于水 可溶于水或硝酸【猜想与分析】 小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是________。 (3) 大家一致认同了红棕色气体B是NO2 , 但对于无色气体A及变化的原因有不同的看法: ①小丽同学认为A是NH3 , 但遭到了大家的一致反对,原是________。 ②小强同学认为A是N2 , 也遭到大家的一致反对,原因是________。 ③经讨论,最终大家获得了A是NO,NO在试管口遇氧气生成NO2的共识。 (4) 【实验探究】 小红同学对硝酸与Cu反应很感兴趣,便取了一小块Cu片投入稀HNO3中,发现Cu片溶解,也出现了上述Zn与稀HNO3反应的类似现象,确认生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的化学计算量数之比为3:8,由此获得了Cu与稀HNO3的反应化学方程式________。 (5) 【交流与反思】 ①根据探究结果,请你解释稀HCl跟Cu不反应而稀HNO3却能跟Cu反应的原因________。 ②实验室制取氢气________ (填“能”“不能”)用稀硝酸。4. 西西和建设两位同学为探究硫酸的化学性质,做了如下实验: 试管A中的现象是________,反应后试管B中可能含有的离子是________(写离子符号);试管C中反应的化学方程式________; 建设同学把D、E试管内反应后的溶液倒入同一个烧杯中,观察到无明显现象,建设同学认为D试管中氢氧化钠溶液和稀硫酸一定恰好完全反应,请评价建设同学的说法________。 (1) 【提出问题】E试管中反应后溶液中溶质是什么? (2)【实验猜想】猜想一:Na2SO4 猜想二:Na2SO4、H2SO4 西西同学的猜想:________(写化学式)。 (3) 【实验验证】西西同学取少量E试管反应后液体于试管中,向其中加入________观察到________,证明自己的猜想是正确的。 结合建设同学的实验,可推知D试管溶液中溶质为________。 (4) 【交流总结】在分析某溶液含有的溶质时,可根据与其混合的溶液中________及混合后的________来得出结论。5. 在学习了酸的化学性质之后,某实验小组选用稀盐酸做了如下图所示实验。 请回答下列问题: (1) A烧杯中,铜不与稀盐酸发生反应的原因是________。 (2) 能产生气泡的是________(填字母序号)。 (3) 写出C烧杯中反应的化学方程式________。 (4) D烧杯中,溶液由红色变为________色,说明盐酸与氢氧化钠发生了反应。 同学们进一步对D烧杯中反应后的溶液进行探究,对其溶质的成分(除酚酞外)做出如下猜想。猜想一:只含有一种溶质;猜想二:含有两种溶质。为了验证上述猜想,进行如下实验,请完成下列表格。 实验操作测定结果得出结论用玻璃棒蘸取D烧杯中反应后的溶液,滴在pH试纸上,与标准比色卡比较pH<7猜想________正确,溶液中的溶质是________。小组同学选用稀硫酸代替稀盐酸重复实验,证明了硫酸与盐酸具有相似的化学性质。酸有一些相似的化学性质,是因为在不同的酸溶液中都含有相同的________。
相关试卷
这是一份2022中考化学总复习专题突破:实验探究题(突破型)(无答案),共11页。试卷主要包含了 探究醋蛋液,09g/L等内容,欢迎下载使用。
这是一份2022中考化学实验探究题:酸的性质探究(必考型)(无答案),共13页。
这是一份2022中考化学实验探究题:酸的性质探究(拔高型)(无答案),共8页。试卷主要包含了 硝酸是实验室常见的一种酸等内容,欢迎下载使用。









