


还剩19页未读,
继续阅读
初中化学人教版九年级上册课题4 化学式与化合价课文ppt课件
展开
这是一份初中化学人教版九年级上册课题4 化学式与化合价课文ppt课件,共27页。PPT课件主要包含了Mg2+,Al3+,Cl-,O2-,AlCl3,氢氧化,氯化铵等内容,欢迎下载使用。
认识常见元素的的化合价(重点、难点)了解化合价的一般规律(重点、难点)掌握化合价的应用(重点、难点)
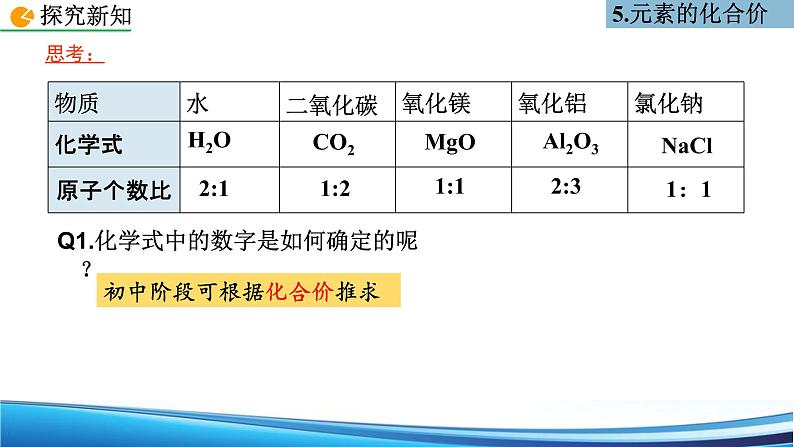
Q1.化学式中的数字是如何确定的呢?
初中阶段可根据化合价推求
Q1.什么是化合价?化合价与物质的组成有什么关系?
定义:元素的化合价是元素的原子之间形成化合物时表现出来的一种性质,用来表示原子之间相互化合的数目。
例:用化学用语表示+1价的钠元素
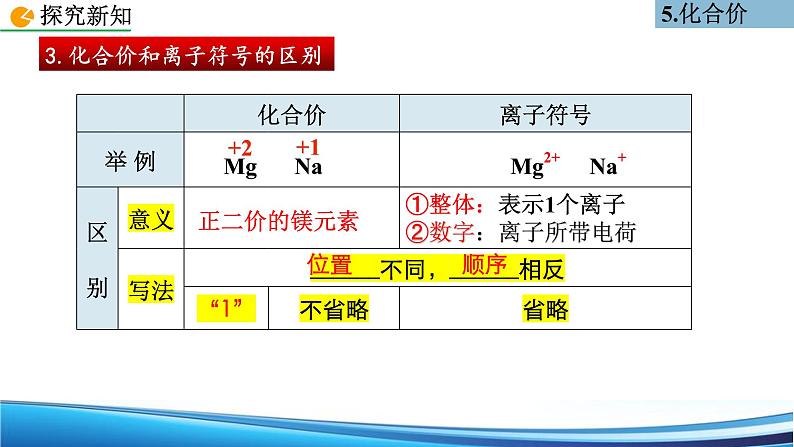
3.化合价和离子符号的区别
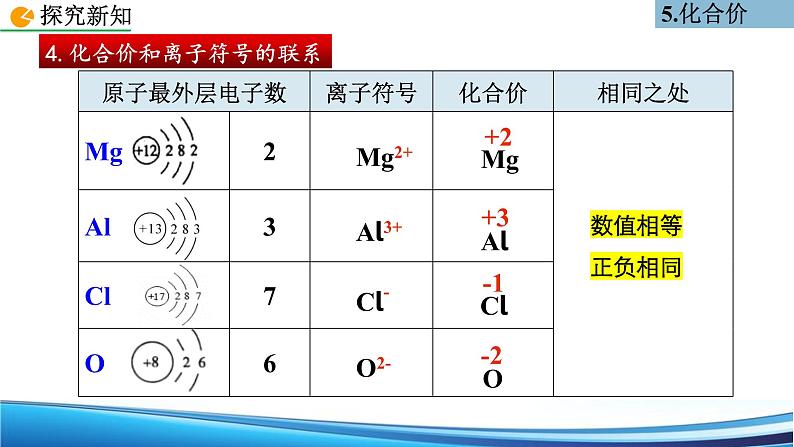
4.化合价和离子符号的联系
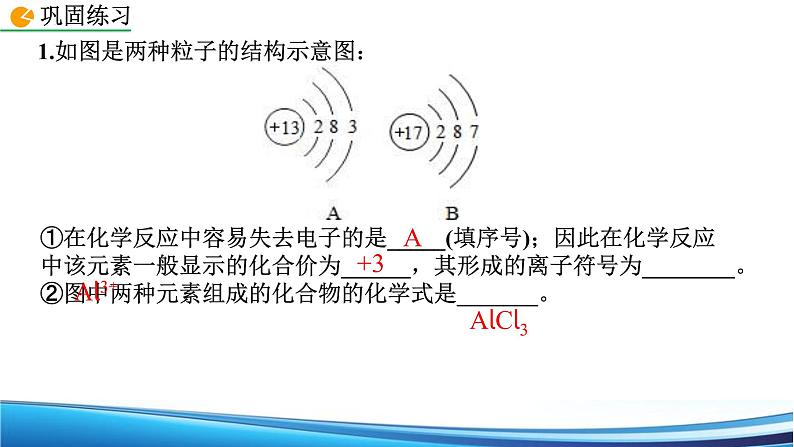
①在化学反应中容易失去电子的是_____(填序号);因此在化学反应中该元素一般显示的化合价为______,其形成的离子符号为________。②图中两种元素组成的化合物的化学式是_______。
1.如图是两种粒子的结构示意图:
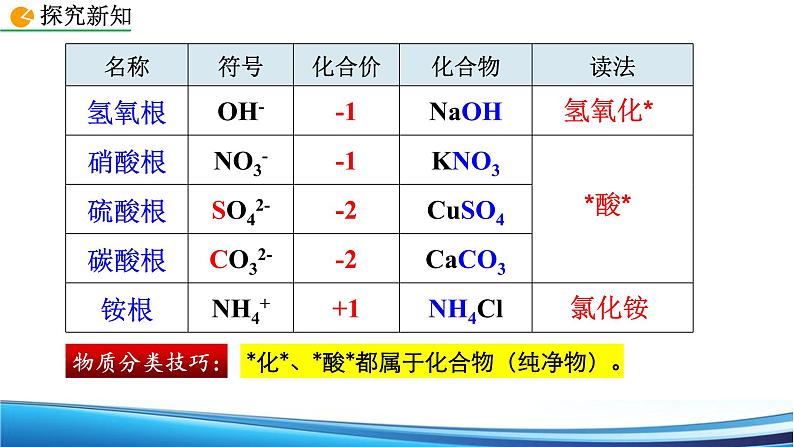
SO42-
一个硫酸根带两个单位的负电荷
1个硫酸根含有4个氧原子
原子团:整体可看作一个离子,又叫根。
2.一种元素可能有多种化合价。
3.不同种元素的化合价可能相同。
4.原子团作为一个整体参加反应,就好像原子一样。
通过观察你能发现哪些规律?
2)化合物里,正负化合价代数和为零。
CaOAl2O3 Fe2O3Cl2 HClOHClFe3O4
1)单质里元素的化合价为零。
3)金属元素通常显正价,非金属元素通常显负价。
4)在化合物里氢通常显+1价,氧通常显-2价。
5)一些元素具有多种化合价。一些元素在不同物质中可显不同的化合价,在同一物质里,同一元素也可显不同的化合价。
6)在原子团中,元素化合价的代数和为原子团的化合价
标出下列物质中标红元素的化合价
H2SO3 H2SO4 HNO3 HNO2H2CO3 H3PO4 HClO3 HClO4
3)金属元素通常显正价,非金属元素通常显负价
5)在原子团中,元素化合价的代数和为原子团的化合价
6)一些元素具有多种化合价。一些元素在不同物质中可显不同的化合价,在同一物质里,同一元素也可显不同的化合价。
1.氧化镁中镁元素的化合价为。
2.标出“MgO”中镁元素的化合价。
4.标出“KMnO4”中锰元素的化合价。
3.高锰酸钾中锰元素的化合价为 。
水中氢元素的化合价为+1价
氢元素的化合价为+1价
1个水分子含有2个氢原子
5.高锰酸钾中锰元素显+7价 。
例1试确定氯酸钾中氯元素的化合价(一遍过P48T6)
①根据化学式求元素化合价
依据:化合物里正负化合价的代数和为零
1.标出下列物质中各元素的化合价
Cu2 (OH)2CO3
1.标出画线元素的化合价(一遍过P48T10)
Fe2O3(氧化铁) FeO(氧化亚铁)Fe2+(亚铁离子)Fe3+(铁离子)KMnO4(高锰酸钾) K2MnO4(锰酸钾)NH4NO3(硝酸铵) SO42- H2O2
2.标出下列物质中标红元素的化合价
Cu2OCuOFeOFe2O3 Fe3O4 MnCl2MnO2 K2MnO4 KMnO4 HClHClOKClO3 HClO4H2SSO2H2SO4COCO2N2ONO NaNO2NO2 N2O5NH4NO3PH3P2O5P2O3
Cu+亚铜离子Cu2+铜离子Fe2+亚铁离子Fe3+铁离子
一价氢氯钾钠银,二价氧钙钡镁锌,三铝四硅五价磷,二三铁、二四碳,二四六硫都齐全,氟氯溴碘负一价,一至五价都有氮,氢一氧二为标准,铜汞二价最常见。负一硝酸氢氧根,负二硫酸碳酸根,负三记住磷酸根,正一价的是铵根,化合物中和为零,单质零价永不变。
②根据元素化合价求化学式
例2 已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式。
1)写元素符号(左正右负)标化合价(正上)
2)求化合价绝对值的最小公倍数
3)求各元素的原子个数
4)写化学式(原子个数写元素符号右下方)
P:6/3=2O:6/2=3
P:10/5=2O:10/2=5
(+5)×2+(-2)×5=0
(+3)×2+(-2)×3=0
根据元素的化合价写化学式可按以下步骤
左正右负,标价交叉,约简复查。
例2 已知磷、硫的氧化物,其中磷的化合价分别为+3和+5,硫的化合价分别为+4和+6,写出这几种氧化物的化学式。
注意:H2O2, Na2O2不用约分。
正价前,负价后;金在左,非金右;氧化物氧在后;个数1可省略;原子数不能漏。
3.已知:Ca为+2价,OH为-1价,写出它们的化学式4.已知:Mg为+2价,SO4为-2价,写出它们的化学式
5.笑气是人类最早应用的医疗麻醉剂之一,它是氮的一种氧化物,该氧化物中氮元素的化合价是+1价,则笑气的化学式为()A.N2B.N2OC.N2O3D.NO2
1.含有原子团的化合物的化学式的书写
碳酸钙: _________ 碳酸钠:___________硫酸铝:__________ 硫酸铵:___________硫酸铁:__________硫酸亚铁:_________硝酸钠:__________硝酸钡:___________氢氧化钠:________ 氢氧化钙:_________
1.写出下列物质的化学式
硫酸钠硝酸铜碳酸钡硝酸铝硝酸铵氢氧化钙
氯化亚铁氯化镁氯化铁硫化锌二氧化硅氧化铜
2.写出下列离子之间形成化合物的化学式和物质名称(一遍过P48T11)
1.(2017·河南)地中含量最的金属元素所形成的氧化物的化学式为 。2.(2019·河南)地壳中含量居前两位的元素所形成化合物的化学式为 。
教材P89:2(4)、3、4
认识常见元素的的化合价(重点、难点)了解化合价的一般规律(重点、难点)掌握化合价的应用(重点、难点)
Q1.化学式中的数字是如何确定的呢?
初中阶段可根据化合价推求
Q1.什么是化合价?化合价与物质的组成有什么关系?
定义:元素的化合价是元素的原子之间形成化合物时表现出来的一种性质,用来表示原子之间相互化合的数目。
例:用化学用语表示+1价的钠元素
3.化合价和离子符号的区别
4.化合价和离子符号的联系
①在化学反应中容易失去电子的是_____(填序号);因此在化学反应中该元素一般显示的化合价为______,其形成的离子符号为________。②图中两种元素组成的化合物的化学式是_______。
1.如图是两种粒子的结构示意图:
SO42-
一个硫酸根带两个单位的负电荷
1个硫酸根含有4个氧原子
原子团:整体可看作一个离子,又叫根。
2.一种元素可能有多种化合价。
3.不同种元素的化合价可能相同。
4.原子团作为一个整体参加反应,就好像原子一样。
通过观察你能发现哪些规律?
2)化合物里,正负化合价代数和为零。
CaOAl2O3 Fe2O3Cl2 HClOHClFe3O4
1)单质里元素的化合价为零。
3)金属元素通常显正价,非金属元素通常显负价。
4)在化合物里氢通常显+1价,氧通常显-2价。
5)一些元素具有多种化合价。一些元素在不同物质中可显不同的化合价,在同一物质里,同一元素也可显不同的化合价。
6)在原子团中,元素化合价的代数和为原子团的化合价
标出下列物质中标红元素的化合价
H2SO3 H2SO4 HNO3 HNO2H2CO3 H3PO4 HClO3 HClO4
3)金属元素通常显正价,非金属元素通常显负价
5)在原子团中,元素化合价的代数和为原子团的化合价
6)一些元素具有多种化合价。一些元素在不同物质中可显不同的化合价,在同一物质里,同一元素也可显不同的化合价。
1.氧化镁中镁元素的化合价为。
2.标出“MgO”中镁元素的化合价。
4.标出“KMnO4”中锰元素的化合价。
3.高锰酸钾中锰元素的化合价为 。
水中氢元素的化合价为+1价
氢元素的化合价为+1价
1个水分子含有2个氢原子
5.高锰酸钾中锰元素显+7价 。
例1试确定氯酸钾中氯元素的化合价(一遍过P48T6)
①根据化学式求元素化合价
依据:化合物里正负化合价的代数和为零
1.标出下列物质中各元素的化合价
Cu2 (OH)2CO3
1.标出画线元素的化合价(一遍过P48T10)
Fe2O3(氧化铁) FeO(氧化亚铁)Fe2+(亚铁离子)Fe3+(铁离子)KMnO4(高锰酸钾) K2MnO4(锰酸钾)NH4NO3(硝酸铵) SO42- H2O2
2.标出下列物质中标红元素的化合价
Cu2OCuOFeOFe2O3 Fe3O4 MnCl2MnO2 K2MnO4 KMnO4 HClHClOKClO3 HClO4H2SSO2H2SO4COCO2N2ONO NaNO2NO2 N2O5NH4NO3PH3P2O5P2O3
Cu+亚铜离子Cu2+铜离子Fe2+亚铁离子Fe3+铁离子
一价氢氯钾钠银,二价氧钙钡镁锌,三铝四硅五价磷,二三铁、二四碳,二四六硫都齐全,氟氯溴碘负一价,一至五价都有氮,氢一氧二为标准,铜汞二价最常见。负一硝酸氢氧根,负二硫酸碳酸根,负三记住磷酸根,正一价的是铵根,化合物中和为零,单质零价永不变。
②根据元素化合价求化学式
例2 已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式。
1)写元素符号(左正右负)标化合价(正上)
2)求化合价绝对值的最小公倍数
3)求各元素的原子个数
4)写化学式(原子个数写元素符号右下方)
P:6/3=2O:6/2=3
P:10/5=2O:10/2=5
(+5)×2+(-2)×5=0
(+3)×2+(-2)×3=0
根据元素的化合价写化学式可按以下步骤
左正右负,标价交叉,约简复查。
例2 已知磷、硫的氧化物,其中磷的化合价分别为+3和+5,硫的化合价分别为+4和+6,写出这几种氧化物的化学式。
注意:H2O2, Na2O2不用约分。
正价前,负价后;金在左,非金右;氧化物氧在后;个数1可省略;原子数不能漏。
3.已知:Ca为+2价,OH为-1价,写出它们的化学式4.已知:Mg为+2价,SO4为-2价,写出它们的化学式
5.笑气是人类最早应用的医疗麻醉剂之一,它是氮的一种氧化物,该氧化物中氮元素的化合价是+1价,则笑气的化学式为()A.N2B.N2OC.N2O3D.NO2
1.含有原子团的化合物的化学式的书写
碳酸钙: _________ 碳酸钠:___________硫酸铝:__________ 硫酸铵:___________硫酸铁:__________硫酸亚铁:_________硝酸钠:__________硝酸钡:___________氢氧化钠:________ 氢氧化钙:_________
1.写出下列物质的化学式
硫酸钠硝酸铜碳酸钡硝酸铝硝酸铵氢氧化钙
氯化亚铁氯化镁氯化铁硫化锌二氧化硅氧化铜
2.写出下列离子之间形成化合物的化学式和物质名称(一遍过P48T11)
1.(2017·河南)地中含量最的金属元素所形成的氧化物的化学式为 。2.(2019·河南)地壳中含量居前两位的元素所形成化合物的化学式为 。
教材P89:2(4)、3、4













