



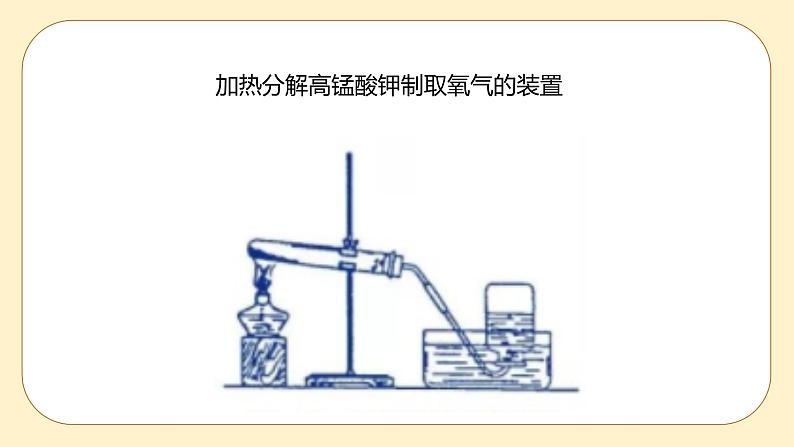


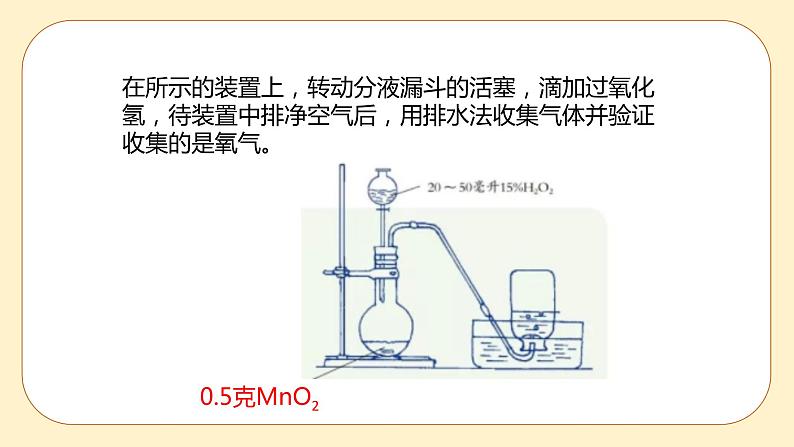



科学八年级下册第1节 空气与氧气精品ppt课件
展开3.1 空气与氧气 第3课时
一、选择题
1.工业上制取大量氧气的方法是( )
A.加热双氧水 B.加热高锰酸钾 C.分离液态空气 D.加热二氧化锰
2.催化剂在化学反应时以及反应前后:①不参加化学反应;②质量不变;③化学性质改变;④化学性质不变;⑤只能加快反应速度;⑥若用双氧水制氧气时忘了添加二氧化锰,则会使氧气的产量减少;⑦二氧化锰可以作为各种化学反应的催化剂。在上述说法中正确的是( )
A.①②④ B.②④⑤⑥ C.②④ D.②③⑤⑦
3.现有两包等质量的固体,其中a包是纯净的氯酸钾,b包是氯酸钾和少量二氧化锰的混合物,分别在酒精灯上加热来制取氧气,当完全反应后,收集到的气体与加热时间的关系为( )
A. B.
C. D.
4.某气体即能用排水法收集,又能用间下排空气法收集。该气体可能具有的性质是( )
A.易溶于水、密度比空气小 B.不易溶于水、密度比空气小
C.易溶于水、密度比空气大 D.不易溶于水、密度比空气大
5.有两份质量相等的固体和,是纯净的氯酸钾,是混有少量高锰酸钾的氯酸钾,将它们分别均匀加热,则图中关于放出氧气的质量和时间的关系图像正确的是…( )
A. B.
C. D.
6.如图是“用双氧水制取一瓶氧气”实验的主要步骤,其中操作错误的是( )
A.放入药品 B.收集气体
C.检查装置气密性 D.验满
7.乐乐用二氧化锰催化分解双氧水的实验中,发现反应速度先快后慢。他猜测该反应为放热反应,温度升高加快了反应。为此,他采用恒温箱、气体发生装置设计了如下表所示的两组实验:
组别 | 温度 | 双氧水量 | 双氧水溶质质量分数 | 二氧化锰 |
甲 | 25℃ | 10克 | 10% | 0.5克 |
乙 | 55℃ | 10克 | 10% | 0.5克 |
若乐乐的猜想正确,则实验制得氧气的质量随时间变化的曲线图正确的是( )A. B.
C. D.
8.某同学误将少量 KMnO4当成 MnO2加入 KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是( )
A.c 代表氧气 B.t2时刻,O2开始产生
C.t1 时刻,KMnO4开始分解 D.起催化作用物质的质量一直保持不变
9.下列图像符合描述情况的是( )
A. ①中表示:用KMnO4制取氧气时,随着反应进行,MnO2质量发生的变化
B. ②中表示:a、b两试管中分别装有等质量等浓度的双氧水,并向a试管中放入催化剂后,随着反应的进行,氧气的生成情况
C. ③中表示:用KMnO4制取氧气时,随着反应的进行,试管中剩余的固体质量变化情况
D. ④中表示:用双氧水制取氧气时,生成的氧气质量的变化情况
10.图像可以直观地表示化学反应中物质质量的变化。现有两份相同的双氧水,分别在有、无二氧化锰的情况下发生分解反应,下列图像能大致反映实验过程的是( )
A. B.
C. D.
11.图示为有关氧气的知识结构图(部分反应条件省略,参加反应的氧气为足量)。下列相关说法合理的是( )
A.反应后④为CO2,⑤为Fe2O3
B.氧气与C、P、Fe发生放热的化合反应
C.用反应①制造氧气时,MnO2是反应物
D.②③两种方法制取氧气时,都不需要检查气密性
二、填空题
12.下图是实验室用氯酸钾和二氧化锰的混合物制取氧气装置,结合所学知识回答下列问题:
(1)请写出图中带有标号仪器的名称:①________。
(2)实验中制取的氧气可以用上图中的_________(填字母)装置来收集。
(3)用制得的氧气完成D装置所示实验,该实验的现象是________。
13.下图是实验室制取气体的常用装置,请回答下列问题:
(1)仪器a的名称是___________。
(2)选用双氧水和二氧化锰制取氧气时,应选用___________(选填*A"或“B")作为气体发生装置。
(3)选用D装置作为氧气收集装置,氧气从___________(选填“a"或“b")管进入。
14.水是常见的溶剂,也是新能源——氢气的重要来源,请回答问题:
(1)如图,水电解实验中,检验试管D中的气体,发现它能使带火星的木条复燃,以此判断D中气体为______;
(2)水电解实验说明水是由______和______组成的;
(3)水是较好的溶剂,许多物质都能溶于水中形成溶液,下列物质属于溶液的是______。(填字母)
A.牛奶 B.泥水 C.肥皂水 D.矿泉水
15.实验室制取氧气的两种方法如下:
方法一:H2O2用二氧化锰作催化剂制O2;方法二:KMnO4加热制O2
(1)两种方法涉及的化学反应都是___________反应(填化学反应基本类型)。
(2)如图是实验室制取、干燥和收集气体的装置图。仪器A的名称是___________,现用方法一制取一瓶干燥的氧气,请按气体流向,用导管的编号将装置连接好___________。(浓硫酸具有吸水性,可作干燥剂)
三、探究题
16.某兴趣小组同学对“双氧水分解产生氧气的速率与哪些因素有关”这一问题展开探究。
| 双氧水的质量 | 双氧水的浓度 | ? |
Ⅰ | 50.0g | 1% |
|
Ⅱ | 50.0g | 2% |
|
Ⅲ | 50.0g | 4% |
|
(1)上述表格中?处应填的内容是___________。
(2)根据表格的设计,实验探究的问题是:___________。
(3)本实验中,测量O2体积的装置是图___________。
17.实验室常用二氧化锰催化过氧化氢分解的方法制取氧气。那么影响过氧化氢分解快慢的因素到底有哪些呢?某兴趣小组对此进行如下研究:
【提出问题】影响过氧化氢分解快慢的因素有哪些?
【猜想与假设】
假设1:过氧化氢溶液的浓度。
假设2:催化剂的质量。
假设3:温度。
【设计实验】小明同学设计如下实验方案进行验证。
序号 | H2O2溶液的浓度 | H2O2溶液的质量 | 温度 | MnO2的质量 | 收集O2的体积 | 时间 |
① | 5% | 12 g | 20℃ | 0.2g | 25 mL | 10 s |
② | 15% | 12 g | 20℃ | 0.2g | 25mL | 5s |
③ | 15% | 12 g | 40℃ | 无 | 25 mL | 80s |
【讨论交流】
(1)图中A装置的名称是______。
(2)通过对比实验①和②可知,过氧化氢分解的快慢与______有关。
(3)小红同学认为实验中用排水法收集氧气的目的是______。
(4)小辉同学提出小明的方案无法验证温度对过氧化氢分解快慢的影响,请你帮他说出理由:______。
18.小明查阅资料得知:除二氧化锰外,许多水果对过氧化氢分解也有催化作用。为了探究苹果质量对过氧化氢分解速度的影响,用如图甲所示装置(固定装置未画出)进行以下实验。
(1)检查装置气密性。
(2)称取1克苹果,切成小块放入烧瓶中,量取10毫升溶质质量分数为5%的过氧化氢溶液倒入烧瓶中,迅速塞紧塞子,当液滴移至A点时开始计时。
(3)当观察到液滴恰好至B点时(AB间玻璃管容积为6毫升),记录所需时间。
(4)依次用不同质量的苹果重复步骤2和3,记录并处理数据,结果如图乙。
①小明把烧瓶放在盛有水的水槽中进行实验,目的是为了保持温度不变。温度升高会导致液滴移动变快,原因是_______________(例举一个)
②第(3)步除了可以用记录液滴移动相同距离所用时间来比较分解速度外,还可以用什么方法来比较_______________。
③本实验可得出的结论是_____________。
④若用20毫升5%的过氧化氢溶液与6克苹果重复上述实验,预测实验中步骤3记录的时间是________秒。
参考答案:
1.C
【解析】
【分析】
【详解】
工业上制取氧气,先将空气液化,然后利用氧气和氮气的沸点不同,从而将二者分离得到氧气,故C正确,而A、B、D错误。
故选C。
2.C
【解析】
【分析】
【详解】
催化剂参加化学反应,只是反应后又会生成回来,选项错误;
②化学反应前后,催化剂的质量不变,选项正确;
③化学反应前后,催化剂的化学性质保持不变,选项错误;
④化学反应前后,催化剂的化学性质保持不变,选项正确;
⑤催化剂能够改变化学反应的速率,即有些催化剂使化学反应速率加快,有些催化剂使化学反应速率减慢,选项错误;
⑥催化剂只改变化学反应的速率,不改变反应物与生成物的质量关系,即用双氧水制氧气时忘了添加二氧化锰,则氧气的产量不变,选项错误;
⑦二氧化锰可以作为过氧化氢制取氧气的反应的催化剂,但并不是各种化学反应的催化剂都说二氧化锰,选项错误;
正确选项是②④,故选C。
3.C
【解析】
【分析】
【详解】
A、a包氯酸钾多生成氧气多,b包中的二氧化锰是催化剂,不能反应生成氧气,所以氯酸钾质量少,生成氧气少,图像不符,选项错误;
B、氯酸钾分解需要一定温度,反应开始不是从原点,选项错误;
C、b包是氯酸钾和少量二氧化锰的混合物,二氧化锰是催化剂,反应开始的早,但是氯酸钾的质量少,生成氧气少,图像相符,选项正确;
D、b包是氯酸钾和少量二氧化锰的混合物,反应开始的早,图像不相符,,选项错误,故选C。
4.B
【解析】
【详解】
某气体能用排水法收集,说明该气体不易溶于水;能用向下排空气法收集,说明该气体的密度小于空气。某气体既能用排水法收集,又能用向下排空气法收集。该气体可能具有的性质是不易溶于水、密度比空气小。故选B。
5.C
【解析】
【分析】
有两份质量相等的固体 A 和 B , A 是纯净的氯酸钾, B 是混有少量高锰酸钾的氯酸钾,将它们分别均匀加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,二氧化锰做了氯酸钾的催化剂,产生的氧气速率B比A大;但是B为混有少量高猛酸钾的氯酸钾,A为纯净的氯酸钾,所以A最终产生的氧气比B多。
【详解】
A、该图表示A反应速率大,产生的氧气多,不符合题意;
B、该图表示B反应速率大,产生的氧气多,不符合题意;
C、该图表示B反应速率大,产生的氧气少,符合题意;
D、该图表示A反应速率大,产生的氧气一样多,不符合题意;
故选:C。
6.D
【解析】
【分析】
【详解】
A、倾倒液体时,取下瓶塞倒放在桌面上,标签朝向手心持瓶,瓶口紧靠试管口缓缓倒入液体,选项正确;
B、氧气的密度大于空气的密度,采用向上排空气法收集气体时,集气瓶口朝上,将导管伸进瓶底附近收集氧气,选项正确;
C、检查装置气密性时,将导管的出气端浸入水中,手紧握试管外壁,观察到导管口处产生气泡,表明装置气密性良好,选项正确;
D、用带火星木条验满氧气时,应将带火星木条伸到集气瓶口处,不能伸进瓶内,选项错误;
故选D。
7.D
【解析】
【分析】
【详解】
若乐乐的猜想正确,即温度越高,反应越快,则相同时间内,乙中生成氧气的质量大于甲,即乙的图像比甲的图像倾斜角度更大。温度高低,只影响反应的快慢,不会影响最终生成氧气的质量,即生成氧气的质量相同,故D正确,而A、B、C错误。
故选D。
8.C
【解析】
【分析】
【详解】
根据高锰酸钾加热生成二氧化锰可以做催化剂,同时生成氧气;氯酸钾在二氧化锰做催化剂和加热的条件下生成氧气。
判断图中a:氯酸钾,b:高锰酸钾,c:氯化钾;t1时刻,KMnO4开始分解产生氧气;起催化作用物质是高锰酸钾分解产生的二氧化锰,随着加热反应进行其质量先增大,直至高锰酸钾完全分解后,二氧化锰质量保持不变。
故选C。
9.D
【解析】
【分析】
【详解】
A、此反应中,二氧化锰是生成物,反应开始后,二氧化锰的质量从零开始不断增加,直到高锰酸钾完全分解后质量不再变化,选项错误;
B、在a、b两支试管里分别装有等质量的双氧水溶液,催化剂只能加快化学反应速率,不影响产生氧气的质量,所以产生的氧气的质量相等,选项错误;
C、加热高锰酸钾会生成氧气、锰酸钾和二氧化锰,所以随着加热的不断进行固体的质量不断减小,直至反应结束后只剩下锰酸钾与二氧化锰,固体质量不再减少,但反应后固体的质量不为零,选项错误;
D、双氧水制取氧气时,双氧水分解生成氧气,随着双氧水的质量不断增加,生成氧气的质量也会不断增加,选项正确;
故选D。
10.C
【解析】
【分析】
【详解】
两份相同的双氧水,分别在有、无二氧化锰的情况下发生分解反应,加二氧化锰的双氧水分解速率快,但双氧水放出氧气的质量与有无催化剂无关,生成的氧气的质量相等。
故选C。
11.B
【解析】
【分析】
【详解】
A、铁在氧气中点燃生成四氧化三铁,故A错误。
B、C、P、Fe分别在氧气中点燃生成二氧化碳、五氧化二磷和四氧化三铁,反应均放出大量热,且为化合反应,故B正确。
C、反应①表示过氧化氢溶液在二氧化锰的催化下产生氧气,二氧化锰是催化剂,不参与反应,故C错误。
D、②③两种方法制取氧气时,采用的分别是加热高锰酸钾、氯酸钾的方法,都需要检查气密性,故D错误。
故选B。
12. 铁架台 C 剧烈燃烧、火星四射、生成黑色固体、放出大量的热
【解析】
【分析】
【详解】
(1)仪器①的名称叫铁架台。
(2)氧气的密度大于空气,因此用向上排空气法收集,故选C。
(3)用制得的氧气完成D装置所示实验,该实验的现象是:剧烈燃烧、火星四射、生成黑色固体、放出大量的热。
13. 长颈漏斗 A a
【解析】
【分析】
【详解】
(1)仪器a的名称是长颈漏斗。
(2)实验室用过氧化氢和二氧化锰混合物制取氧气,该反应是固液不加热型,发生装置选A。
(3)氧气的密度比空气略大,用装置D收集氧气,气体应从导管口a端通入。
14. 氧气 氢##(氢元素) 氧##(氧元素) D
【解析】
【详解】
(1)电解水实验中,正氧负氢,氢二氧一。 氧气能使带火星的木条复燃,该实验中,发现试管D中的气体能使带火星的木条复燃, 以此判断D中气体为氧气;
(2)水电解时,生成氢气和氧气,根据化学反应前后各种元素的种类不变,水电解实验说明水是由氢元素和氧元素组成的。
(3)A.牛奶不能溶于水形成溶液,此选项不符合题意;B.泥水不能溶于水形成溶液,此选项不符合题意;C.肥皂水不能溶于水形成溶液,此选项不符合题意;D.矿泉水能溶于水形成溶液,此选项符合题意。故选D。
15. 分解 分液漏斗 ①③④⑧⑦(或①③④⑧)
【解析】
【分析】
【详解】
(1)制取氧气的两种方法中,反应物只有一种,而生成物有多种,因此它们都是分解反应。
(2)根据图片可知,仪器A的名称为分液漏斗。
使用方法一制取氧气时,由于反应物为液体和固体,不需加热,因此发生装置选择“固液常温型”,故选①;用浓硫酸进行干燥;氧气的密度大于空气,应该用“向上排空气法”收集。干燥氧气时,氧气必须进入浓硫酸中,因此①与③相连;收集氧气时,氧气的密度大于空气,则应该从长导管进入集气瓶,因此④与⑧相连,最终的连接顺序为①③④⑧⑦。
16. 相同时间产生氧气的体积多少或收集相同体积的氧气所用的时间 双氧水分解产生氧气的速率是否与双氧水的浓度有关? 3
【解析】
【分析】
【详解】
(1)表格中“?”应该填写用来表示产生氧气快慢的物理量,即相同时间产生氧气的体积多少或收集相同体积的氧气所用的时间。
(2)根据表格可知,双氧水的质量相同而溶液浓度不同,因此实验探究的问题为:双氧水分解产生氧气的速率是否与双氧水的浓度有关?
(3)测量氧气体积的装置中,应该短导管通入氧气,长导管排出水,故选丙。
17. 分液漏斗 过氧化氢溶液的浓度 排水法能准确测定收集氧气的体积 方案中没有温度不同、其他变量全部相同的对照实验
【解析】
【详解】
(1)图中A装置的名称是分液漏斗。
(2)通过对比实验①和②可知,过氧化氢分解的快慢与过氧化氢溶液的浓度有关。
(3)收集氧气的方法有两种,向上排空气法和排水法,向上排空气法无法准确测量氧气的体积,排水法可准确测量氧气的体积,所以小红同学认为实验中用排水法收集氧气。
(4)方案中没有温度不同、其他变量全部相同的对照实验,故小辉同学提出小明的方案无法验证温度对过氧化氢分解快慢的影响。
18. 温度升高导致生成的气体膨胀,体积变大(其他合理答案也可) 记录液滴在相同时间内移动的距离 过氧化氢溶液用量一定时,其分解速度随苹果质量的增大而增大,且增大得越来越慢 100(只要时间不超过150秒即可)
【解析】
【分析】
【详解】
(4)①过氧化氢分解会生成氧气,气体受热膨胀,体积变大,因此液滴移动速度会变快,所以需要保持温度不变。
②还可以记录液滴在相同时间内移动的距离来比较分解速度。
③根据图乙中信息可以看出,在一定量的过氧化氢溶液中,加入苹果的质量越大,产生氧气的速率越快,但是苹果质量增加到一定程度,速率增大幅度变小,说明增大越来越慢。
④此时加入苹果为6克,说明分解速率可达0.04毫升/秒,若不改变反应物的量,此时收集6毫升氧气需要的时间为150秒,而此时加入反应物量变大,因此也会提高反应速率,则预测时间为100秒(只要时间不超过150秒即可)。
初中浙教版第3章 空气与生命第1节 空气与氧气优质课ppt课件: 这是一份初中浙教版<a href="/kx/tb_c94224_t3/?tag_id=26" target="_blank">第3章 空气与生命第1节 空气与氧气优质课ppt课件</a>,文件包含31空气与氧气3pptx、31空气与氧气3教学设计表格式doc、31空气与氧气3学案含答案doc、双氧水制氧气mp4等4份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
科学八年级下册第1节 空气与氧气精品ppt课件: 这是一份科学八年级下册第1节 空气与氧气精品ppt课件,文件包含31空气与氧气第4课时课件pptx、31空气与氧气第4课时练习docx等2份课件配套教学资源,其中PPT共27页, 欢迎下载使用。
初中科学浙教版八年级下册第1节 空气与氧气完整版课件ppt: 这是一份初中科学浙教版八年级下册第1节 空气与氧气完整版课件ppt,文件包含31空气与氧气第2课时课件pptx、31空气与氧气第2课时练习docx等2份课件配套教学资源,其中PPT共21页, 欢迎下载使用。













