人教版课题2 原子的结构优秀ppt课件
展开(2) 原子在化学变化中可不可以再分?
(1) 原子有哪些特征?
原子是化学变化中的最小粒子原子的质量和体积很小原子在不停运动原子之间有间隔原子在化学变化中不可再分
1911年,卢瑟福认为原子的质量几乎全部集中在直径很小的核心区域,叫原子核,电子在原子核外绕核作轨道运动。原子核带正电,电子带负电。
汤姆逊认为原子是一个平均分布着正电荷的粒子,其中均匀地镶嵌着许多电子,中和了正电荷,从而形成了中性原子,人称葡萄干布丁模型。
19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。
1926年,奥地利学者薛定谔提出了电子云模型,电子云并不表示电子的实际运动轨迹,小黑点的疏密表示电子在核外空间单位体积内出现的机会的多少。
1913年,丹麦科学家玻尔提出了量子化的原子结构模型,即核外电子只能在限定的轨道内绕核运转,按能量高低而距离核远近不同。
年 级:九年级 学 科:化学(人教版)主讲人:路学丽 学 校:北京市西城外国语学校
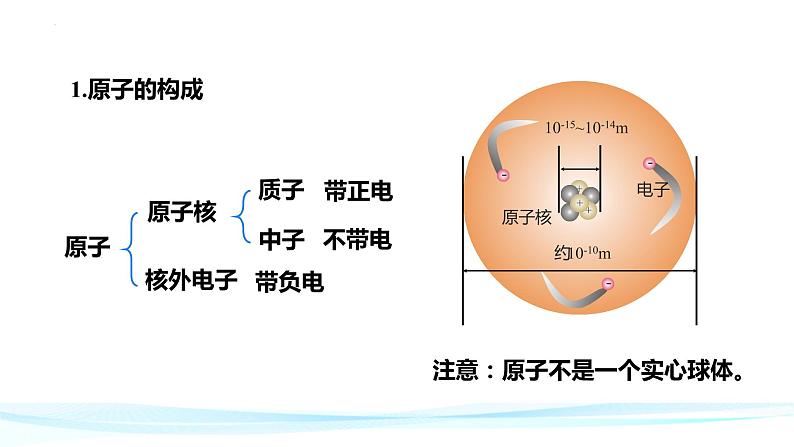
10-15~10-14m
注意:原子不是一个实心球体。
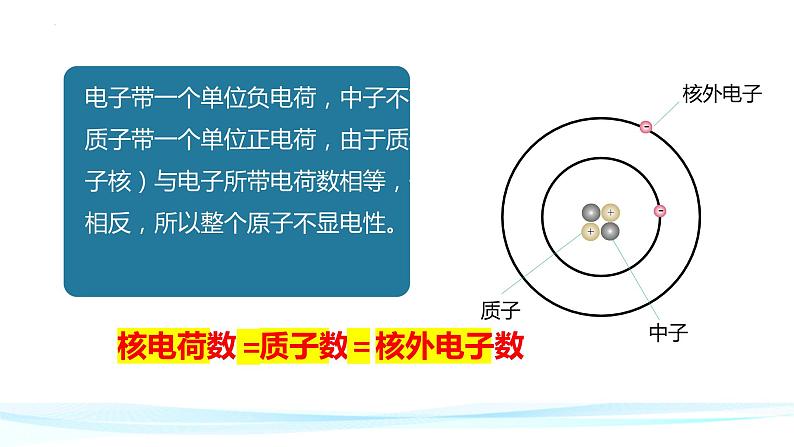
电子带一个单位负电荷,中子不带电,质子带一个单位正电荷,由于质子(原子核)与电子所带电荷数相等,但电性相反,所以整个原子不显电性。
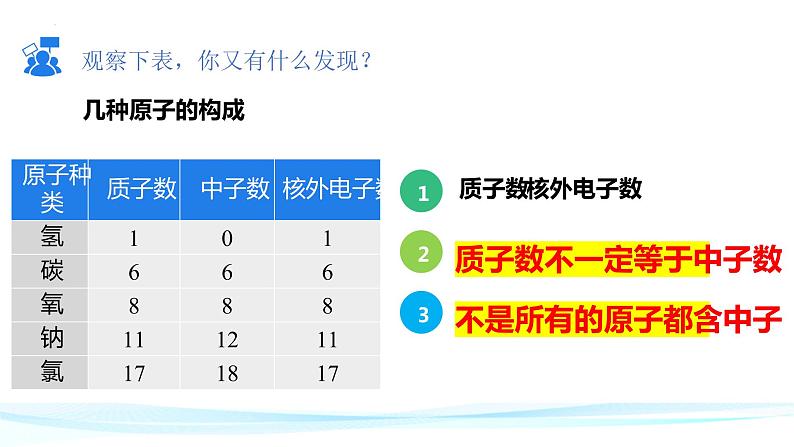
观察下表,你又有什么发现?
质子数不一定等于中子数
不是所有的原子都含中子
1、所有原子都是由质子、中子、电子构成的吗?
2、原子核内质子数和核外电子数相等吗?整个原子对外界显电性吗?
3、不同种原子之间质子数相等吗?
4、质子和中子能否再分?
质子和中子还能再分吗?
构成原子的粒子的和质量
观察下表,你有什么发现?
一个质子和一个中子的质量约相等。
原子的质量主要集中在原子核上。
在含有多个电子的原子里,有的电子通常在离核较近的区域运动,有的电子通常在离核较远的区域运动。为了形象说明,通常用电子层表示。
电子层: 离核远近: 能量高低:
一 二 三 四 五 六 七
低 高
近 远
离核最远的电子层叫作最外层,最外层电子数不超过 8 个;只有一层的,电子数不超过 2 个。
1~18号元素的原子结构示意图
观察质子数为1~18的原子结构示意图,说说你的发现。
原子种类与原子结构的关系
既不易得电子,也不易失电子
原子的最外层电子数决定原子的化学性质
稀有气体原子结构是相对稳定结构,金属原子和非金属原子都有达到相当稳定结构的趋势。如何达到呢?
钠原子和氯原子最外层电子分别为1个和7个,怎么样才能达到稳定结构呢?
用原子结构示意图解释钠与氯气的反应。
阳离子:带正电荷的原子或原子团。(质子数>电子数)
阴离子:带负电荷的原子或原子团。(质子数<电子数)
带电的原子或原子团叫做离子。
(1)离子符号的书写先写原子(或原子团)符号,再在符号的右上角标出离子所带的电荷数及电性,先写数字再写正负号,当离子所带电荷数为1时, 1 可以不写。
离子所带电荷数等于原子失去或得到的电子数
离子所带的电荷数与什么有关?
写出下列离子的离子符号。
1个氯离子带1个单位负电荷
1个铝离子带3个单位正电荷
原子与离子有什么区别和联系?
质子数=电子数(不带电荷)
质子数>电子数(带正电)
质子数<电子数(带负电)
1.右图为氯原子的结构示意图,下列有关说法错误的是( )A.氯原子的核电荷数为17B.氯原子最外层有7个电子C.氯原子的质子数为17D.在化学反应中氯原子容易失去电子
2.下列说法中正确的是( )A.结构示意图为 的粒子一定是氖原子 B.M2+的核电荷数是12,则其核外电子数为14C.Na和Na+的化学性质相同 D.原子变成离子时,得失电子都有可能
3. 根据下图所示的粒子结构示意图,回答问题:
① ② ③ ④ ⑤ ⑥
(1)属于相对稳定结构的是_________;(2)核电荷数相同的的是______;(3)在反应中易失电子的是_____,易得电子的是_____;(4)属于原子的是____________,属于阳离子的是______;属于阴离子的是______;
(5)属于稀有气体原子的是_______,属于金属原子的是______,属于非金属原子的是______;(6)与①化学性质相似的是_______;(7)图中粒子的符号分别为:_______________________________。
一个原子的实际质量太小啦!书写和使用都不方便!说说你有何建议?
例:碳12原子的质量为1.993×10-26kg,一种氢原子的质量为1.67 × 10-27 kg,计算该氢原子的相对原子质量。
解:该氢原子的相对原子质量为
1.67 × 10-27kg
1993×10-26kg×1/12
①相对原子质量不等于原子的实际质量,是个比值。②原子实际质量越大,它的相对原子质量数值越大。③相对原子质量的单位:“1”(书写时一般不写出)。原子实际质量的单位是:千克。
相对原子质量与原子实际质量的关系
原子质量一个质子质量×质子数 + 一个中子质量×中子数
1.67×10-27 kg
1.66×10-27 kg
相对原子质量 约等于 质子数 + 中子数
m(原子)=m(质子)+ m(中子) =m(原子核)
相对原子质量与质子数和中子数的关系
相对原子质量=质子数+中子数
从表中你发现了什么规律?
1.已知原子的核电荷数,可以确定它的( )A.相对原子质量 B.质子数 C.中子数 D.电子数
2.原子中决定相对原子质量大小的主要微粒是( )A.质子数和电子数 B.核电荷数 C.中子数和电子数 D.质子数和中子数
人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构精品作业ppt课件: 这是一份人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构精品作业ppt课件,文件包含课件pptx、教案docx、作业doc、学案docx等4份课件配套教学资源,其中PPT共32页, 欢迎下载使用。
化学第三单元 物质构成的奥秘课题2 原子的结构示范课课件ppt: 这是一份化学第三单元 物质构成的奥秘课题2 原子的结构示范课课件ppt,共32页。PPT课件主要包含了微粒构成物质,金箔-黄金锤成的薄片,原子还能再分吗,请说出你的猜想,请说出你的证据,原子不能再分的证据,原子能再分的证据,电子的发现,建立模型,科学实验等内容,欢迎下载使用。
人教版九年级上册课题2 原子的结构说课课件ppt: 这是一份人教版九年级上册课题2 原子的结构说课课件ppt,共19页。PPT课件主要包含了一个单位正电荷,一个单位负电荷,难得失,易失去,不稳定,易得到,ABD,原子中子,改变了原来的,运动方向等内容,欢迎下载使用。