

2021威海威海文登区高三上学期期中考试化学试题含答案
展开高三化学
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。考试结束,将答题卡交回。
第Ⅰ卷(选择题 共40分)
注意事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、考试号、考试科目填涂在答题卡上。
2.每题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号,不能答在试题上。
相对原子质量:
H 1 Li 7 C 12 N 14 O 16 Na 23 Mg 24 S 32 Fe 56 C 59 Br 80 Ba 137
一、选择题(本题共10小题,每小题2分,共20分,每小题只有一个选项符合题意)
1.中国传统文化蕴含着很多科学知识,下列说法错误的是
A.唐·王建“内园分得温汤水,二月中旬已进瓜”,所利用的能源为地热能
B.宋·王希孟《千里江山图》中的绿色颜料铜绿的主要成分是碱式碳酸铜
C.《梦溪笔谈》记载“以剂钢为刃,柔铁为茎干,不尔则多断折”,说明铁合金的硬度比纯铁的高
D.《本草纲目》中“石碱”条目下记载“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面”,这里的“石碱”主要成分是KOH
2.下列物质组合正确的是
3.我国倡导低碳生活,减少二氧化碳的排放,“碳捕捉技术”可实现二氧化碳的分离、储存和利用。实际生产中,常利用NaOH溶液来“捕捉”CO2,其工艺流程如图所示(部分条件及物质未标出),下列说法正确的是
A.CO2是引起酸雨的主要物质之一
B.整个过程中,只有CO2可循环利用
C.能源消耗低是该技术的一大优点
D.该生产过程中,没有涉及到氧化还原反应
4.下列有关物质性质和用途说法错误的是
A.液氨可用作制冷剂
B.MgO熔点很高,可用于制造耐火材料
C.SO2可用作食品防腐剂
D.ClO2可用于杀菌消毒,H2O2不可以
5. 下列相关条件下的离子方程式书写正确的是
A. 过量铁粉与稀硝酸反应:Fe+NO3−+4H+═Fe3++NO↑+2H2O
B. 泡沫灭火器原理:2Al3++3CO32−+3H2O═2Al(OH)3↓+3CO2↑
C. 向Ca(HCO3)2溶液中加入足量Ca(OH)2溶液:Ca2++HCO3−+OH−═CaCO3↓+H2O
D. 向BaCl2溶液中通入少量SO2气体:Ba2++SO2+H2O=BaSO3↓+2H+
6.设NA为阿伏加德罗常数的值,下列说法正确的是
A.过量的铜与含0.2mlHNO3的浓硝酸反应,转移电子的数目大于0.1NA
B.100g质量分数17%H2O2溶液中含有H—O键数目为NA
C.标准状况下,11.2 L的HF中所含分子数为0.5NA
D.在K37C1O3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若反应中电子转移的数目为10NA则有420g氯气生成
7.硫酸盐(含SO42−、HSO4−)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下,下列说法错误的是
A.NO2是生成硫酸盐的氧化剂
B.该过程中SO3−为催化剂
C.硫酸盐气溶胶呈酸性
D.SO3−转化为HSO4−的方程式为:SO3−+NO2+H2O=HNO2+HSO4−
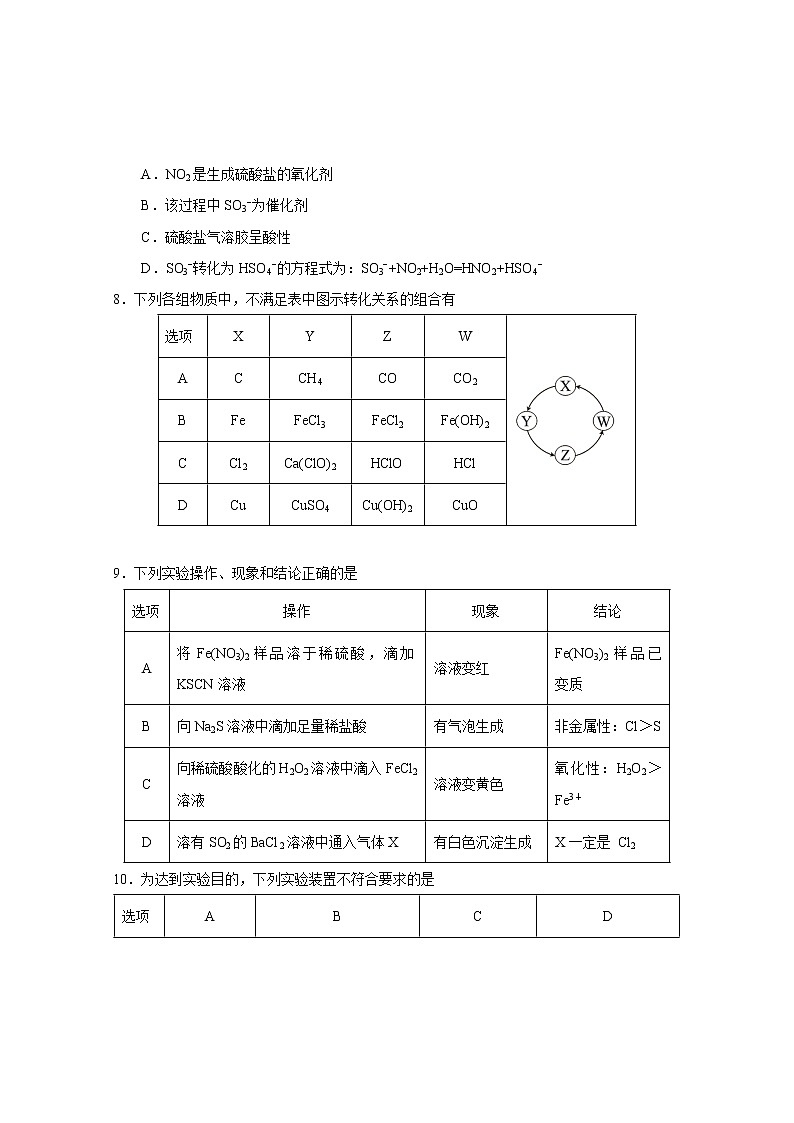
8.下列各组物质中,不满足表中图示转化关系的组合有
9.下列实验操作、现象和结论正确的是
10.为达到实验目的,下列实验装置不符合要求的是
二、选择题(本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分)
11.M、X、Y、Z、W是原子序数依次增大的短周期元素,Z的最外层电子数是次外层电子数的3倍,M和Y二者原子核外电子数之和等于W的原子核外电子数。由五种元素组成的化合物结构如图所示(箭头表示共同电子对由W提供)。下列说法正确的是
M+
X
Y
Z
W
Y
Z
Z
Z
W
A.最高价氧化物对应的水化物酸性:Y>X
B.M的氢化物是共价化合物
C.Y和Z可形成二种有毒的化合物
D.X和W组成的化合物中二原子都满足8电子稳定结构
12.处理某废水时,反应过程中主要存在HCO3−、N2、ClO−、CNO−、Cl−等微粒,反应过程中部分离子浓度与反应进程关系如图所示。下列说法错误的是
A.CNO−中C的化合价为+4价
B.反应过程中每有1ml HCO3−反应或生成,转移2mle−
C.该反应中,还原产物与氧化产物的物质的量之比为3:1
D.氧化性:ClO−>CNO−
13.部分短周期元素原子半径与原子序数的关系如图所示,下列说法错误的是
A.最高价氧化物对应水化物的碱性:M<Z
B.组成单质的熔点:Z<M<N
C.Y、R 两种元素气态氢化物的还原性:Y>R
D.简单离子的半径:R>M>Y
浓H2SO4
⑤
焦性没食子酸
③
②
④
①
水
气体产物
14.NH4ClO4为白色晶体,在高温条件下分解会产生三种单质气体和H2O(g),某研究小组在实验室设计如下装置检验NH4ClO4分解的产物。该小组连接好装置后,依次检查装置的气密性→装入试剂→通干燥的惰性气体排尽装置内的空气→将导管末端移入盛满水的试管→通入气体产物。已知:焦性没食子酸溶液用于吸收氧气,下列说法错误的是
A.NH4ClO4中Cl的化合价为+7价
B.NH4ClO4分解反应中O元素被还原
C.装置①、②、③、④中盛放的药品可以依次为无水硫酸铜、湿润的红色布条、饱和食盐水、Cu
D.装置⑤中收集的气体为N2
15.某含铬(Cr2O72−)废水用硫酸亚铁铵[FeSO4•(NH4)2SO4•6H2O]处理,回收得到a ml 磁性材料FeO•FeyCrxO3(Cr为+3价),其流程如图所示,则下列说法错误的是
加入
FeSO4•(NH4)2SO4•6H2O
含Cr2O72−废水
混合
溶液
加入NaOH溶液至
pH为9.0,过滤
焙烧
滤液
滤渣
FeO•FeyCrxO3
A.“滤渣”的主要成分为Cr(OH)3、Fe(OH)2、Fe(OH)3
B.消耗硫酸亚铁铵的物质的量为(3-x) a ml
C.反应中发生转移的电子物质的量为3ya ml
D.在FeO•FeyCrxO3中,x=1.5 y=0.5
高三化学
第Ⅱ卷
注意事项:第Ⅱ卷包括5小题,共60分,将答案写在答题卡上
16.(12分)
X、Y、Z、M、W为原子序数依次增大的短周期元素。已知:
①化合物MaYbXc中a、b、c均为整数,三者之和为13。
②取0.1 ml上述化合物与过量的水反应产生4.8g气体A,同时生成0.1ml白色胶状沉淀B,B既能溶于NaOH溶液,又能溶于盐酸。
③A是最简单的有机物,可导致地球表面温室效应不断增加。
④C、D、E、F、G五种物质均含有W元素,C为单质,E和F均为二元化合物且相对分子质量相差16。它们之间有如下转化关系。
C
D
E
F
G
⑤Z与W族序数相差5。
回答下列问题:
(1)Y和Z的名称分别为 、 。W在周期表中的位置为 。
(2)B、F的化学式分别为 、 。Y与W形成的二元化合物电子式为 。
(3)MaYbXc与水反应的化学方程式为 。
(4)在④中,D→E化学方程式为 。
(5)若C、D、E、F、G五种物质均含有Z元素,且发生如上图所示的转化关系。C为淡黄色固体,惰性电极电解F的水溶液可生成D和两种气体单质,则F→G的化学方程式为 。
17.(12分)
逐滴加稀盐酸
至过量
116.5g沉淀A
无明显
现象
滤液I
少量CO2
加过量
Ba(NO3)2溶液
加过量
NaOH溶液,△
4.48L(标准状况)无色气体Y
滤液Ⅱ
37.9g沉淀B
沉淀C
待测液
2.24L(标准状况)
无色气体X
某学习小组欲检测一失去标签的试剂瓶中固体物质的成分,将固体溶于水,形成的溶液中含有Na+、NH4+、Mg2+、Fe2+、SO32-、MnO4-、CO32-、SO42-中的若干种,取一定量待测液进行如下实验:
回答下列问题:
(1)该待测液中一定含有的离子是 ;无法确定是否含有的离子是 ;
(2)沉淀B的成分及物质的量为 (物质写化学式)。
(3)生成无色气体X时的离子方程式为 。
(4)生成沉淀C时的离子反应方程式为 。
(5)在催化剂、加热条件下气体X与气体Y可以反应转化为对环境无害的物质,该反应的化学方程式为 ,所得氧化产物与还原产物的质量之比为 。
18.(12分)
氢溴酸常用于合成镇静剂和麻醉剂等医药用品。下图是模拟工业制备质量分数为48.6%的氢溴酸的流程如下:
SO2
冰水
操作Ⅰ
反应室①
H2SO4
48.6%的氢溴酸
Br2
…
反应室②
Na2SO3
操作Ⅱ
BaSO4
少量Ba(OH)2
无色溶液
操作Ⅲ
混合溶液
粗品
已知:液溴的沸点为58.78℃。质量分数为48.6%的氢溴酸沸点为126℃。回答下列问题:
(1)反应室①使用冰水的目的为 。
(2)反应室②中发生反应的离子方程式为 。
(3)操作Ⅰ的装置如图所示(部分夹持装置省略),仪器a的名称是_________ ,装置中明显的错误是 。
a
水
碎瓷片
热水
(4)工业生产制得的氢溴酸常常有淡淡的黄色,可能的原因是 。
(5)工业上用黄铁矿(主要成分FeS2)在高温下制取SO2,其化学方程式为 。
(6)若开始加入m1g液溴,得到m2g48.6%的氢溴酸,则其产率为 。
19.(12分)
氮化锂(Li3N)是有机合成的催化剂,Li3N遇水剧烈反应,金属Li的化学性质与镁相似。某小组设计实验制备氮化锂并测定其纯度,装置如图所示:
Ⅰ、制备氮化锂:实验室用NH4Cl溶液和NaNO2溶液共热制备N2。选择下图中的装置制备氮化锂(装置可重复使用):
⑦
⑤
⑥
⑧
③
②
④
A
B
C
D
E
①
碱石灰
浓硫酸
水
(1)装置的接口连接顺序为 (从左至右,填数字序号)。
(2)实验室将锂保存在 (填“煤油”“石蜡油”或“水”)中。
(3)制备N2的化学方程式为 。
Ⅱ、测定Li3N产品纯度:取a g Li3N产品按如下图所示装置实验。
(4)连接好装置后,检查装置气密性的操作是 。装好药品,启动反应的操作是 。
量气管①
煤油
水准管
量气管②
水
水准管
ag产品
水
Y形管
(5)反应完毕并冷却之后,将气体全部排入量气管①中,量气管①的读数为V1 mL(已换算成标准状况,下同),将量气管①中气体缓慢导入量气管②,读数为V2 mL。该样品的纯度为 (用含a、V1、V2的代数式表示,不必化简)。若在量气管②中V2读数时,水准管液面高于左侧液面,测得产品纯度将 (填“偏高”“偏低”或“无影响”)。
20.(12分)
三氯化六氨合钴[C(NH3)6]Cl3 是一种微溶于水的配合物,是合成其它含钴配合物的原料。某学习小组以含钴废料(主要成分为C,含少量Fe、Al2O3、SiO2等杂质) 制取产品[C(NH3)6]Cl3的工艺流程如图所示:
盐酸
适量
NaClO3
粉碎
浸出液
酸浸
Na2CO3调pH
滤渣
滤液
盐酸调
pH至2~3
操作I
CCl2•6H2O
NH4Cl溶液、
氨水、H2O2
系列操作
产品
含钴
废料
回答下列问题:
(1)流程中加“适量 NaClO3”发生反应的离子方程式为 。
(2)“滤渣”的成分为 (填化学式)。
(3)操作Ⅰ的步骤包括 、减压过滤。
(4)流程中NH4Cl的作用除作反应物外,还可 。
(5)最后一步得到产品的化学方程式为 。
(6)通过碘量法可测定产品中钴的含量。称取10.0g产品,将产品中 [C(NH3)6]Cl3 转化成C3+后,加入过量KI 溶液,再用1.00ml·L−1Na2S2O3标准液滴定(淀粉溶液做指示剂),反应原理为:2C3++2I-=2C2++I2,I2+2S2O32-=2I-+S4O62-,经多次滴定消耗Na2S2O3标准液的体积平均值为33.00mL。则产品中钴的含量为 (结果保留三位有效数字)。实验过程中,下列操作会导致所测钴含量数值偏高的是 。
a.用天平称量产品时,产品与砝码的位置放颠倒
b.盛装Na2S2O3标准液的碱式滴定管未润洗
c.滴定前滴定管内无气泡,滴定结束后发现滴定管内有气泡
d.滴定管读数时,开始时俯视刻度线,结束时平视刻度线
高三化学答案
一、选择题(每题2分,共20分)
1.D 2.B 3.D 4.D 5.C 6.A 7.B 8.B 9.C 10.A
二、选择题(每题4分,共20分,全部选对得4分,对而不全得2分,有错选得0分)
11.A 12.B 13.CD 14.BC 15.CD
16. (12分)(除标明外,其他均为2分,下同)
(1)碳 钠 第三周期第ⅥA族(各1分)
(2)Al(OH)3 SO3 (各1分)
(3)AlC3H9+3H2O=3CH4↑+Al(OH)3↓ (4)2H2S+3O2=2SO2+2H2O
(5)NaCl+CO2+NH3+H2O =NH4Cl+NaHCO3↓
17.(12分)
(1)NH4+、Fe2+、Mg2+、SO42- 无(1分)
(2)0.3ml Fe(OH)3、0.1ml Mg(OH)2
(3)3Fe2++NO3-+4H+=2H2O+3Fe3++NO↑
(4)Ba2++CO2 +2OH-= BaCO3↓ + H2O
(5)4NH3+6NO 5N2+6H2O,2∶3 (1分)
18.(12分)
(1)防止Br2和HBr挥发(只答“挥发”或“一种物质挥发”得1分)
(2)SO32-+Br2 +H2O=2Br-+ SO42-+2H+
(3)直形冷凝管 (1分)
温度计水银球应与蒸馏烧瓶支管口相平(1分)不能用水浴加热(1分)
(4)含有Fe3+或Br2或两者混合物(1分)
(5)4 FeS2+11O2高温
2Fe2O3+8SO2 (6)
19.(12分)
(1)①⑦⑥②③④⑤(②③可颠倒) (2)石蜡油(1分)
(3)NaNO2+NH4ClNaCl+N2↑+2H2O
(4)向量气管中加水至左右出现液面差,静置,若液面差保持稳定,则装置气密性良好 倾斜Y形管,将蒸馏水全部注入a g产品中
(5)35(V1-V2) /22.4a×100% 偏高(1分)
20.(12分)
(1)6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O (2)Fe(OH)3、Al(OH)3
(3)蒸发浓缩、冷却结晶 (1分)
(4)防止加氨水时c(OH-) 过大产生C(OH)3沉淀(1分)
(5)H2O2+2CCl2+2NH4Cl+10NH3·H2O=2[C(NH3)6]Cl3↓+12H2O
(6)19.5%或0.195 bd序号
纯净物
混合物
非电解质
弱电解质
强电解质
A
盐酸
水煤气
HD
醋酸
硫酸
B
胆矾
漂白粉
NH3
HNO2
硫酸钡
C
火碱
蔗糖溶液
三氧化硫
氨水
碳酸氢钠
D
冰醋酸
福尔马林
乙醇
碘化氢
苛性钾
选项
X
Y
Z
W
A
C
CH4
CO
CO2
B
Fe
FeCl3
FeCl2
Fe(OH)2
C
Cl2
Ca(ClO)2
HClO
HCl
D
Cu
CuSO4
Cu(OH)2
CuO
选项
操作
现象
结论
A
将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液
溶液变红
Fe(NO3)2样品已变质
B
向Na2S溶液中滴加足量稀盐酸
有气泡生成
非金属性:Cl>S
C
向稀硫酸酸化的H2O2溶液中滴入FeCl2 溶液
溶液变黄色
氧化性:H2O2>Fe3+
D
溶有SO2的BaCl2溶液中通入气体X
有白色沉淀生成
X一定是 Cl2
选项
A
B
C
D
实验
装置
实验
目的
将干海带灼烧成灰
收集少量NO
用于铜丝与Cl2反应,防污染
提纯Al(OH)3胶体
2021威海高二上学期期末考试化学试题(可编辑)PDF版含答案: 这是一份2021威海高二上学期期末考试化学试题(可编辑)PDF版含答案
2020威海文登区高三下学期一轮总复习测试化学试题PDF版含答案: 这是一份2020威海文登区高三下学期一轮总复习测试化学试题PDF版含答案
2020威海荣成高三上学期期中考试化学试题含答案: 这是一份2020威海荣成高三上学期期中考试化学试题含答案












