

2020宁波咸祥中学高一下学期期中考试化学试题含答案
展开www.ks5u.com
2019学年 | 咸祥中学高一年级化学学科期中考试试卷 |
第二学期 |
命题人:王 磊 审核人:崔超亚
一、选择题(本题包括25小题,每小题只有1个选项符合题意,每小题2分,共50分)
- “绿水青山就是金山银山”。下列做法不利于保护环境的是
A.推广使用电动汽车等低碳交通工具
B.推广垃圾分类,电子设备以旧换新
C.用生物方法脱除生活污水中的氮和磷
D.加大铅酸蓄电池、含汞锌锰等电池的生产
2.下列化学用语表示正确的是
A.CH4分子的比例模型: B.CO2的电子式:
C.苯的分子式:C6H6 D.Cl-离子的结构示意图:
3.下列物质属于共价化合物的是
A. CCl4 B. Na2SO4 C. N2 D. NH4Cl
4.下列变化中,不属于化学变化的是
A.煤的气化 B.石油的裂解 C.煤的干馏 D.石油的分馏
5.下列有关性质的比较,不能用元素周期律解释的是
A.酸性:H2SO4 > H3PO4 B.热稳定性:Na2CO3 > NaHCO3
C.与水反应的速率:Na > Mg D.非金属性:Cl > Br
6.下列反应过程中的能量变化情况符合如图所示的是
A.2Al+Fe2O32Fe+Al2O3
B.C+H2OCO+H2
C.CH4+2O2 CO2+2H2O
D.HCl+NaOH NaOH+H2O
7.下列物质形成的晶体中,属于分子晶体的是
A.CCl4 B.NaOH C.金刚石 D.KCl
8.可逆反应A(g)+3B(g)C(g)+2D (g)在不同条件下的反应速率如下,其中反应速率最快的是
A.v(A)=0.2mol/(L•s) B.v(B)=0.6mol/(L•s)
C.v(C)=0.3mol/(L•s) D.v(D)=0.5mol/(L•s)
9.下列下列各组物质的性质比较中,不正确的是
A.离子半径:Br->Cl->F-
B.酸性强弱:HClO4>H2SO4>H3PO4
C.碱性强弱:KOH>NaOH>Mg(OH)2
D.氢化物的稳定性:NH3>PH3>H2S
10.下列变化中,需要克服分子间作用力是的
A.NaCl溶于水 B.干冰升华
C.加热碘化氢使之分解 D.加热硅晶体使之熔化
11.已知断开 1 mol Cl2(g)中 Cl-Cl键需要吸收243kJ能量,根据能量变化示意图,下列说法或热化学方程式正确的是
A.H2(g)+Cl2(g) = 2HCl(g) ΔH= + 185 kJ·mol-1
B.生成 1mol H2(g)中的 H-H键放出 121.5 kJ能量
C.断开 1mol HCl(g)中的 H-C1键要吸收864 kJ能量
D.HCl(g) = 1/2H2(g)+1/2Cl2(g) ΔH= + 92.5kJ·mol-1
12. 下列说法正确的是
①需要加热才能发生的反应一定是吸热反应
②放热反应在常温下一定很容易发生
③一个化学反应是放热反应还是吸热反应,决定于反应物和生成物所具有总能量的相对大小
④化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因
A.①④ B.①② C.②③ D.③④
13.下列说法中,正确的是
A.水和冰互为同素异形体 B.35Cl和37Cl互为同位素
C.白磷与红磷互为同位素 D.CH4和CH3CH3互为同分异构体
14.下列有关元素周期表的说法正确的是
A.元素周期表有7个周期,8个主族
B.零族原子的最外层电子数均为8
C.同一主族元素,最外层电子数一定相同
D.短周期是指第1、2、3、4周期
15.关于苯的结构和性质叙述中,不正确的是
A.苯能使酸性高锰酸钾溶液褪色 B.苯燃烧时能产生大量黑烟
C.苯难溶于水 D.常温下,苯不能与溴水发生反应
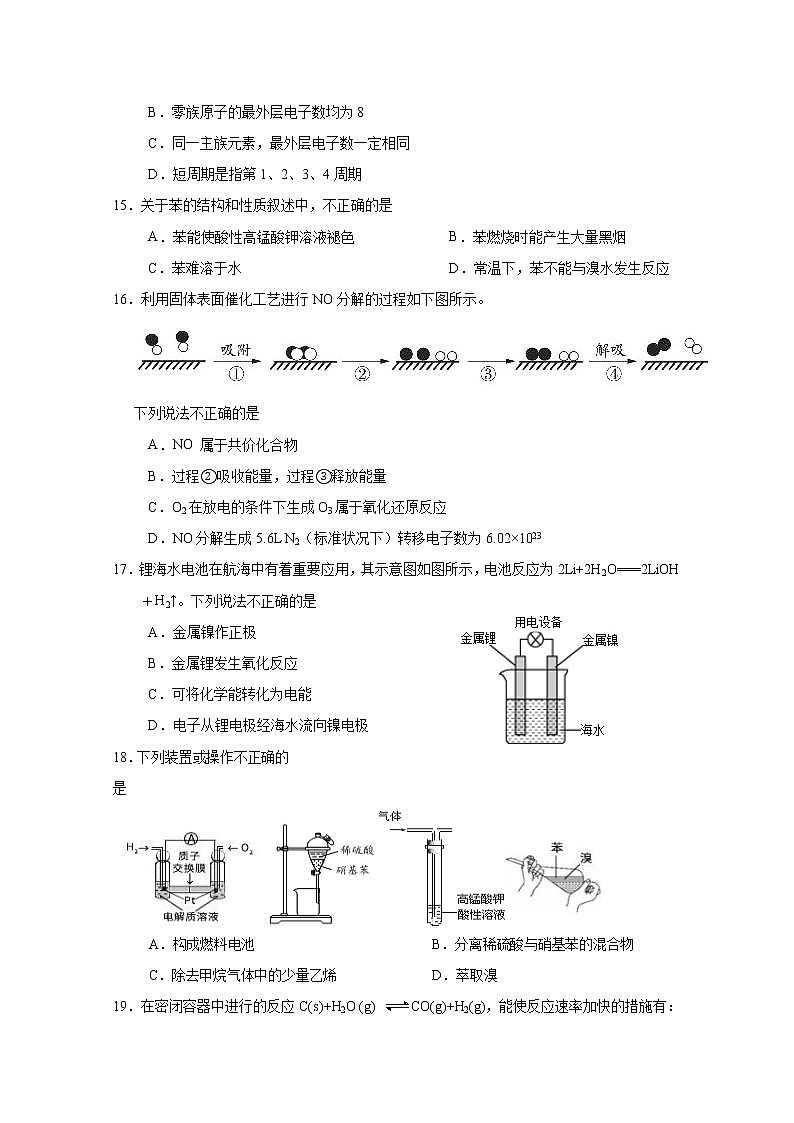
16.利用固体表面催化工艺进行NO分解的过程如下图所示。
下列说法不正确的是
A.NO 属于共价化合物
B.过程②吸收能量,过程③释放能量
C.O2在放电的条件下生成O3属于氧化还原反应
D.NO分解生成5.6L N2(标准状况下)转移电子数为6.02×1023
17.锂海水电池在航海中有着重要应用,其示意图如图所示,电池反应为2Li+2H2O===2LiOH+H2↑。下列说法不正确的是
A.金属镍作正极
B.金属锂发生氧化反应
C.可将化学能转化为电能
D.电子从锂电极经海水流向镍电极
18.下列装置或操作不正确的是
A.构成燃料电池 B.分离稀硫酸与硝基苯的混合物
C.除去甲烷气体中的少量乙烯 D.萃取溴
19.在密闭容器中进行的反应C(s)+H2O (g) CO(g)+H2(g),能使反应速率加快的措施有:①增加炭的量;②升高温度;③将炭粉碎;④恒容通入水蒸气;⑤通过减小容器体积增大压强;⑥恒容通入N2
A.②③④⑤ B.②③④⑤⑥ C.①②③④⑤ D.①②③④
20.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列说法正确的是
A.该反应的化学方程式为3X +Y2Z
B.3s时,正逆反应速率相等
C.平衡时X的浓度为0.40mol/L
D.10s时,该反应达到了最大限度
- 某两种气态烃组成的混合物,取其2.24L(标准状况下)充分燃烧,得到0.16mol二氧化碳气体和3.6g液态水。据此判断下列分析中不正确的是
A.此混合气体中可能含有乙烷
B.此气体中一定含有甲烷
C.此混合气体中一定不含有丙烷
D.此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2:3
22.短周期的X、Y、Z、W、R五种元素,原子序数依次增大。元素X的原子半径最小,Y、W同主族,W的最高正价是其最低负价绝对值的3倍,Z的二价阳离子与氖原子具有相同的核外电子排布。下列说法正确的是
A.X与Y形成的化合物只有一种
B.单质的氧化性:R>W
C.Y、Z形成的化合物为共价化合物
D.Z、W、R最高价氧化物对应的水化物相互之间可发生反应
23. 100mL浓度为2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
A. 加入适量的6 mol·L-1的盐酸 B. 加入数滴氯化铜溶液
C. 加入适量蒸馏水 D. 加入适量的氯化钠溶液
24. 铅蓄电池的两极分别为 Pb、PbO2,电解质溶液为30% H2SO4溶液,放电时的电池反应为Pb+PbO2+2H2SO4 == 2PbSO4+2H2O,下列说法正确的是
A. Pb 为正极,被氧化
B. 溶液的pH不断减小
C. SO42-向PbO2极移动
D. 溶液的pH不断增大
25. 下列说法正确的是
A.碘的升华和白磷的熔化所需破坏的微粒间作用力相同
B.在 Na2O、Na2O2、NaHSO4晶体中,阳离子与阴离子个数比均为 2∶1
C.1 mol SiO2 晶体与 1 mol CH4 晶体中共价键的个数比为 1∶2
D.NaOH 晶体溶于水,晶体中离子键和共价键被破坏,并与水分子形成水合钠离子等
二、非选择题(共40分)
26.(10分)下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① |
|
|
|
|
|
|
|
2 |
|
|
| ② | ③ | ④ | ⑤ |
|
3 | ⑥ |
| ⑦ | ⑧ |
| ⑨ |
| ⑩ |
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为_________________,
形成的单质是半导体的是 (填元素名称)。
(2)⑥与⑨形成的化合物的电子式为 ,①与②形成的最简单化合物的结构
式为 。
(3)最高价氧化物对应的水化物中,碱性最强的是 (填化学式,下同),呈两性的是 。
(4)气态氢化物最稳定的是 (填化学式),②、③、⑧的原子半径最小是
_________(填素符号)。
(5)④与⑧形成的化合物的属于 (填“离子化合物”或“共价化合物”),该晶体属于 晶体(填“离子”、“分子”、“原子”)。
27.(10分)某化学兴趣小组为了探究原电池产生电流的过程,设计了如图所示实验:
(1)下列叙述中正确的是________。
A.打开开关K时铜片作负极,关闭开关K时铜片作正极
B.打开开关K,锌片和铜片上均有气泡产生
C.关闭开关K后,溶液中的H+浓度减小
D.关闭开关K产生气泡的速率比打开开关K时慢
(2)打开开关K后,装置中发生反应的离子方程式为______________________________。
(3)关闭开关K后,则该装置为 (填“原电池”或“电解池”),铜极上的电极反应式为__________________。若反应过程中有0.3mol的电子发生转移,则产生的气体在标准状况下的体积为____L。
28.(12分)乙烯的产量通常用来衡量一个国家的石油化工水平,某化学实验小组为了探究石蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如下实验方案:
(查阅资料可知:乙烯与酸性高锰酸钾溶液反应产生二氧化碳。)
(1)乙烯的结构式是_____________________.
(2)B中实验现象:_________________________________________________________。
(3)C中发生反应的化学方程式:______________________________________________,
反应类型:_____________________。
(4)通过上述实验探究可知,除去乙烷中混有的乙烯,可以选择的试剂是____________
A.水 B.溴水
C.氢氧化钠溶液 D.酸性高锰酸钾溶液
(5)关于乙烯,下列说法中不正确的是__________
A.聚乙烯塑料可以用做食品包装袋
B.乙烯在一定条件下可以和水反应制乙醇
C.乙烯分子中所有原子不共面
D.乙烯是一种植物生长调节剂,可以延长果实和花朵的成熟期
29.(8分) 炼制石油能得到许多有机化合物,相关物质的转化关系如下图所示,其中A的产量是衡量一个国家石油化工发展水平的重要标志,标况下,B气体的密度为0.71g•L-1,C是一种红色固体单质,D是一种混合气体。
请回答:
(1)A的结构简式为______,A与溴的四氯化碳溶液的反应类型为 。
(2)B与CuO反应的化学方程式 。
(3)下列说法不正确是______。
a.A中所有原子共平面
b.A与溴的四氯化碳溶液反应现象,和A与溴水反应的现象完全相同
c.等物质的量A与B混合物在足量氧气中完全燃烧,生成水的物质的量相等
d.B是引起温室效应的气体之一
浙江省宁波市咸祥中学高二下学期期中考试化学试题: 这是一份浙江省宁波市咸祥中学高二下学期期中考试化学试题,文件包含精品解析浙江省宁波市咸祥中学高二下学期期中考试化学试题解析版docx、精品解析浙江省宁波市咸祥中学高二下学期期中考试化学试题原卷版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
2022宁波咸祥中学高一下学期期末考试化学含答案: 这是一份2022宁波咸祥中学高一下学期期末考试化学含答案,文件包含化学试题docx、化学答案docx等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。
2022宁波咸祥中学高一下学期期末考试化学含解析: 这是一份2022宁波咸祥中学高一下学期期末考试化学含解析,文件包含浙江省宁波市咸祥中学2021-2022学年高一下学期期末考试化学试题含解析docx、浙江省宁波市咸祥中学2021-2022学年高一下学期期末考试化学试题无答案docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。












