















高中化学人教版 (2019)选择性必修1第二节 化学平衡习题ppt课件
展开
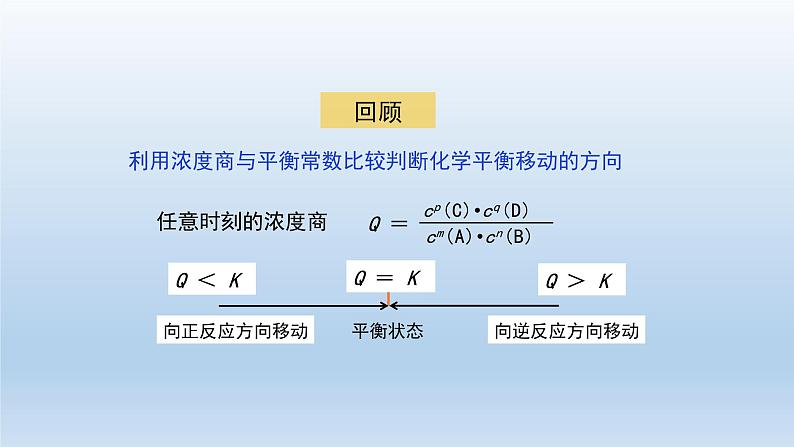
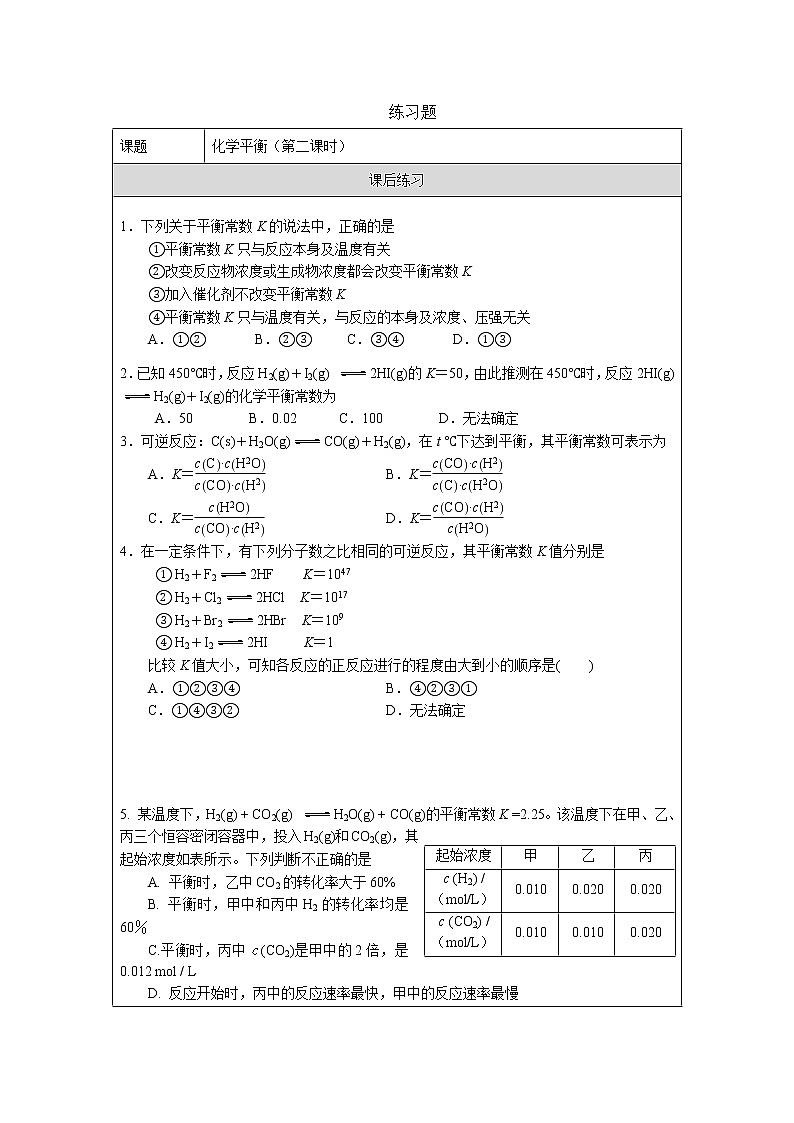
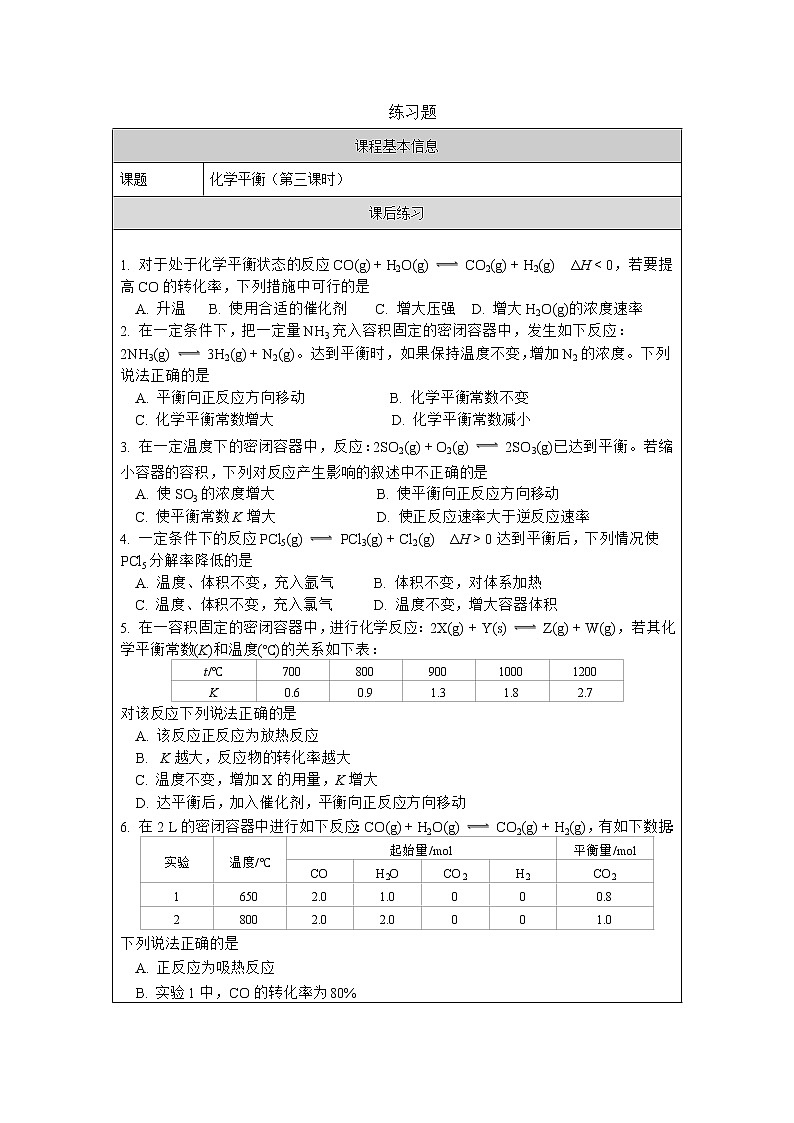
这是一份高中化学人教版 (2019)选择性必修1第二节 化学平衡习题ppt课件,文件包含高二化学人教版化学平衡第二课时-课件pptx、高二化学人教版化学平衡第三课时-课件pptx、高二化学人教版化学平衡第一课时-课件pptx、化学平衡第一课时-练习题docx、化学平衡第三课时-练习题docx、化学平衡第二课时-练习题docx等6份课件配套教学资源,其中PPT共132页, 欢迎下载使用。
练习题课题化学平衡(第一课时)课后练习1.下列关于化学反应限度的说法中正确的是A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度B.当一个可逆反应达到平衡状态时,正反应速率和逆反应速率相等都等于0C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变D.化学反应的限度不可以通过改变条件而改变2.在一密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是A.SO2为0.4 mol·L-1,O2为0.2 mol·L-1 B.SO2为0.25 mol·L-1C.SO2、SO3均为0.15 mol·L-1 D.SO3为0.4 mol·L-13.一定条件下的密闭容器中,起始时投入一定量的SO2(g) 和O2(g),发生反应:2SO2(g) +O2(g) 2SO3(g)。t min达到平衡。下列说法不正确的是A.若投入2 mol SO2与 1 mol O2,则生成2 mol SO3B.若用18O2进行反应,则一段时间后,18O在反应物和生成物中均存在C.t min前,该反应的正反应速率大于逆反应速率D.平衡时反应物与生成物浓度均不再变化4.下列各关系中能说明反应N2+3H2 2NH3已达到平衡状态的是A.3υ正(N2)=υ正(H2) B.υ正(N2)=υ逆(NH3)C.2υ正(H2)=3υ逆(NH3) D.υ正(N2)=3υ逆(H2)5.可逆反应:2NO2(g) 2NO(g)+O2(g)在容积固定的密闭容器中进行,达到平衡状态的标志的是____________。①单位时间内生成a mol O2的同时生成2a mol NO2②单位时间内生成a mol O2的同时生成2a mol NO③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态6.在某一容积为5 L的密闭容器内,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下加热至高温,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH>0。反应中CO2的浓度随时间变化情况如图:(1)根据上图数据,反应开始至达到平衡时,CO的化学反应速率为________;反应达到平衡时,c(H2)=________,CO的转化率为________。(2)判断该反应达到平衡的依据是________(填序号)。①CO减少的化学反应速率和CO2减少的化学反应速率相等②CO、H2O、CO2、H2的浓度都相等③CO、H2O、CO2、H2的浓度都不再发生变化④正、逆反应速率都为零(3)写出该反应的化学平衡常数表达式____________________________。 【课后作业参考答案】1.A 2.B 3.A 4.C 5.①④⑥⑦6.(1)0.003 mol·L-1·min-1 0.03 mol·L-1 75% (2)①③ (3)
相关课件
这是一份高中化学人教版 (2019)选择性必修1第一节 化学反应速率多媒体教学课件ppt,共27页。PPT课件主要包含了普通分子,活化能,活化分子,合理取向的碰撞,有效碰撞,一个反应经历的过程,产生气体慢,产生气体快,变浑浊快,变浑浊慢等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1实验活动1 探究影响化学平衡移动的因素课堂教学课件ppt,文件包含第二章化学反应速率与化学平衡_实验活动1探究影响化学平衡移动的因素-课件ppt、第二章化学反应速率与化学平衡_实验活动1探究影响化学平衡移动的因素-教案docx等2份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
这是一份人教版 (2019)选择性必修1第二节 化学平衡图文课件ppt,共32页。PPT课件主要包含了内容索引,自主预习新知导学,合作探究释疑解惑,课堂小结,课标定位素养阐释,问题引领,归纳提升,典型例题等内容,欢迎下载使用。










