





所属成套资源:全套中考物理复习题型教学课件
- 中考物理复习题型五浮力专题课件 课件 0 次下载
- 中考物理复习题型六代数思维课件 课件 0 次下载
- 中考物理复习题型八物理计算课件 课件 0 次下载
- 中考物理复习题型九生物探究课件 课件 0 次下载
- 中考物理复习题型十健康生活课件 课件 0 次下载
中考物理复习题型七化学计算课件
展开
这是一份中考物理复习题型七化学计算课件,共29页。PPT课件主要包含了例题演练,拓展提升,HCl,m1-m2g,无气泡再产生,CO中混有的CO2,H2SO4等内容,欢迎下载使用。
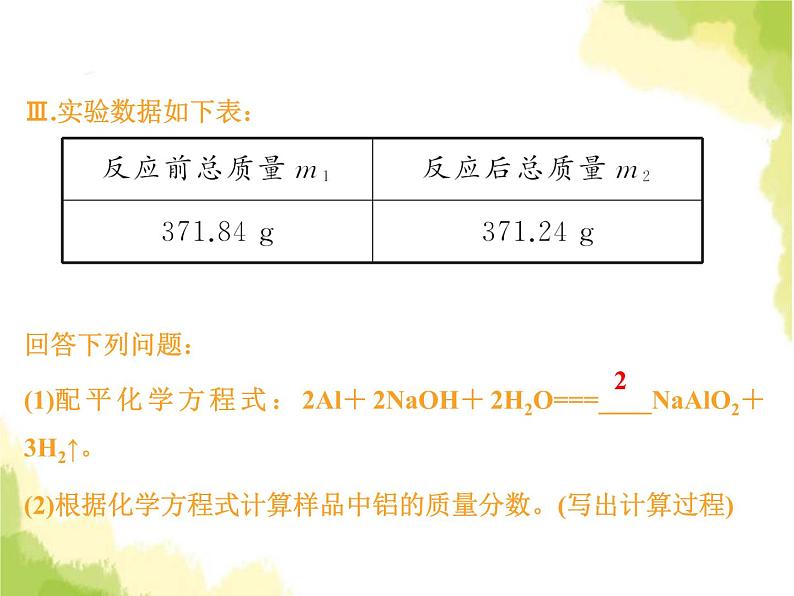
例 有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等淤积物的腐蚀,同时产生氢气增加管道内的气压,利于疏通。小柯利用如图装置测定疏通剂中铝的质量分数。Ⅰ.取样品20 g,倒入容积为200 mL的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:回答下列问题:(1)配平化学方程式:2Al+2NaOH+2H2O===____NaAlO2+3H2↑。(2)根据化学方程式计算样品中铝的质量分数。(写出计算过程)
(3)以下情形会导致样品中铝的质量分数测量结果偏高的原因可能有__________。A.向锥形瓶中倒入样品时,撒出了部分粉末B.在反应过程中有水蒸气逸出C.没有等装置中氢气全部排尽就称量
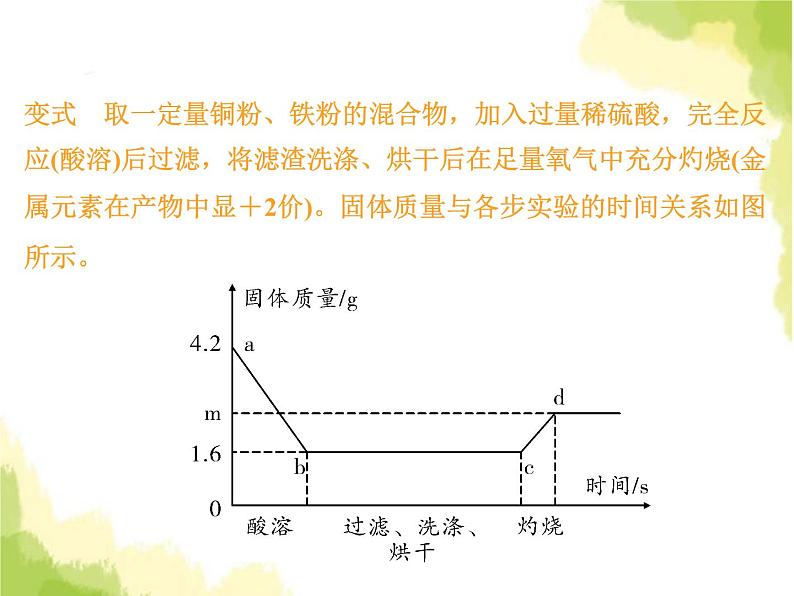
变式 取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗涤、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图所示。
(1)b点时溶液中溶质的化学式为__________________。(2)原粉状混合物中铁粉的质量为______g。(3)求m的值。(写出计算过程)
FeSO4、H2SO4
1.用500吨含Fe2O3 80%的赤铁矿在高炉内可炼出含杂质3%的生铁__________吨。2.有0.4 g某种铁的氧化物,用足量的CO在高温条件下将其还原,把生成的CO2全部通入到足量澄清石灰水中,得到沉淀0.75 g。请回答:(1)生成CO2的质量为_______g。(2)通过计算确定这种铁的氧化物的化学式。
3.在一烧杯中盛有22.3克碳酸钠和氯化钠组成的固体混合物,向其中逐渐滴加稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答问题:(1)当滴加了73克稀盐酸时,放出气体的总质量为_______克。(2)当滴加稀盐酸至图中的B点时,烧杯中溶液里的溶质是:_____________(写化学式)。
(3)当滴加了73克稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出此时所得溶液的溶质的质量分数。
4.小金欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品5 g,把60 g稀盐酸分四次加入,实验过程所得数据如表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。根据实验数据计算:(1)表中x=________。(2)第____次加入稀盐酸时,碳酸钙已经反应完全。
(3)求原60 g稀盐酸中溶质质量分数。(写出计算过程,计算结果精确到0.1%)
5.现有含杂质的氧化铁样品(杂质不参加反应),为了测定该样品中氧化铁的质量分数,某同学称取样品10克,并用下图所示装置进行实验,得到以下两组实验数据。
你认为,应当选择____组实验数据来计算样品中氧化铁的质量分数。实验计算的结果为多少?(写出计算过程)
6.为了验证某碳酸钙样品质量分数为98%(样品中杂质不反应),小组同学设计了如下方案:(1)方案1:取m1 g样品于试管中,用酒精喷灯加热,完全反应。再次称量剩余固体质量为m2 g,可以得出CO2的质量为_______________。(2)方案2:①取m1 g样品,称量装有样品的烧杯和装有足量稀盐酸的烧杯共计m2 g。②将稀盐酸倒入样品中,搅拌,当看到烧杯中_______________时,称量两个烧杯总质量共计m3 g,计算样品中碳酸钙质量分数的公式是________________________。
(3)方案3:取m1 g样品,加入足量的稀盐酸,使生成的气体全部通入足量的石灰水中,将生成的沉淀过滤、烘干,称量其质量为m2 g,计算样品中碳酸钙质量分数的公式是______________。【结论和反思】以上几种方案都能测得样品的纯度。但从实验结果看,方案2测得的结果却超过了100%,原因可能是_____________________________________________________。
反应过程中水蒸气(或氯化氢)溢出,使测定结果偏大
(1)下列仪器从左向右组装连接的顺序是____→b→____→____→____→____→____→____。(用a,b…表示)(2)装置乙的作用是除去_______________________。(3)实验结束后,先熄灭_____处的酒精灯,再熄灭_____处的酒精灯,其主要原因是____________________________________。(4)实验前氧化铁矿粉末的质量为a克,实验后测得乙和丙的质量分别增加了y克和z克,则氧化铁矿粉末中氧化铁的质量分数为多少?
使生成的Fe在CO气流中冷却,防止倒吸
8.某科学小组利用如图装置对FeSO4·nH2O晶体中的结晶水的含量进行测定(铁架台等已省略)。已知:①FeSO4和FeSO4·nH2O加热时易被空气氧化;②FeSO4·nH2OFeSO4+nH2O。实验步骤如下:
请回答:(1)步骤Ⅰ打开K1导入二氧化碳气体,排尽装置中的空气,其目的是__________________________________________________。(2)步骤Ⅳ中的操作乙是通二氧化碳直至C装置冷却至室温,则操作甲指的是_______________________________________。(3)有同学建议,为加快产生CO2的速率,可将A中装置中盐酸浓度增大、石灰石磨成粉状。试问,制取气体时反应速度是否越快越好?其理由是_____________________________________________________________________________________________。
防止空气中的氧气氧化FeSO4和FeSO4·nH2O
加热至晶体质量不再变化
不是,反应速度过快易造成安全事故,也不利于气体的收集
(4)步骤Ⅵ称量,若晶体FeSO4·nH2O质量为m,反应前后C装置质量减少了m1,D装置质量增加了m2,则此晶体中的结晶水的百分含量为_________(用字母表示),n的数值是____________。(用字母表示)
9.图甲中A是一种常见的酸,它能与黑色固体B反应,B的质量为8 g。将NaOH溶液渐渐加到C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2,能生成一种不溶于稀硝酸的白色沉淀。
(1)A溶液中溶质的化学式为__________。(2)操作Ⅰ的名称是_________。(3)NaOH溶液中溶质的质量分数是多少?
相关课件
这是一份中考物理复习题型五计算题练习课件,共60页。
这是一份中考物理复习题型六计算题作业课件,共60页。
这是一份人教版中考物理复习题型七计算应用题作业课件,共60页。









