
湖北省咸丰春晖学校2022-2023学年高三上学期10月月考化学试题
展开
这是一份湖北省咸丰春晖学校2022-2023学年高三上学期10月月考化学试题,共6页。试卷主要包含了下列有关说法错误的是,下列实验操作正确的是,设NA为阿伏加德罗常数的值,某化学反应X+Y→Z分两步进行等内容,欢迎下载使用。
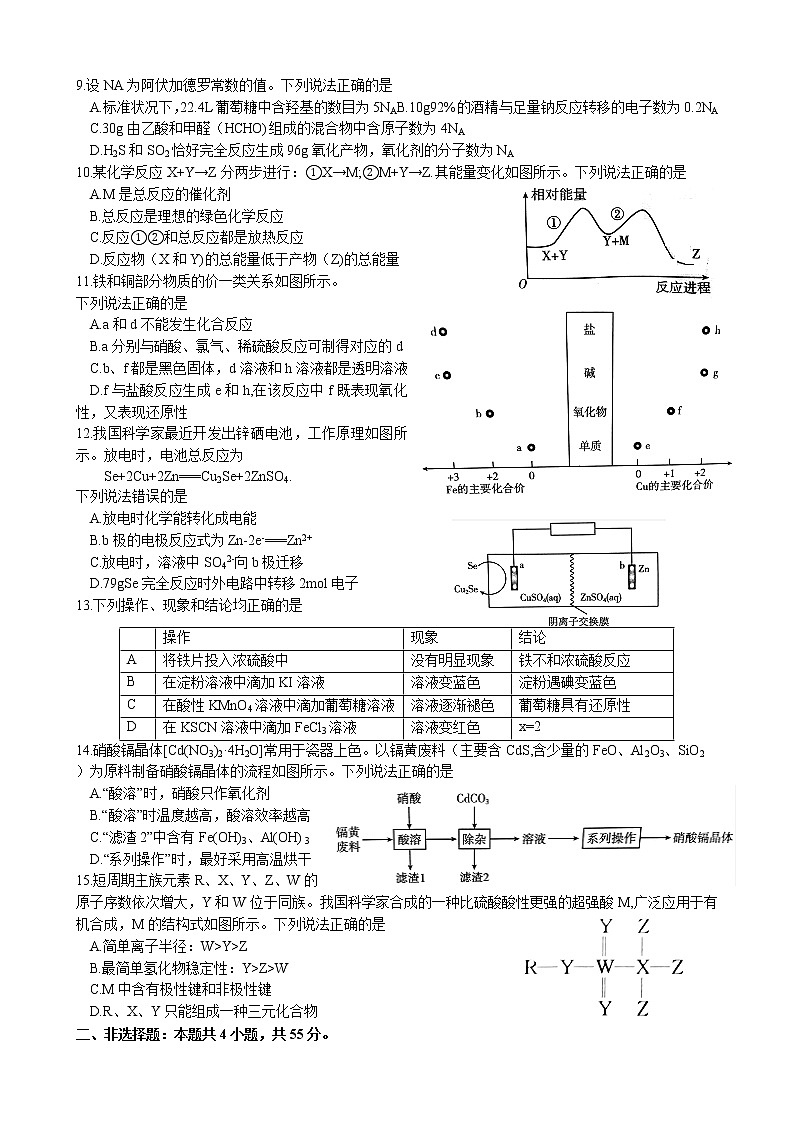
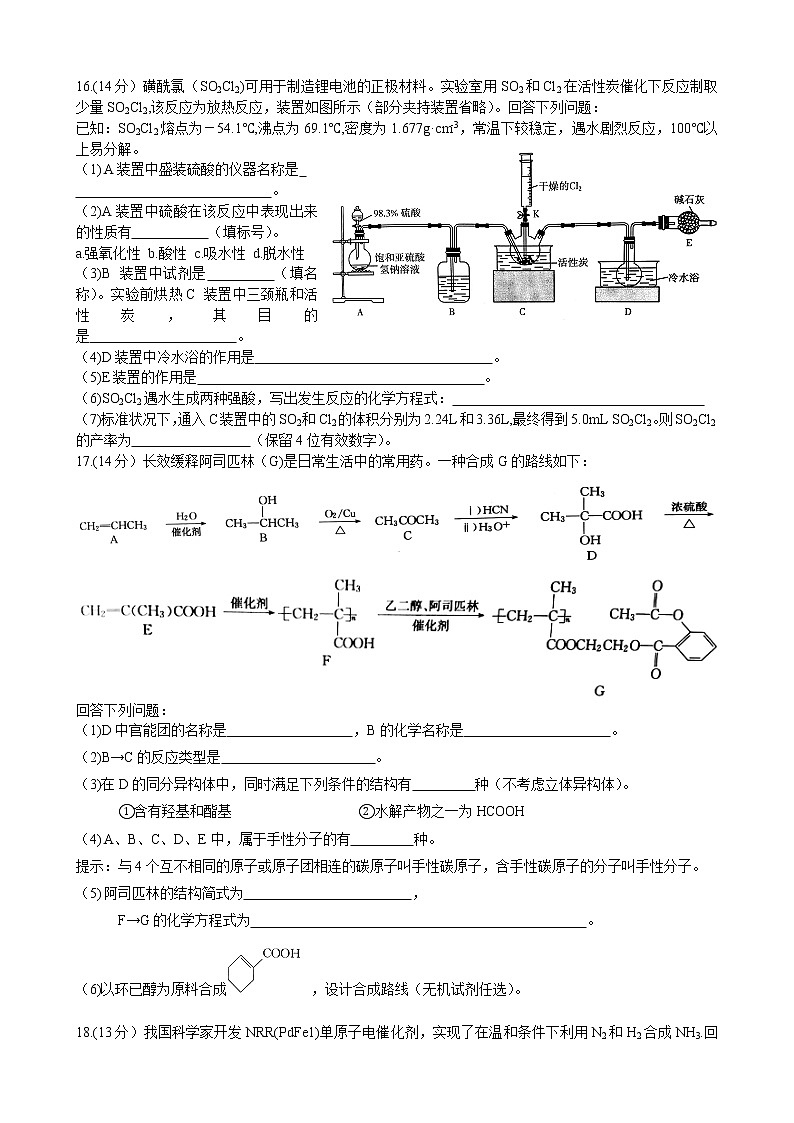
2022高三10月联考化学考试 10.9下午本试卷主要考试内容:人教版必修第一册、必修第二册。.可能用到的相对原子质量:H1 C 12 O16 S 32 C1 35.5 Mn 55 Se 79一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。1.下列有关说法错误的是A.金刚砂常作砂纸和砂轮的磨料 B.高纯度硅是制造光伏电池板的主要材料C.生产普通玻璃和水泥的原料都是石英砂 D.我国古代烧制的精美瓷器,其主要成分是硅酸盐2.我国科学家在铜电催化剂上锚定离子液体,提高了CO2转化为C2H4的效率。化学反应原理是2CO2(g)+6H2(g)→C2H4(g)+4H2O(g),,下列说法正确的是A、CO2的结构式为 B.中子数为36的铜原子表示为3629CuC.C2H4的分子式为 D.H2O的空间填充模型为3.粘康酸常用作抗紫外线的防护剂及航天隐形飞机的涂层材料,它的结构简式如图所示。下列说法错误的是A.粘康酸的分子式为C6H8O4B.粘康酸能与H2发生加成反应C.粘康酸中只含有2种官能团 D.1 mol粘康酸与足量NaHCO3溶液反应生成88gCO24.铁粉与稀硝酸反应的化学方程式为8Fe+30HNO3===8Fe(NO3)3+3NH4NO3+9H2O.下列有关说法正确的是A.氧化性:HNO3<Fe3+ B.作氧化剂的HNO3是参与反应的HNO3的10%C.若铁粉过量,则氧化剂与还原剂的物质的量之比为3:8D.在反应后的混合物中滴加少量氢氧化钠溶液,有气体逸出5.在我国古代,春节的民间习俗有祭灶、扫尘、吃灶糖等。下列说法错误的是A.“祭灶”时燃放鞭炮,会产生一种大气污染物CO2 B.“祭灶”时烧纸钱,纸钱的主要成分是纤维素C.“扫尘”时阳光照射空气,会产生丁达尔效应D.“灶糖”的主要成分是蔗糖,一定条件下蔗糖能水解生成葡萄糖和果糖6.下列各组离子在指定溶液中能大量共存的是A.NaI溶液中:A l3+、Fe3+、NO3-、C1- B.能使酚酞变红的溶液中:K+、Na+、S2O32-、CO32-C.稀H2SO4中:Mg2+、Na+、NO3-、CH3COO-D.常温下由水电离的c(H+)·c(OH-)=1×10-26的溶液中:Ba2+、Na+、HCO3-、Cl-7.工业上制备粗硅发生的反应之一是SiO2(s)+C(s)SiO(s)+CO(g)。在一定温度下,向某恒容密闭容器中加入足量的SiO2和炭粉,仅发生上述反应。下列说法正确的是A.SiO2、SiO和CO均属于酸性氧化物 B.当n(SiO)=n(CO)时,该反应达到平衡C.平衡后再加入SiO2,平衡正向移动 D.当CO的质量不再改变时,该反应达到平衡8.下列实验操作正确的是 9.设NA为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,22.4L葡萄糖中含羟基的数目为5NAB.10g92%的酒精与足量钠反应转移的电子数为0.2NAC.30g由乙酸和甲醛(HCHO)组成的混合物中含原子数为4NAD.H2S和SO2恰好完全反应生成96g氧化产物,氧化剂的分子数为NA10.某化学反应X+Y→Z分两步进行:①X→M;②M+Y→Z.其能量变化如图所示。下列说法正确的是A.M是总反应的催化剂B.总反应是理想的绿色化学反应C.反应①②和总反应都是放热反应D.反应物(X和Y)的总能量低于产物(Z)的总能量11.铁和铜部分物质的价一类关系如图所示。下列说法正确的是A.a和d不能发生化合反应B.a分别与硝酸、氯气、稀硫酸反应可制得对应的dC.b、f都是黑色固体,d溶液和h溶液都是透明溶液D.f与盐酸反应生成e和h,在该反应中f既表现氧化性,又表现还原性12.我国科学家最近开发出锌硒电池,工作原理如图所示。放电时,电池总反应为Se+2Cu+2Zn===Cu2Se+2ZnSO4.下列说法错误的是A.放电时化学能转化成电能B.b极的电极反应式为Zn-2e-===Zn2+C.放电时,溶液中SO42-向b极迁移D.79gSe完全反应时外电路中转移2mol电子13.下列操作、现象和结论均正确的是 操作现象结论A将铁片投入浓硫酸中没有明显现象铁不和浓硫酸反应B在淀粉溶液中滴加KI溶液溶液变蓝色淀粉遇碘变蓝色C在酸性KMnO4溶液中滴加葡萄糖溶液溶液逐渐褪色葡萄糖具有还原性D在KSCN溶液中滴加FeCl3溶液溶液变红色x=214.硝酸镉晶体[Cd(NO3)2·4H2O]常用于瓷器上色。以镉黄废料(主要含CdS,含少量的FeO、Al2O3、SiO2)为原料制备硝酸镉晶体的流程如图所示。下列说法正确的是A.“酸溶”时,硝酸只作氧化剂B.“酸溶”时温度越高,酸溶效率越高C.“滤渣2”中含有Fe(OH)3、Al(OH)3D.“系列操作”时,最好采用高温烘干15.短周期主族元素R、X、Y、Z、W的原子序数依次增大,Y和W位于同族。我国科学家合成的一种比硫酸酸性更强的超强酸M,广泛应用于有机合成,M的结构式如图所示。下列说法正确的是A.简单离子半径:W>Y>ZB.最简单氢化物稳定性:Y>Z>WC.M中含有极性键和非极性键D.R、X、Y只能组成一种三元化合物二、非选择题:本题共4小题,共55分。16.(14分)磺酰氯(SO2Cl2)可用于制造锂电池的正极材料。实验室用SO2和Cl2在活性炭催化下反应制取少量SO2Cl2,该反应为放热反应,装置如图所示(部分夹持装置省略)。回答下列问题:已知:SO2Cl2熔点为-54.1℃,沸点为69.1℃,密度为1.677g·cm-3,常温下较稳定,遇水剧烈反应,100℃以上易分解。(1) A装置中盛装硫酸的仪器名称是 。(2)A装置中硫酸在该反应中表现出来的性质有 (填标号)。a.强氧化性 b.酸性 c.吸水性 d.脱水性(3)B装置中试剂是 (填名称)。实验前烘热C装置中三颈瓶和活性炭,其目的是 。(4)D装置中冷水浴的作用是 。(5)E装置的作用是 。(6)SO2Cl2遇水生成两种强酸,写出发生反应的化学方程式: (7)标准状况下,通入C装置中的SO2和Cl2的体积分别为2.24L和3.36L,最终得到5.0mL SO2Cl2。则SO2Cl2的产率为 (保留4位有效数字)。17.(14分)长效缓释阿司匹林(G)是日常生活中的常用药。一种合成G的路线如下:回答下列问题:(1)D中官能团的名称是 ,B的化学名称是 。(2)B→C的反应类型是 。(3)在D的同分异构体中,同时满足下列条件的结构有 种(不考虑立体异构体)。①含有羟基和酯基 ②水解产物之一为HCOOH(4) A、B、C、D、E中,属于手性分子的有 种。提示:与4个互不相同的原子或原子团相连的碳原子叫手性碳原子,含手性碳原子的分子叫手性分子。(5) 阿司匹林的结构简式为 ,F→G的化学方程式为 。(6)以环已醇为原料合成 ,设计合成路线(无机试剂任选)。 18.(13分)我国科学家开发NRR(PdFe1)单原子电催化剂,实现了在温和条件下利用N2和H2合成NH3.回答下列问题:(1)工业合成氨的化学方程式为 。已知:1 mol N2(g)和3molH2(g)总能量大于2molNH3(g)总能量,则工业合成氨的反应是 (填“放热”或“吸热”)反应。2)其他条件相同,在Cat1、Cat2、Cat3三种催化剂作用下,测得反应速率增大倍数与温度关系如图所示。实际生产中,宜选择的催化剂是(填“Cat1”、“Cat2”或“Cat3”),如果Cat1、Cat3是同一种催化剂,T3时反应速率增大倍数小于T1时的可能原因是 。(3)一定温度下,在1L恒容密闭容器中充入1molN2和3mol H2,测得NH3的物质的量(n)与时间(t)关系如表所示:时间/min0510152025物质的量/mol00.300.500.650.700.70①0~10min内,H2的平均反应速率v(H2)= mol·L-1·min-1.②15min时,N2的正反应速率 (填“大于”、“小于”或“等于”)N2的逆反应速率。③在上述条件下,N2的平衡转化率为 (4)氨气碱性(KOH溶液)燃料电池能量转化率较高,电池反应为4NH3+3O2===2N2+6H2O,电池放电时,负极的电极反应式为 。19.(14分)硫酸锰晶体(MnSO4·H2O)常用作动物饲料的添加剂。工业上以软锰矿(含MnO2和少量的Fe3O4、Al2O3、SiO2)为原料制备硫酸锰晶体的流程如下:已知几种金属离子沉淀的pH如表所示:金属氢氧化物Fe(OH)3Fe(OH)2Al(OH)3Mn(OH)2开始沉淀的pH2.77.64.07.7完全沉淀的pH3.79.65.29.8回答下列问题:(1)“酸浸”前需要将软锰矿粉碎,粉碎的目的是 ,“酸浸”中MnO2和FeSO4反应的离子方程式为 。(2)“滤渣1”的主要成分是 (填化学式)。“系列操作”包括 、降温结晶、过滤、洗涤、干燥等。(3)“过滤”时,用到的玻璃仪器有 。(4)从绿色化学角度分析,试剂A宜选择 (填标号)。a.HNO3 b.H2O2 c.Cl2 d.O3(5)如果省略“氧化”工艺,产品中可能会混有 (填化学式)。(6)测定产品纯度:准确称取wg样品,加适量ZnO及H2O煮沸、冷却后,转移至锥形瓶中,用c mol·L-1KMnO4标准溶液滴定至溶液呈红色且半分钟不褪色,消耗KMnO4标准溶液VmL。MnSO4·H2O样品的纯度为 (用含w、c、V的代数式表示)。已知:①2KMnO4+3MnSO4+2H2O===5MnO2↓+K2SO4+2H2SO4②杂质不与KMnO4反应。2022金太阳高三10月联考化学考试化学试题参考答案一、选择题:本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求题号123456789101112131415答案CDABABDBCBDDCCA二、非选择题(共4题,共55分)16.(1)分液漏斗(1分)(2)bc(2分)(3)浓硫酸(1分);除去三颈瓶内水蒸气,避免水蒸气与产品反应(或其他合理答案,2分)(4)冷却SO2Cl2,减少损失(2分)(5)吸收尾气中SO2和Cl2,防止空气中的水蒸气进入装置D(2分)(6)SO2Cl2+2H2O ===H2SO4+2HC1(2分(7)61.85%(2分)17.(1)羧基、羟基(2分);2-丙醇(或异丙醇)(1分)(2)氧化反应(1分)(3)5(2分)(4)0(1分)(1)N2+3H22NH3(2分);放热(1分)(2) Cat2(1分);温度过高,催化剂活性降低(或温度过高,催化剂选择性降低等)(2分)(3) ①0.075(2分)②大于(1分)③35%(2分)(4)2NH3+6OH--6e-===N2+6H2O(2分)19.(1)增大接触面积,加快反应速率(2分);MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O(2分)(2)SiO2(1分);蒸发浓缩(1分)(3)烧杯、玻璃棒、漏斗(答对1个或2个均给1分,2分)(4)bd(2分)(5)FeSO4·7H2O或其他合理答案,2分)(6)
相关试卷
这是一份湖北省春晖教育集团2023-2024学年高一上学期12月月考化学试题含答案,共17页。试卷主要包含了5 Cu 64等内容,欢迎下载使用。
这是一份湖北省咸丰春晖学校2023-2024学年高一上学期12月月考化学试题,共12页。试卷主要包含了5 Cu 64等内容,欢迎下载使用。
这是一份湖北省咸丰春晖学校2023-2024学年高一上学期12月月考化学试题(Word版含解析),文件包含试题docx、答案pdf等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。









