

2023届四川省绵阳市高三第一次诊断性考试化学卷无答案(文字版)
展开
这是一份2023届四川省绵阳市高三第一次诊断性考试化学卷无答案(文字版),共6页。试卷主要包含了《后汉书·蔡伦传》中记载,为阿伏加德罗常数的值,【化学——选修3等内容,欢迎下载使用。
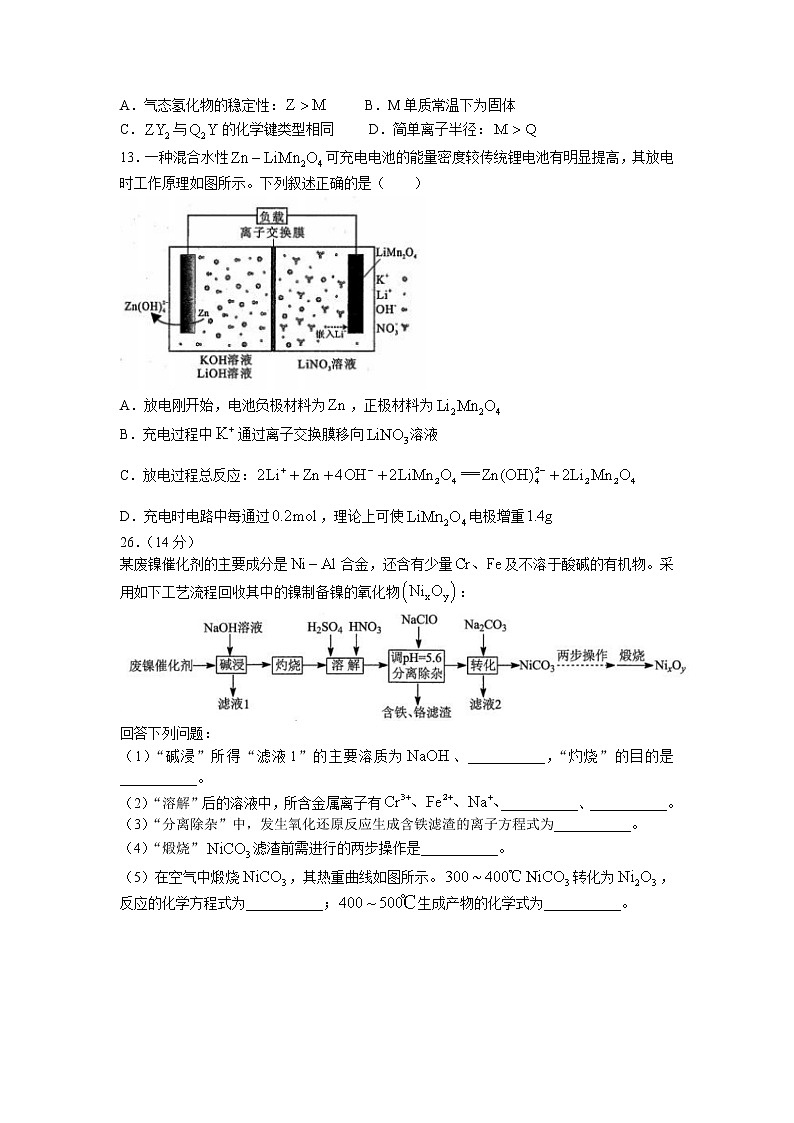
绵阳市高中2020级第一次诊断性考试化学试卷7.《后汉书·蔡伦传》中记载:“自古书契多编以竹简,其用缣帛者,谓之纸。缣贵而简重,不便于人,伦乃造意用树肤,麻头及弊布、渔网以为纸。”下列叙述错误的是( )A.“缣帛”是丝质品,其主要成分为蛋白质 B.“树肤”与“麻头”的主要成分属于糖类C.造纸过程中可以采用过氧化氢漂白纸浆 D.现代渔网的主要成分是尼龙,属于纤维素8.有机化合物性质多样,下列说法正确的是( )A.用饱和碳酸钠溶液可以鉴别乙醇和乙酸乙酯 B.甲苯能发生加成反应,但不能发生取代反应C.酸性条件下,植物油的水解产物所含官能团相同 D.环成烯()分子中所有碳原子共平面9.下列化学表达式正确,且与所给事实相符的是( )A.硫酸铜溶液中滴加稀氨水:B.中性环境中,钢铁电化学腐蚀的正极电极反应式:C.稀硝酸中加入过量铁粉:D.湿润的淀粉碘化钾试纸遇氯气变蓝:10.下列实验操作和实验现象不相匹配的是( ) 实验操作实验现象A将一小块钠投入硫酸铜溶液中有气泡冒出,产生蓝色沉淀B将加入适量水中,滴入几滴酚酞溶液先变红后褪色,有气泡产生C向重铬酸钾溶液中滴加几滴浓硫酸随着浓硫酸加入,溶液颜色变浅D将铜丝在盛满氯气的烧瓶中点燃烧瓶中充满棕黄色的烟A.A B.B C.C D.D11.为阿伏加德罗常数的值。下列说法正确的是( )A.与的混合物中所含中子数为B.标准状况下,丙烷具有的共价键数为C.电解精炼铜时,若电路中转移电子,阳极质量减少D.常温下,投入浓硫酸中,反应转移的电子数为12.X、Y、Z、M、Q为前20号主族元素,其原子序数依次增大。X的核外电子数等于其周期数,是最常用的溶剂,Z的最外层电子数是Y电子总数的一半,Q为前四周期金属性最强的元素。下列说法一定正确的是( )A.气态氢化物的稳定性: B.M单质常温下为固体C.与的化学键类型相同 D.简单离子半径:13.一种混合水性可充电电池的能量密度较传统锂电池有明显提高,其放电时工作原理如图所示。下列叙述正确的是( )A.放电刚开始,电池负极材料为,正极材料为B.充电过程中通过离子交换膜移向溶液C.放电过程总反应:D.充电时电路中每通过,理论上可使电极增重26.(14分)某废镍催化剂的主要成分是合金,还含有少量及不溶于酸碱的有机物。采用如下工艺流程回收其中的镍制备镍的氧化物:回答下列问题:(1)“碱浸”所得“滤液1”的主要溶质为、___________,“灼烧”的目的是___________。(2)“溶解”后的溶液中,所含金属离子有___________、___________。(3)“分离除杂”中,发生氧化还原反应生成含铁滤渣的离子方程式为___________。(4)“煅烧”滤渣前需进行的两步操作是___________。(5)在空气中煅烧,其热重曲线如图所示。转化为,反应的化学方程式为___________;生成产物的化学式为___________。(6)利用制得溶液,调节其至7.5~12,采用惰性电极进行电解,阳极上可沉淀出用作锌镍电池正极材料的。电解时阳极的电极反应式为___________。27.(15分)高锰酸钾具有强氧化性,广泛应用于化工、医药、金属冶炼等领域。实验室可通过固体碱溶氧化法制备高锰酸钾。回答下列问题:(1)称取和,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要___________(填仪器名称),不使用瓷坩埚的原因是___________。(2)将分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色。该步反应的化学方程式为___________,分多次加入的原因是___________。(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入,使歧化为与2。用玻璃棒蘸取溶液于滤纸上,观察到___________,表明转化已完全。静置片刻,抽滤。该步骤若用代替,可能的后果是___________。(4)水浴加热滤液至出现晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是___________。下表是部分化合物溶解度随温度变化的数据,步骤(3)中不宜通入过多,目的是___________,产品经纯化后称重,质量为。本实验中的产率为___________%。温度/2030405011011411712133.739.947.565.66.49.012.616.928.(14分)我国的能源以煤炭为主,燃煤烟气中等有害气体的排放会污染环境,用还原脱除将其转化为单质硫,对工业生产具有重要的意义。(1)已知常温常压下,的燃烧热为,的燃烧热为,则还原脱除:___________。(2)在某温度时,进行还原脱除:。①若在刚性容器中进行,下列说法一定能确定反应达到平衡状态的是___________。A. B.与的浓度之比不再改变C.容器内的压强不再改变 D.的值不再改变②若控制进料比(物质的量)为4∶1,反应达平衡时,混合气体中的体积分数为5%,则该反应在此温度下的平衡常数为___________.(3)在时,发生如下系列反应,测得不同进料比(物质的量)下平衡体系各物质分布如图所示(图中起始投料固定为)。反应Ⅰ:反应Ⅱ:反应Ⅲ:①该条件下,为减少有毒物质的产生,同时脱除,实际生产中应控制进料比为___________,在进料比大于2.5之后,的含量会明显增大,试分析原因___________。②根据图中曲线,可判断___________(填“>”“=”或“<”)。(4)—空气质子交换膜燃料电池也可用于处理,其原理如图。若用该电池处理标准状况下含量为20%的燃煤烟气,则理论上电路中转移电子数为___________。35.【化学——选修3:物质结构与性质】(15分)碳元素是形成化合物最多的元素,碳及其化合物构成了丰富多彩的物质世界。回答下列问题:(1)基态碳原子的电子占据的最高能级电子云形状为___________,与碳元素同主族的第四周期元素基态原子外围电子排布式为___________。(2)是常见的含碳化合物,其构成元素电负性从大到小的顺序为___________,该分子中具有孤对电子的原子是___________。(3)碳酸盐是构成岩石、土壤等的主要成分,其阴离子的立体构型为___________。已知碳酸镁的热分解温度()比碳酸钙()低,试解释原因___________。(4)在碳酸氢盐中,存在阴离子的多聚链状结构(其结构单元如图),连接结构单元的主要作用力是氢键,请在下图中前后各链接一个结构单元:该结构中,碳原子杂化方式为___________。(5)一种碳化钨的晶体结构如图,若晶胞的高为,阿伏加德罗常数值为,晶体的密度为,则晶胞底面六边形的边长为___________(列出计算式)。36.【化学——选修5:有机化学基础】(15分)活性亚甲基化合物和,不饱和羰基化合物发生缩合生成-羰烷类化回答下列问题:(1)芳香化合物A的化学名称是___________。(2)C中所含官能团的名称是___________。(3)F的结构简式为___________,由F生成G的反应类型是___________。(4)己知I的分子中:①含有三个六元环;②不含甲基;③含有两个羰基。I的结构简式为___________。(5)芳香化合物X是C的同分异构体,可发生银镜反应,分子中有五种不同化学环境的氢。写出两种符合上述条件的X的结构简式___________。(6)H分子中有___________个手性碳(碳原子上连有4个不同的原子或基团时,该碳称为手性碳)。如果要合成化合物()参照上述合成路线,写出相应的和的结构简式:___________、___________。
相关试卷
这是一份四川省绵阳市2023届高三下学期第三次诊断性考试(三模)化学答案,共3页。试卷主要包含了 A 8, [化学—选修3, [化学—选修5等内容,欢迎下载使用。
这是一份四川省绵阳市2023届高三下学期第三次诊断性考试(三模)化学答案,共3页。
这是一份四川省绵阳市2023届高三第二次诊断性考试化学试卷(含答案),共13页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。










