

山东省烟台市蓬莱区2022-2023学年九年级上学期期中化学试题(含答案)
展开
这是一份山东省烟台市蓬莱区2022-2023学年九年级上学期期中化学试题(含答案),共11页。试卷主要包含了选择题,填空与简答题,实验探究题,计算题等内容,欢迎下载使用。
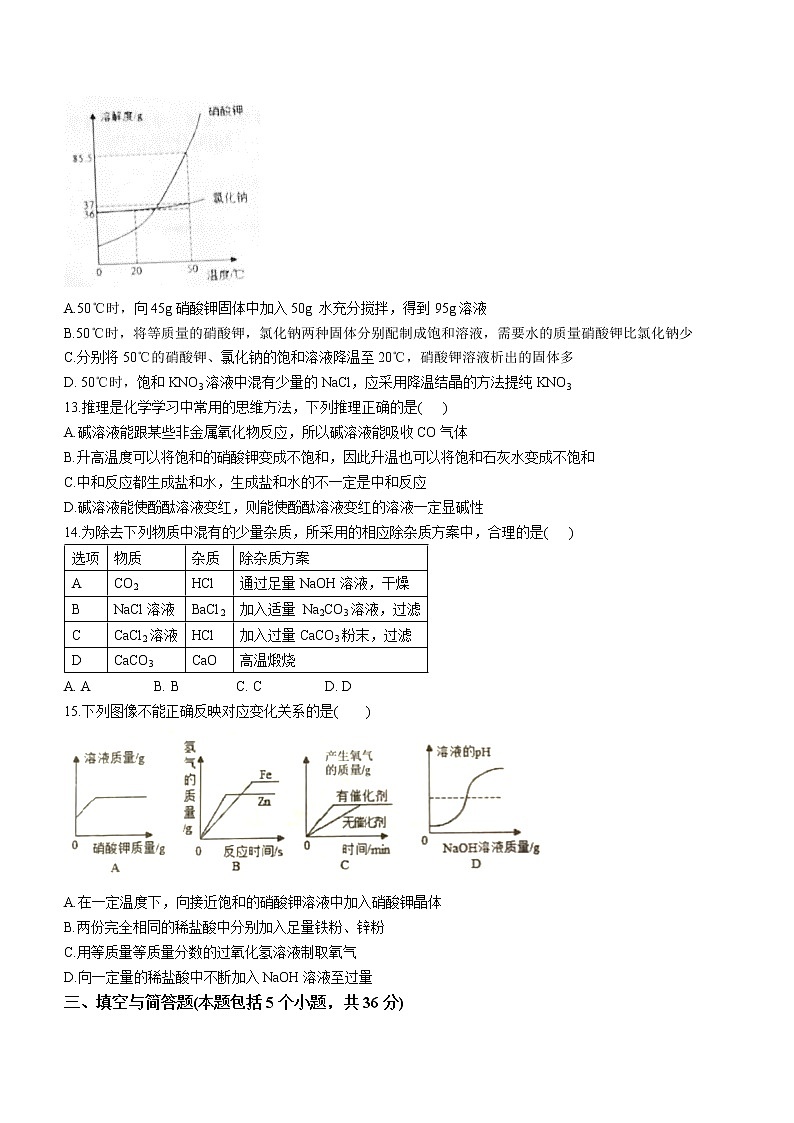
2022—2023学年度第一学期期中教学质量检测初四化学试题一、选择题(本题包括10个小题,每小题只有一个选项符合题意,共20分)1.下列各组物质中,前者为后者溶质的是( )A.酒精、碘酒 B.冰、冰水C.植物油、油水 D.氯化氢、盐酸2.下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是( )A.浓盐酸 B.浓硫酸 C.石灰水 D.烧碱溶液3.了解溶液的酸碱性,对于生活、生产以及人类的生命活动具有重要的意义。现测得生活中一些物质的pH (常温)如下:物质淡盐水肥皂水汽水蔗糖水苏打水自来水pH7103~477.5~9.06~7下列说法中不正确的是( )A.自来水呈中性或弱酸性 B.苏打水比肥皂水的碱性强C.淡盐水、蔗糖水呈中性 D.汽水能使蓝色石蕊试纸变红4.下列说法不正确的是( )A.浓硫酸敞口放置一段时间后,溶液的质量减小B.浓盐酸在空气中会冒白雾C.浓盐酸敞口放置一段时间后, 溶质的质量分数减小D.浓硫酸溶于水时放出热量5.溶液对我们的生产生活都有非常重要的意义、下列有关溶液的说法不正确的是( )A.饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液B.乳化后形成的乳液与溶液同样稳定C.物质在溶解过程中都会伴随着能量的变化D.升高温度可使大多数固体物质的饱和溶液变为不饱和溶液6.下列各选项是初中化学中常见的实验操作,其中操作完全正确的是( )A.稀释浓硫酸 B.倾倒液体C.称量固体 D.过滤7.硫酸是一种经常用到的酸。下列有关硫酸的说法正确的是( )A.构成:硫酸溶液中H+和的数目相等B.性质:能与CO2等非金属物质反应C.用途:用于生产化肥、农药、炸药、染料等D.生产:含硫酸的工业废水,用CaCl2处理后直接排放8.下列能发生复分解反应的是( )A.氯化银和稀硝酸 B.碳酸钡和硫酸钠C.硝酸钠和氯化铁 D.氢氧化锁和稀硝酸9.下图是氢氧化钙的溶解度曲线,下列说法正确的是( )A氢氧化钙易溶于水B加热氢氧化钙的饱和溶液,溶液会变浑浊C 30℃时氢氧化钙的饱和溶液中溶质质量分数为15%D.将80℃时氢氧化钙的饱和溶液降温到30℃,溶质质量分数碱小10.向氢氧化钠溶液中加入一定量的稀硫酸,取少量反应后的混合液进行下列实验,能证明二者恰好完全中和的是( )A.滴入几滴酚酞溶液,溶液变红色B.滴入适量CuCl2溶液,无沉淀生成C.滴入适量BaCl2溶液和稀硝酸,观察到有白色沉淀D.测得混合液中Na+与的个数比为2: 1二、选择题(本题包括5个小题,每小题有1个或2个选项符合题意,共10分)11.有一瓶失去标签的无色溶液,有四位同学在实验前,对其中所含的离子进行了不同的猜测,请你判断可能正确的是( )A. Na+、、H+ B. Ca2+、、C. H+、Ba2+、Cl- D.OH-、K+、H+12.如图是氯化钠、硝酸钾两种物质的溶解度曲线。下列说法正确的是( )A.50℃时,向45g硝酸钾固体中加入50g 水充分搅拌,得到95g溶液B.50℃时,将等质量的硝酸钾,氯化钠两种固体分别配制成饱和溶液,需要水的质量硝酸钾比氯化钠少C.分别将50℃的硝酸钾、氯化钠的饱和溶液降温至20℃,硝酸钾溶液析出的固体多D. 50℃时,饱和KNO3溶液中混有少量的NaCl,应采用降温结晶的方法提纯KNO313.推理是化学学习中常用的思维方法,下列推理正确的是( )A.碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体B.升高温度可以将饱和的硝酸钾变成不饱和,因此升温也可以将饱和石灰水变成不饱和C.中和反应都生成盐和水,生成盐和水的不一定是中和反应D.碱溶液能使酚酞溶液变红,则能使酚酞溶液变红的溶液一定显碱性14.为除去下列物质中混有的少量杂质,所采用的相应除杂质方案中,合理的是( )选项物质杂质除杂质方案ACO2HCl通过足量NaOH溶液,干燥BNaCl溶液BaCl2加入适量 Na2CO3溶液,过滤CCaCl2溶液HCl加入过量CaCO3粉末,过滤DCaCO3CaO高温煅烧A. A B. B C. C D. D15.下列图像不能正确反映对应变化关系的是( )A.在一定温度下,向接近饱和的硝酸钾溶液中加入硝酸钾晶体B.两份完全相同的稀盐酸中分别加入足量铁粉、锌粉C.用等质量等质量分数的过氧化氢溶液制取氧气D.向一定量的稀盐酸中不断加入NaOH溶液至过量三、填空与简答题(本题包括5个小题,共36分)16. (5分)溶液在日常生活、工农业生产中与我们息息相关。(1)生理盐水是医疗上常用的一种溶液,其溶质是______;其溶液里存在的微粒是_______(用符号表示)。(2)喝了冰镇汽水以后,常常会打唱,这种现象说明气体的溶解度与______有关。(3)现有100g溶质质量分数为10%的葡萄糖溶液,若使溶液的溶质质量分数增大一倍,应向此溶液中加入葡萄糖________g。(4)浓硫酸有吸水性,常用作某些气体的干燥剂,下列气体不能用浓硫酸干燥的是_______(填写序号)。A.H2 B.CO2 C.NH3 D. HCl17. (11分)构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络:请完成下列问题:(1)如用湿润的pH试纸测定盐酸的pH,则结果会___ (填“偏大”“偏小”或“无影响”)。(2)图1中①的现象是____________。(3)世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的_______(填“Fe2+”或“Fe3+”),该反应的原理是利用了酸的________(填序号 “②”“③”“④”或“⑤”)化学性质。请再列举一个化学反应体现酸的该条性质,写出反应方程式______________。(4)小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是_______(用符号表示),该反应的微观实质可表示为H++OH-=H2O。依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为_____________。(5)图1中⑤的性质可用于除铁锈,反应的化学方程式为__________________。(6)盐酸、硫酸,食醋具有相似化学性质是因为它们水溶液中都含有_______(用符号表示)。18. (8分)如图为碳酸钠和碳酸氢钠两种物质的溶解度曲线,请回答下列问题:(1)30℃时,Na2CO3的溶解度是________g。(2)40℃时,向两只各盛有100g水的烧杯中,分别加入Na2CO3、NaHCO3固体,至恰好不再溶解为止,所得溶液的溶质质量分数大的是_________溶液,将这两份饱和溶液分别升温到60℃,溶液质量分数的变化分别为:______________。(3)将40℃时等质量的Na2CO3和NaHCO3的饱和溶液同时降温到10℃,析出晶体较少的是_______溶液。(4)A、B两点分别表示Na2CO3的两种溶液,要使B点的溶液变为A点的溶液,可采取措施是_______、________。(5)小英同学说,常温下,她配制了一瓶溶质质量分数为16.4%的NaHCO3饱和溶液,请判断小英同学的说法是否正确,________(填“是”或“否”)。(6)20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中(如图)。向烧杯中加入某物质后,试管底部的粉末消失,则加入的物质可能是_______(填字母序号)。①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体A.①③④ B.②⑤⑥ C.①③⑤ D.②④⑧19. (6分)图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。(1)性质①,将紫色石蕊试液滴入氢氧化钠溶液中,溶液呈______色。(2)性质②,将氢氧化钠溶液滴入稀盐酸中反应的化学方程式是:____________,图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是_____ (填化学式)。(3)依据性质③,氢氧化钠与二氧化硫反应的化学方程式为__________________。(4)性质④,将氢氧化钠溶液和某种盐反应产生蓝色沉淀,该盐的化学式可能是________。20. (6分)A、B、C、D、E、F是初中化学中常见的物质,A是常用食品干燥剂的主要成分,D是温室气体之一,F可用于玻璃、造纸、纺织、洗涤剂的生产。它们之间的关系如图(图中“-”表示相连两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物或生成物及反应条件),分析推理,回答下列问题:(1) F物质的俗称是________,B物质分类属于____ ( 填“酸”或“碱”或“盐”)。(2) A生成C的反应中能_______热量(填“吸收”或“放出”)。(3) 写出C→E反应的化学方程式____________,此反应的基本反应类型是_______反应。四、实验探究题(本题包括3个小题,共28分)21.(8分)实验室配制质量分数为10%的NaCl溶液,如图1是某同学的实验操作过程:(1)用图1中的序号表示配制溶液的正确操作顺序是________。(2)若③中游码读数为1.2,则他称取NaCl的质量是________g。(3)按照图③称量的药品来配制溶液,该同学需要用水的体积是_________mL。(水的密度为1.0g/mL)(4)他按图2量取水的体积,若其他操作步骤均无误差,则其所配溶液溶质质量分数________(填“大于”“等于”或“小于”)10%。(5)配制好的溶液应装入________(填仪器名称)中,并贴上标签。装瓶时,若有液体洒出会导致溶质质量分数______(填“变大”“变小”“不变”)。(6)现在需要该溶液80g,实验室提供100g质量分数为16%的NaCl溶液和足量NaCl固体和水,请再拟定一个配制方案:_____ (写出所选试剂和用量即可)。22. (11分)小明同学在整理实验室时发现了一瓶敞口放置的氯氧化钠溶液,他认为该溶液可能变质了,于是邀来小琳和小可,对该溶液中溶质成分进行实验探究。[猜想与假设]小可认为该溶液中溶质是NaOH;小琳认为该溶液中溶质是Na2CO3;小明却认为该溶液中溶质是________(填化学式)。【查阅资料】氯化银溶液显中性:碳酸钡难溶于水。【进行实验】实验实验操作实验现象①小可取适量该溶液,滴入几滴无色酚酞溶液溶液变红色②小琳取适量该溶液,滴入过量氯化钡溶液产生白色沉淀③小明取适量该溶液,滴入过量氯化钡溶液产生白色沉淀④小明取适量实验③所得的上层清液,滴入几滴无色酚酞溶液溶液变红色【实验结论】(1)根据实验①和②可以得出结论:该溶液中一定含有的溶质是____ (填化学式)。_______同学的猜想一定是错误的。原因是________。(2)实验③中,加入过量氯化钡的原因是_______,根据实验③和④。你认为小明同学的猜想_______(填“正确”或“错误”)。(3)实验③反应后,溶液中存在的大量离子是______,其中使实验④中酚酞试液变红的的离子是_______。【反思与交流】(4)氢氧化钠溶液变质的原因是(用化学方程式表示)_____,实验室为了防止氢氧化钠溶液变质,正确的措施是______________。23. (9分) 在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老师引导下开展实验探究活动,请你参与下列活动。【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。(1)测定溶液pH变化的方法甲同学在实验过程中测得pH变化如图1所示,则该同学是将_________(填字母序号)。a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中(2)测混合过程中的温度变化乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是____________(填“放热”或“吸热”)反应。图2中B点表示的含义是____________。(3)借助于酸碱指示剂丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为____________。【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。【猜想与假设】猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH【进行实验】为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:实验方案实验操作实验现象实验结论方案一取少量反应后的溶液于试管中,加入Fe2O3粉末________溶液中有H2SO4猜想二正确方案二取少量反应后的溶液于试管中,滴加BaCl2溶液②产生白色沉淀溶液中有H2SO4,猜想二正确【实验结论】通过探究,同学们一致确定猜想二是正确的。【评价与反思】(4)丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是____________。(5)同学们经过反思与讨论,最后认为方案一中的 Fe2O3粉末可以用下列的某些物质代替,也能得到同样的实验结论,请你选出可用药品的字母序号________。A. Mg B. CuO C. KCl D. Na2CO3(6)分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还要考虑____________。五、计算题(本题包括1个小题,共6分)24. (6分)工业上从海水中提取出MgCl2、KCl两种物质的混合物,为了测定其中KCl的质量分数,现进行如下测定。取混合物样品19g,向其中加入100g水,完全溶解后,滴加KOH溶液,生成沉淀的质量与加入KOH溶液的质量关系如图所示。请计算:(1)混合物样品中KCl的质量分数。(2)当恰好完全反应时,所得溶液中溶质的质量分数。(计算结果精确至0.1% )2022—2023学年度第一学期期中教学质量检测初四化学参考答案及评分标准一、二选择题答题表(第一大题每题2分,第二大题每题2分,有2个选项的漏选得1分,错选、多选均不得分,共30分)1~5:DCBAB 6~10:CCDBD11.C 12.BD 13.CD 14.BC 15.B三、填空与简答题(本题包括5个小题,共36分)16.(5分)(1)氯化钠;Na+、Cl-、H2O;(2)温度;(3)12.5;(4)C17.(11分)(1)偏大;(2)变红色;(3)Fe2+;②;Mg+2HCl=MgCl2+H2↑;(4)Na+、;Ag++Cl-=AgCl↓;(5)Fe2O3+6HCl=2FeCl3+3H2O;(6)H+18.(8分)(1)40;(2)碳酸钠;碳酸钠溶液减小,碳酸氢钠溶液不变;(3)碳酸氢钠(NaHCO3);(4)增加碳酸钠质量;恒温蒸发溶剂;(5)否;(6)B19.(6分)(1)蓝;(2)NaOH+HCl=NaCl+H2O;NaOH、NaCl;(3)2NaOH+SO2=Na2SO3+H2O(4)Cu(NO3)2、CuCl2、CuSO4等20.(6分)(1)苏打或纯碱;酸;(2)放出;(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;复分解。四、实验探究题(本题包括3个小题,共28分21.(8分)(1)②③①⑤④;(2)5.8;(3)52.2;(4)小于;(5)细口瓶;不变;(6)50g16%的NaCl溶液和50g水。22.(11分)【猜想与假设】NaOH和Na2CO3(1) Na2CO3;小可;加入氯化钡溶液出现白色沉淀说明一定含有碳酸钠(2)除尽溶液中的碳酸钠;正确(3) Na+、Cl-、Ba2+、OH-;OH-(4) CO2+2NaOH=Na2CO3+H2O;密封保存氢氧化钠溶液23. (9分)(1)a;(2)放热;KOH和H2SO4恰好完全反应;(3)2KOH+H2SO4=K2SO4+2H2O;固体粉末减少(或消失),溶液变成黄色(4)K2SO4与BaCl2反应也会产生白色沉淀,无法证明H2SO4一定存在(5) ABD;(6)反应物是不过量(或反应物是否有剩余)。五、计算题(本题包括1个小题,共6分)24. (6分)解:设样品中氯化镁的质量为x,滴加氢氧化钾溶液恰好反应生成氯化钾的质量为yMgCl2+2KOH=Mg(OH)2↓+2KCl95 58 149x 5.8g y,解得x=9.5g ,解得y=4.9g样品中氯化钾的质量分数为×100% =50%反应后所得溶液的溶质质量分数是×100%=10%。答:略
相关试卷
这是一份山东省烟台市蓬莱区(五四制)2021-2022学年九年级上学期期末考试化学试题,共23页。试卷主要包含了5 Fe-56 Ba-137,3%,钢中的含碳量为0,0 刷漆等内容,欢迎下载使用。
这是一份16,2024年山东省烟台市蓬莱区中考二模化学试题,共23页。试卷主要包含了考试结束后,只交答题卡,可能用到的相对原子质量, 空气是一种宝贵的自然资源等内容,欢迎下载使用。
这是一份03,山东省烟台市蓬莱区(五四制)2023-2024学年九年级上学期期末考试化学试题,共24页。试卷主要包含了选择题,理解与应用,实验与探究,计算题等内容,欢迎下载使用。









