






所属成套资源:全套中考化学复习难点加强练课件
- 中考化学复习难点加强练一溶解度曲线及其应用课件 课件 0 次下载
- 中考化学复习难点加强练三酸碱盐课件 课件 1 次下载
- 中考化学复习难点加强练四微观反应示意图课件 课件 0 次下载
- 中考化学复习难点加强练五根据信息书写化学方程式课件 课件 0 次下载
中考化学复习难点加强练二金属课件
展开
这是一份中考化学复习难点加强练二金属课件,共35页。PPT课件主要包含了答案C,答案A,答案D,无毒合理即可,耐腐蚀合理即可,不易破损合理即可,携带方便合理即可,子的最外层电子数相同,金或Au,铁完全反应等内容,欢迎下载使用。
1.兴趣小组同学用未打磨的铝片与稀盐酸反应,并用压力传感器测定密闭容器中气体压强与时间的关系如图。下列对该反应的说法不正确的是( )
考察角度1 金属与酸反应的曲线
A.反应过程中有热量放出B.AB段曲线变化不明显,是因为铝表面有氧化膜C.BC段气体压强迅速增大,是温度升高的原因D.CD段曲线下降,是反应停止温度降低的原因
【点拨】A.氧化铝和稀盐酸的反应是放热反应,故反应过程中有热量放出,故正确;B.AB段曲线发生的是氧化铝和稀盐酸反应,故此时压强变化不明显,故正确;C.BC段发生的是铝与稀盐酸反应,此时气体压强迅速增大,故错误;D.铝与稀盐酸的反应也是放热反应,而CD段曲线下降,是因为反应停止温度降低,故正确;故选C。
2.【2022泉州一检3分】常温下,往盛有一定质量稀H2SO4的烧杯中加入过量锌粒,测得烧杯内溶液温度随时间变化的关系如图。下列分析正确的是( )A.Zn与稀H2SO4反应先放热后吸热B.往y点对应的溶液中加入铁粉,有气泡产生C.x、y点对应的溶液中,参加反应的Zn与H2SO4质量比相等D.x、z点对应的溶液中ZnSO4质量相等
3.【2022三明模拟3分】下列事实不能用金属活动性解释的是( )A.铝制品比铁制品耐腐蚀B.用硫酸铜溶液和铁制取铜C.用硫酸铜溶液、铁、银验证铁、铜、银金属活动性D.金属铜不能与稀硫酸反应
考察角度2 金属活动性顺序的判断及探究
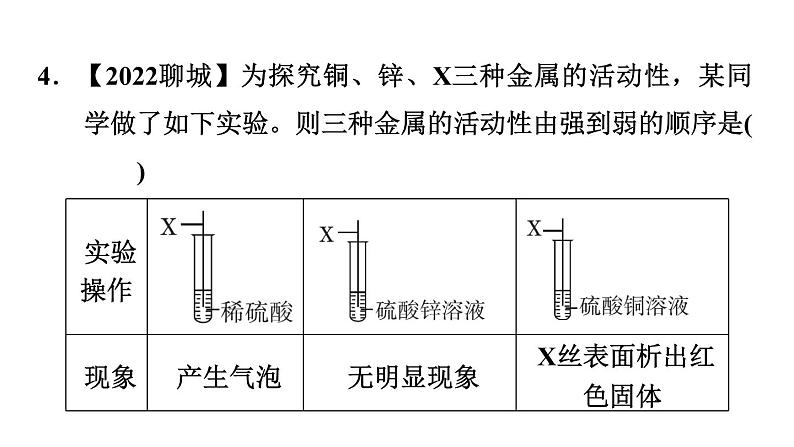
4.【2022聊城】为探究铜、锌、X三种金属的活动性,某同学做了如下实验。则三种金属的活动性由强到弱的顺序是( )
A. 锌、X、铜 B.X、锌、铜C.锌、铜、X D.铜、X、锌
5.已知铁、铜、银三种金属的转化关系如图(“→”表示在溶液中一步进行的置换反应)。下列有关推理正确的是( )
A.转化①的现象是红色金属表面附上银白色固体B.转化②的原理可表示为Fe+3AgNO3===Fe(NO3)3+3AgC.由该转化图可得,铁在金属活动性顺序中位于氢后D.完成转化③可用的试剂为Cu和AgNO3溶液
6.【2022湖北二模】向盛有10g 49%稀硫酸的烧杯中加入5.6 g铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )A.取a点溶液,加入锌粉,有气体放出B.b点时,溶液中溶质只有一种C.c点时,烧杯中固体一定有铜,可能有铁D.m=15.4
考察角度3 金属与盐溶液反应后的物质分析
7.【2022宜昌】 向装有一定量硝酸铜和硝酸银混合溶液的试管中,缓慢加入细铁粉,充分反应。下列关于试管中物质的变化关系图错误的是( ) A B C D
8.物尽其用——金属之“铝”。(1)铝制易拉罐(如图1):某品牌碳酸饮料的易拉罐是由铝合金制成的,内壁附着一层有机薄膜。该铝合金中铝的含量约为97%,还含有镁、锰、铁、铟(In)等。
考察角度4 金属的综合应用
①将易拉罐剪成条状,打磨后与纯铝片相互刻画,发现纯铝片表面有划痕,说明____________________________。②请你推测组成有机薄膜的物质具有的性质:_____________、____________________。
合金的硬度比纯金属的大
③“是否应该停止使用铝制易拉罐”是当前的一个社会性科学议题。有同学认为应该停止使用铝制易拉罐,理由可能是___________________________________(写一条即可);也有同学支持继续使用铝制易拉罐,请你结合铝的性质阐述理由:____________________、___________________。
提炼铝制易拉罐会产生污染(合理即可)
④生活垃圾要分类投放,可与废弃易拉罐作为同一类投放的是______(填字母)。A.废旧电池 B.废弃口罩C.厨余垃圾 D.废旧铁锅(2)制备铝:工业上常用电解氧化铝的方法制备金属铝,反应的化学方程式为_______________________________。
(3)铝合金中的铟(In):如图2为铝、铟的原子结构示意图。某同学推测金属铟与铝的化学性质相似,理由是____________________________。实验证明,铟可以与稀盐酸反应,其反应的化学方程式为_________________________________________________。
2In+6HCl===2InCl3+3H2↑
9.【2022泉州期末6分】废旧手机的电路板中含有铝、铁、铜、金等多种金属,随意丢弃会造成资源浪费,还会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如图所示实验。已知:铜在稀硫酸和H2O2中溶液会发生反应,生成硫酸铜和水,金不发生类似反应。
(1)将电路板粉碎成粉末的目的是__________________________________________________________________。(2)步骤一所得滤渣中的贵重金属是__________,用过量稀硫酸的目的是_____________________________。
增大反应物接触面积,使反应更充分
(3)写出步骤三中生成铜反应的化学方程式:___________________________________________。
Fe+CuSO4===FeSO4+Cu
10.物质王国正在举行排球赛,A~F均为参赛球员,分别是铜、铁、水、氧气、氧化铜、四氧化三铁中的一种,A、F含有一种相同的金属元素且A、C、D为单质。六位球员分为两组,如图所示,能接住对方的发球即为对方反应的生成物(同组内不互相接球),若本次比赛中它们的传球顺序为A→D→……→F(每位球员均参与了一次传球),请回答下列问题:
(1)E的名称为____________。(2)C的一种用途是____________________。(3)D传球给“下一位球员”时所发生反应的化学方程式为________________________________。(4)只有能与三个“参赛球员”发生反应的物质才能作为“裁判”,下列能当裁判的物质是________(填序号)。①CaO ②AgNO3 ③CO ④CO2
11.【2022三明模拟10分】化学反应的快慢与许多因素有关,控制变量法是科学探究中常用的方法。 某兴趣小组设计以下实验探究影响金属与酸反应快慢的因素。 【实验1】取四份等质量的铁分别与足量的盐酸进行反应,实验条件如下表所示;图1为反应时间与产生气体体积的关系曲线。
(1)对比图1中实验a和b的曲线,得出的结论是____________________________________________,能得出相同结论的另一对比的组别是____(用字母 a、b、c、d 表示);该实验中还有另外一组对比实验,能得出的结论是__________________________________________________________。
相同条件下,温度越高,金属与酸反应速率越快
相同条件下,金属表面积越大,金属与酸反应速率越快
(2)实验中观察到气体产生速率“逐渐变快又变慢”,“逐渐变快”的原因是_________________________________。(3)该反应的化学方程式为___________________________。
铁与稀盐酸反应放热,反应速率加快
Fe+2HCl===FeCl2+H2↑
【实验2】常温时,用足量的铁、锌、镁三种金属分别与等量同浓度的盐酸反应。 实验发生装置如图甲所示;压强变化如图乙所示(压强越大,表示产生氢气的量越多)。
(4)实验中,还需要控制的变量是___________________。(5)实验得出的结论是金属与酸反应的速率与______________有关。(6)该实验中发现镁与盐酸反应,最终测得的压强比锌和铁更大一点。忽略误差,其合理的原因是_____________________________________________________。
镁与稀盐酸反应放出热量较多,使气体膨胀
12.【2022南平质检7分】 某校化学兴趣小组,确定了“探究铁生锈的影响因素”的研究性学习项目,请你参与他们的研究项目,完成相关研讨。(1)如图1是来自教材的实验设计,若要证明“与氧气接触是铁生锈的必要条件”,需将试管________(填“①”或“②”)与试管③对照。
(2)使用“迅速冷却的沸水”目的是_____________________。(3)同学们用图2中A装置探究铁生锈的原理,测量实验过程中装置内温度与相对湿度(体现水蒸气含量)的变化分别如图2中B、C所示。请解释装置内相对湿度升高的原因:________________________。
铁生锈放热,使水分蒸发
(4)同学们从耗氧量的角度设计实验,研究铁生锈原理,以及在稀醋酸、氯化钠溶液存在时对铁生锈速率的影响,实验方案如下表所示。
测得4组实验装置内氧气含量变化如图3中D所示。①实验a和b对照的结论是___________________________。②通过实验________对照,可以证明“氯化钠溶液存在会加速铁的生锈”。
与水接触是铁生锈的必要条件
(5)兴趣小组向全班同学汇报实验成果时,表演了一个趣味实验,设计如图3中E的实验装置,测量铁生锈过程中装置内压强变化,数据见图3中F。请解释:图3F中曲线BC段压强突然增大的原因是______________________________________________________________________________________________________________________。
铁生锈消耗氧气,装置内压强减小,稀硫酸被吸入试管,与铁粉反应生成氢气,使装置内压强增大
相关课件
这是一份中考化学复习难点加强练五根据信息书写化学方程式课件,共17页。PPT课件主要包含了硫酸铜合理即可,HCHO和O2,NH3·H2O等内容,欢迎下载使用。
这是一份中考化学复习难点加强练四微观反应示意图课件,共15页。PPT课件主要包含了答案C等内容,欢迎下载使用。
这是一份中考化学复习难点加强练三酸碱盐课件,共46页。PPT课件主要包含了答案C,OH-,CuSO4,CaOH2,氧化物,答案B,Na+和Cl-,碳酸根离子和氢离子,FeOH3,稀盐酸等内容,欢迎下载使用。









