





科粤版九年级上册第五章 燃料综合与测试复习课件ppt
展开考点一 单质碳的性质和用途
1. 碳单质的物理性质和用途(1)金刚石、石墨 C60 都是碳单质 金刚石、石墨由原子构成 C60 由分子构成(2)石墨在一定条件下可转化为金刚石,属于________(填“物理”或“化学”)变化。(3)用炭黑墨汁绘制的字画经久不变色是由于
在常温下碳的化学性质不活泼
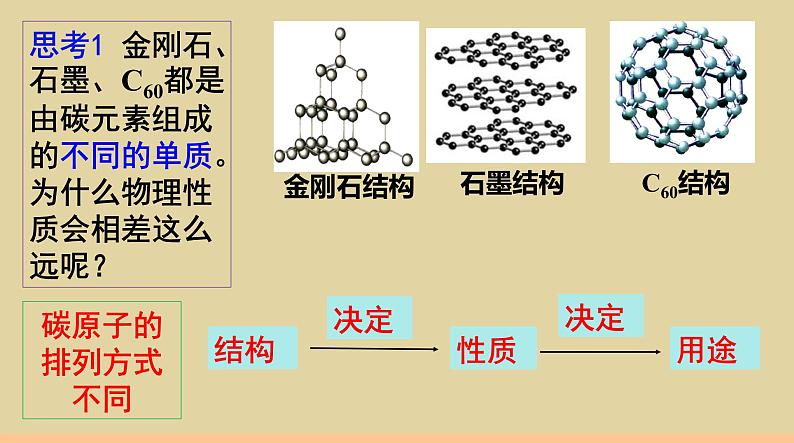
思考1 金刚石、石墨、C60都是由碳元素组成的不同的单质。为什么物理性质会相差这么远呢?
碳的各种单质虽然物理性质差别很大,但都具有相同的化学性质,这是因为它们都是由________构成的。
(1)碳的单质在常温下化学性质__________。
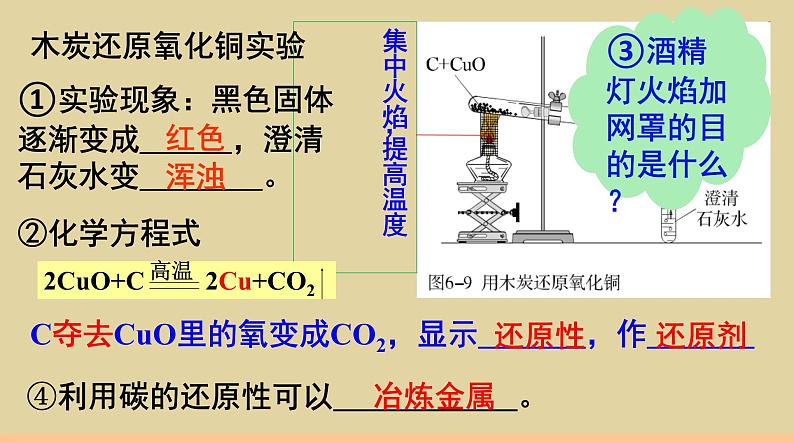
C+2CuO === 2Cu+CO2↑
C+ CO2 === 2CO
①实验现象:黑色固体逐渐变成______,澄清石灰水变________。
C夺去CuO里的氧变成CO2,显示_______,作_______
③酒精灯火焰加网罩的目的是什么?
④利用碳的还原性可以____________。
1、下列有关碳单质的说法错误的是( ) A.金刚石是天然存在最硬的物质 B.石墨和C60是由不同种原子构成 C.金刚石和石墨的化学性质相似 D.活性炭包可放在冰箱中除异味
2、化学上把同种元素组成的不同单质互称为同素异形体,例如白磷和红磷。下列各组物质互为同素异形体的是 ( ) A.一氧化碳和二氧化碳 B.金刚石和石墨 C.冰和干冰 D.氧气和液氧
3.下列有关碳单质的说法不正确的是( )A. 金刚石是自然界最硬的物质,可作钻头B. 石墨有导电性,可制作电极C. C60具有稳定结构,不能燃烧D. 活性炭疏松多孔,具有强烈的吸附性,可用于净水
_________,在1体积水里约溶解1体积二氧化碳。
2.CO2的化学性质:
不能燃烧不支持燃烧不能供给呼吸。
CO2能使澄清石灰水变浑浊。这个反应常用于检验CO2的存在。
CO2通入紫色石蕊溶液,使之变红色。
灭火、人工降雨、气体肥料、化工原料
①一般情况下,不燃烧也不支持燃烧如图1,向放有阶梯蜡烛的烧杯中倾倒CO2,观察到______层蜡烛先熄灭,______层蜡烛后熄灭。结论:CO2______________________(化学性质);_______________(物理性质)。②与水反应如图2,向紫色石蕊溶液中通CO2一段时间后,观察到紫色石蕊溶液变______。结论:CO2通入紫色石蕊溶液生成能使紫色石蕊溶液呈红色的物质______,化学方程式为____________________;加热上述所得的溶液,观察到_________________________原因是碳酸不稳定,容易分解成CO2和H2O,化学方程式为____________________。
H2O+CO2=== H2CO3
有气泡产生,溶液由红色变成紫色
③与碱反应a.与澄清石灰水反应,如图3,向澄清石灰水中通入CO2,澄清石灰水变________,反应的化学方程式为__________________________________,此反应常用来检验CO2气体。④与C反应:C+CO2 2CO(吸热反应)⑤光合作用:6CO2+6H2O C6H12O6+6O2。
Ca(OH)2+CO2=== CaCO3↓+H2O
注意:点燃一氧化碳前应做什么?
一氧化碳跟血液中的血红蛋白的结合能力比氧气强,使人体缺少氧气而窒息,甚至死亡。
4. CO与CO2的区别与联系(1)CO与CO2化学性质不同的原因:分子构成不同。(2)CO与CO2在一定条件下可以相互转化:5. CO和CO2的鉴别及除杂(1)鉴别方法
使紫色石蕊溶液变为红色
(2)互为杂质时的除杂方法(括号内为杂质)①CO2(CO):将混合气体通过灼热的氧化铜;②CO(CO2):将混合气体依次通过足量的氢氧化钠溶液和浓硫酸,或将混合气体通过灼热的碳粉。【易错警示】不能用点燃的方法除去CO2中的CO。
4、 要除去二氧化碳中混有的一氧化碳,可把混合气体通过( ) A.水 B.灼热的氧化铜 C.澄清石灰水 D.炽热的炭层
解题思路: 一氧化碳不能溶于水,而二氧化碳能溶于水;把混合气体通过澄清石灰水,一氧化碳不与氢氧化钙发生反应,而二氧化碳与氢氧化钙发生反应而被除去;通过炽热的炭层,一氧化碳不与碳反应,二氧化碳却与碳反应生成一氧化碳而被除去。本题选B
解题思路:CO2的化学性质主要就是三不二水一碳;CO2的物理性质主要考察密度和溶解性。通常情况下,CO2的密度比空气大。本题选D。
5、
6. 下列说法不正确的是( )A. 二氧化碳有毒,不能供给呼吸B. 二氧化碳能溶于水,所以可以用来制作汽水C. 干冰升华时吸收大量的热,所以常用于人工降雨D. 二氧化碳不能燃烧,不支持燃烧,密度比空气大,所以常用于灭火
7、如图烧杯底部木块上固定有一根铜丝,铜丝上绑了四朵纸花,其中①④是干燥的紫色石蕊纸花,②③是湿润的紫色石蕊纸花,向烧杯中慢慢倾倒二氧化碳。
(1)你将会观察到什么现象? (2)石蕊纸花变色的原因是什么? (3)该实验说明二氧化碳具有什么物理性质?
②比③先变红,①和④均不变色。
二氧化碳和水反应生成了碳酸,碳酸显酸性,能使紫色石蕊溶液变为红色。
二氧化碳密度比空气大。
8、如图所示,将充满CO2的试管倒扣在装有氢氧化钠溶液的烧杯中。(1)本实验可观察到的现象是什么?
试管内液面上升,烧杯内液面下降。
(2)请用化学方程式解释产生上述现象的原因:_________________________________。
9、“低碳生活”倡导低能量、低消耗、减少某种含碳物质的排放,该含碳物质是( )A. 一氧化碳 B. 二氧化碳 C. 甲烷 D. 甲醇
10、 金刚石、石墨和C60都是碳元素的单质。下列说法中正确的是( ) A.它们是同种物质 B.它们的原子排列方式不同 C.它们都能导电 D.常温下它们都能与氧气反应
11、下列验证二氧化碳性质的实验中,不能证明二氧化碳化学性质的是( )
12.下列说法错误的是( ) A.古代字画年深日久不褪色,是因为碳在常温下化学性质不活泼B.产生温室效应的主要气体是二氧化碳 C.SO2和NO2是形成酸雨的主要物质D.在过氧化氢溶液中加入二氧化锰能生成的氧气更快、更多 13、 下列有关碳和碳的氧化物的说法,错误的是( ) A.CO和CO2组成元素相同,所以它们的化学性质也相同B.碳在空气中充分燃烧时生成CO2,不充分燃烧时生成COC.CO用于冶炼金属、做气体燃料;CO2同用于人工降雨、灭火D.清明上河图至今图案清晰可见,是因为在常温下碳单质的化学性质稳定
生活中处处有化学,请回答: (1)自来水生产过程中常用活性炭去除水中异味,这是利用活性炭的______性;(2)有些农村村民使用地下水作为生活用水,人们常用________检验地下水是硬水还是软水,生活中常用________的方法降低水的硬度(3)为了使燃料充分燃烧,应做的措施是________(写一条即可)(4)二氧化碳可以灭火说明它具有的性质_____ (5)自然界的水呈弱酸性原因(用化学方程式表示)_____ ___。 (6)二氧化碳只能用排水法收集,说明它具有的性质_____
不燃烧也不支持燃烧,密度比空气大
考点三 实验室制取气体的思路
1.实验室制取气体的思路(1)发生装置:由_______________________决定。 通常有______________和________________。(2)收集方法:由气体的_______________决定。 难溶于水的气体可用__________收集。 密度比空气大的气体,可用________________收集; 密度比空气小的气体,可用________________收集。
反应物状态及反应条件
2.二氧化碳的实验室制法(1)实验药品:___________________________。(2)实验原理:__________________________________。
石灰石(或大理石) 、稀盐酸
CaCO3+2HCl===CaCl2+H2O+CO2↑
(4)验满:将________木条放在集气瓶________,若火焰_____,则说明二氧化碳已经集满。
(5)检验:将气体通入澄清石灰水中,若澄清石灰水________,则证明该气体是二氧化碳。3.二氧化碳的工业制法工业上利用高温煅烧石灰石的方法制取二氧化碳,化学方程式为_________________________________。
CaCO3 =CaO+CO2↑
【14】根据如图所示实验装置图,回答有关问题。
(1)写出图中标有序号的仪器名称:①__________,②________。(2)实验室用大理石与稀盐酸反应制取二氧化碳,反应的化学方程式为____________________________________,制取二氧化碳最好选用的发生装置是____,该装置与另一个可选用的装置相比,其主要优点是____________________________。
CaCO3+2HCl===CaCl2+H2O+CO2↑
可以控制反应的发生和停止
(3)装入药品前应进行的操作是 ________________。
(4)请写出一种检验收集的气体为二氧化碳的方法______________________________________________________ ;
将收集到的气体通入澄清石灰水中,若石灰水变浑浊,则气体是二氧化碳
⑸用装置C制取气体,在反应过程中,用弹簧夹夹住导气管上的橡皮管,过一会儿反应就会停止。其原因是 。
气压增大,使稀盐酸与大理石脱离接触
(6)若利用装置A加热高锰酸钾制取氧气,还需要进行的改进是_______________________。
5. 某化学小组选用以下装置和药品进行探究实验。
①A中反应的化学方程式为__________________________________。②若将A、B连接,A中产生的气体并不能使B中的溶液变浑浊,这是为什么?
CaCO3+2HCl=== CaCl2+H2O+CO2↑
浓盐酸具有挥发性,A中生成的CO2气体中混有挥发出的HCl气体,不能生成CaCO3沉淀。
考点四 自然界中的CO2循环及温室效应
(3)防治:使用清洁能源,倡导“低碳”生活。
1.自然界中的CO2循环
2.温室效应(1)概念:大气中的____________就像温室的玻璃或塑料薄膜一样,既能让太阳光透过,又能使地面吸收的太阳光的热量不易向外散失,从而使全球变暖。(2)危害:全球气候______,两极冰川______,海平面升高,淹没部分沿海城市,使土地沙漠化,农业减产等。
15、按题意从O2、N2、H2、CO2、CO中选择适宜的化学式,填入下列横线上(1)有剧毒的气体:_____; (2)使带火星的木条复燃的气体:_____; (3)能在空气中燃烧的体: ; (4)空气中含量最多的气体:_______; (5)能使澄清石灰水变浑浊的气体:_____; (6)密度最小的是 ;(7)既有可燃性又有还原性的气体化合物是_____; (8)只能用向上排空气法收集的是_________。
1.由同种元素组成的物质不一定是单质。2.二氧化碳通入紫色石蕊溶液中使紫色石蕊溶液变红,是因为有碳酸生成,易误认为是二氧化碳本身使紫色石蕊溶液变红。3.二氧化碳的过多排放会导致温室效应,易误认为二氧化碳是空气污染物。4.二氧化碳不供给呼吸,易被学生误认为有毒。5.二氧化碳的溶解性是能溶于水而不是“易”溶于水;一氧化碳的毒性是一氧化碳的化学性质而不是物理性质。
考点五 化石燃料及其对环境的影响
_____、______、______称为三大化石燃料,是不可再生能源。1.煤及其对环境的影响(1)煤:“工业的粮食”,主要含_____元素。煤燃烧排放的污染物有_____ 、______、____等,其中能引起酸雨的有_________。(2) 煤的综合利用:将煤隔绝空气加强热(干馏),可以使煤分解成_______、_________、焦炉煤气等多种有用的物质,此过程为________ (填“物理”或“化学”)变化。
2.石油及其对环境的影响(1)石油:“工业的血液”主要含______、______两种元素。(2)石油的炼制:利用石油中各成分的______不同,将它们分离(分馏),可得到________、________、柴油等不同的产品,此过程为__________(填“物理”或“化学”)变化。(3)汽车尾气中的污染物有__________、_____________、_____________________、___________等。
3.天然气——较清洁的能源天然气的主要成分是甲烷,化学式为CH4。甲烷是最简单的有机化合物。物理性质:甲烷是______色______味的气体,________溶于水,可用__________法收集。化学性质:甲烷易燃烧,产生____色火焰,放出热量,燃烧的化学方程式:______________________________。
考点六 能源的利用与开发
1.清洁燃料:乙醇和氢气(1)乙醇乙醇俗称酒精,化学式为______________。物理性质:无色透明、易________、有特殊气味的液体,能与水以________________,并能溶解各种有机物。化学性质:酒精易燃烧,其燃烧的化学方程式: _____________________________。
车用乙醇汽油就是将变性乙醇和汽油以一定比例混合而形成的汽车燃料。
初中化学科粤版九年级上册1.4 物质性质的探究授课ppt课件: 这是一份初中化学科粤版九年级上册1.4 物质性质的探究授课ppt课件,共21页。PPT课件主要包含了化学性质,物理性质,导热性,导电性,延展性,溶解性,挥发性,吸附性,正在发生或改变,胆矾呈蓝色等内容,欢迎下载使用。
初中化学1.3 物质的变化教案配套课件ppt: 这是一份初中化学1.3 物质的变化教案配套课件ppt,共22页。PPT课件主要包含了观察活动,一物理变化,没有生成新物质,判断方法,实验1-6镁条燃烧,耀眼白,释放大量,化学变化,有新物质生成,观察实验三部曲等内容,欢迎下载使用。
化学九年级上册第五章 燃料5.2 组成燃料的主要元素——碳示范课课件ppt: 这是一份化学九年级上册第五章 燃料5.2 组成燃料的主要元素——碳示范课课件ppt,共24页。PPT课件主要包含了新课导入,金刚石,碳的化学性质,可燃性,1氧气充足,2氧气不足,用途作燃料等内容,欢迎下载使用。













