




所属成套资源:人教版化学选择性必修1PPT课件
人教版 (2019)第二章 化学反应速率与化学平衡第二节 化学平衡精品备课ppt课件
展开
这是一份人教版 (2019)第二章 化学反应速率与化学平衡第二节 化学平衡精品备课ppt课件,共18页。PPT课件主要包含了化学平衡状态,化学平衡常数,化学平衡常数K,浓度商Q等内容,欢迎下载使用。
定义:一定条件下的可逆反应里,当反应进行到一定程度时,正反应速率和逆反应速率相等,反应物和生成物的浓度不再发生改变。我们把这种状态称为化学平衡状态。
如何判断一个可逆反应是否达到平衡状态?
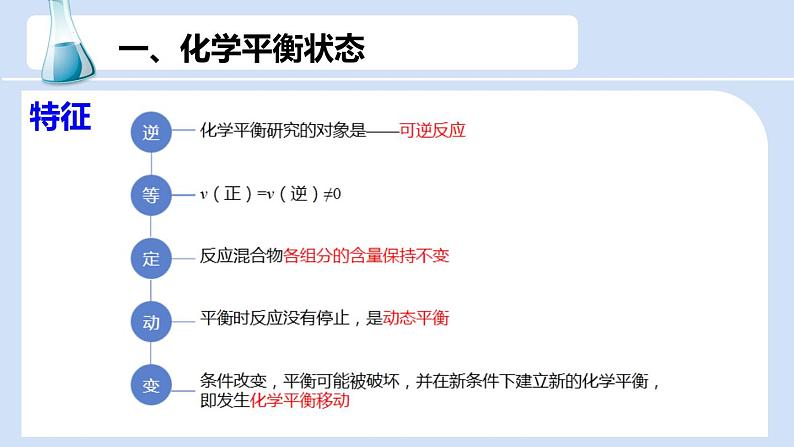
(1)v(正)=v(逆)≠0
①同一物质, V消=V生(消耗速率等于生成速率)
②不同物质,方向相反,速率之比=系数之比
(2)各种“量”不变 ①各物质的质量、物质的量或浓度不变。 ②各物质的百分含量(物质的量分数、质量分数等)不变。 ③温度、压强(化学方程式两边气体体积不相等)或颜色(某组分有颜色)不变。
“变量不变”时,达到平衡状态;若物理量恒为“不变量”,则不能作为平衡标志。
1.下列方法可以证明 H2(g)+I2(g) 2HI(g),已达平衡状态的是________________________________ A.单位时间内生成 n mlH2的同时,生成2n mlHI B.一个H-H键断裂的同时有两个 H-I键断裂 C.H2的百分含量与I2的百分含量相等 D.H2 I2 HI的反应速率之比为1:1:2 E.c(H2):c(I2):c(HI)== 2:2:1 F.温度和体积一定时,某一生成物浓度不再变化 G.温度和体积一定时,容器内压强不再变化 I.温度和体积一定时,混合气体颜色不再变化
A B F I
在一定温度下,化学平衡体系中反应物浓度与生成物浓度之间有什么关系呢?下面以反应H2(g)+ I2 (g) 2 HI(g) 为例进行分析。
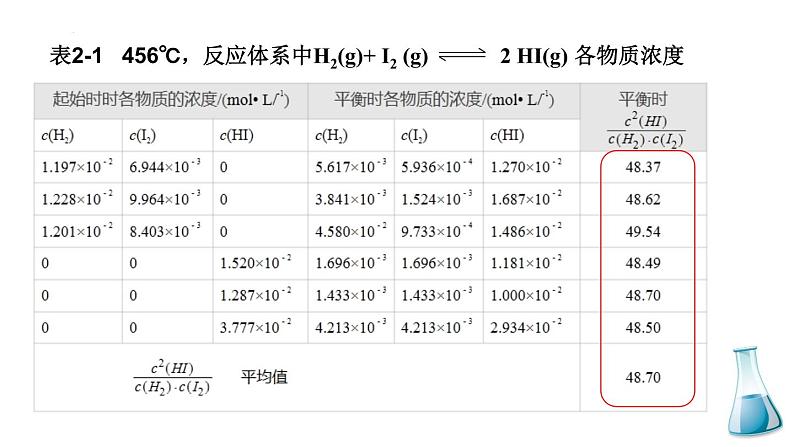
表2-1 456℃,反应体系中H2(g)+ I2 (g) 2 HI(g) 各物质浓度
分析上述数据可知,该反应在457.6℃达到平衡时,
是一个常数,与反应起始浓度大小,平衡建立方向无关。
对于一般的可逆反应,mA(g)+nB(g) pC(g)+qD(g) 在一定温度下的平衡体系:
在温度不变时,K为一常数,它用于定量地评价一个可逆反应在达平衡时限度,K值越大,化学反应的限度就越大。
一般来说,当K>105时,该反应就进行的基本完全了
对于一般的可逆反应,mA(g)+nB(g) pC(g)+qD(g)一定温度下任一时刻
注:固体和纯液体一般不列入浓度商或平衡常数
例1.在某温度下,将含有H2和I2各0.10ml的气态混合物充入10L的密闭容器中,充分反应并达到平衡后,测得c(H2)=0.0080ml•L-1。
(1)计算该反应的平衡常数
H2(g)+ I2 (g) 2 HI(g)
起始浓度/(ml·L-1)变化浓度/(ml·L-1)平衡浓度/(ml·L-1)
0.010 0.010 00.0020 0.0020 0.0080 0.0040
(2)在上述温度下,若起始时向该容器中通入H2和I2(g)各0.20ml,试求达到化学平衡时各物质的浓度。
0.020 0.020 0 x x 2x0.02-x 0.02-x 2x
设H2的变化浓度为xml/L
平衡时c(H2)=c(I2)=0.016ml/Lc(HI)=0.0080ml/L
2.在容积不变的密闭容器中,将2.0mlCO与10mlH2O混合加热到830℃,达到下列平衡:
此时该反应的K为1.0。求达到平衡时CO转化为CO2的转化率。
1.化学平衡常数只与温度有关,与反应物或生成物的浓度无关。2.固体或纯液体存由于其浓度可看作“1”而不代入公式。3.平衡常数的表达式与方程式的书写方式有关。 ①对于给定的化学反应,正逆反应的平衡常数互为倒数。 ②若化学方程式中各物质的化学计量数等倍扩大或缩小,系数变为原来的几倍,平衡常数变为原来的几次方。
使用化学平衡常数应注意的问题
相关课件
这是一份人教版 (2019)选择性必修1第二节 化学平衡优质ppt课件,共45页。PPT课件主要包含了动脑想一想,化学平衡状态,课堂练习,几乎相等,化学平衡常数,课堂小结,表达式及书写注意事项,意义及影响因素等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第二节 化学平衡获奖课件ppt,文件包含221化学平衡状态化学平衡常数练习解析版docx、221化学平衡状态化学平衡常数练习原卷版docx等2份课件配套教学资源,其中PPT共0页, 欢迎下载使用。
这是一份人教版 (2019)选择性必修1第二节 化学平衡获奖课件ppt,文件包含人教版高中化学选择性必修一221《化学平衡状态化学平衡常数》课件pptx、人教版高中化学选择性必修一221《化学平衡状态化学平衡常数》学案docx等2份课件配套教学资源,其中PPT共40页, 欢迎下载使用。










