




化学第一节 化学反应速率优质课件ppt
展开炎炎夏日,食物也怕“热”,需要及时放到电冰箱中;而发酵时却常用温水。【思考】(1)其中的道理是什么?(2)影响化学反应速率的因素有哪些?
1、认识浓度、压强、温度、催化剂等对化学反应速率的影响。(重点)2、初步运用有效碰撞、碰撞的取向和活化分子等来解释影响化学反应速率的外界因素。(难点)
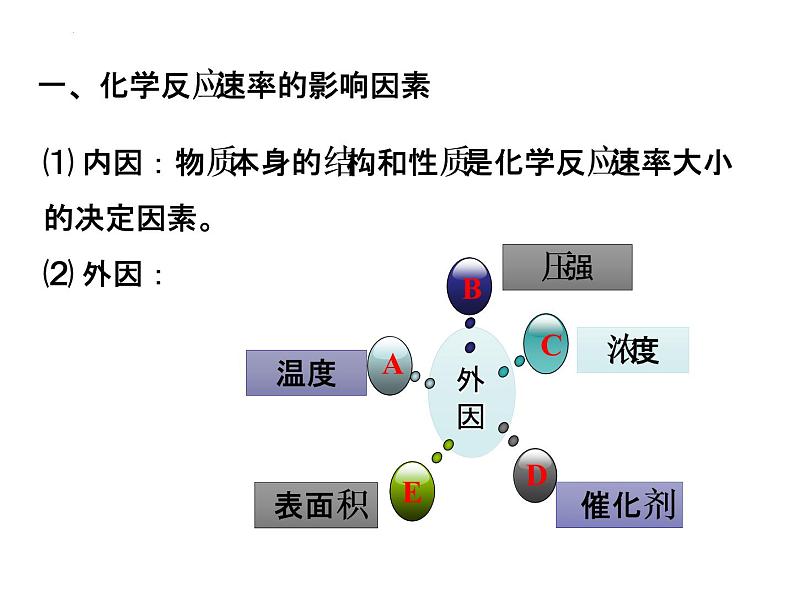
⑴ 内因:物质本身的结构和性质是化学反应速率大小的决定因素。⑵ 外因:
一、化学反应速率的影响因素
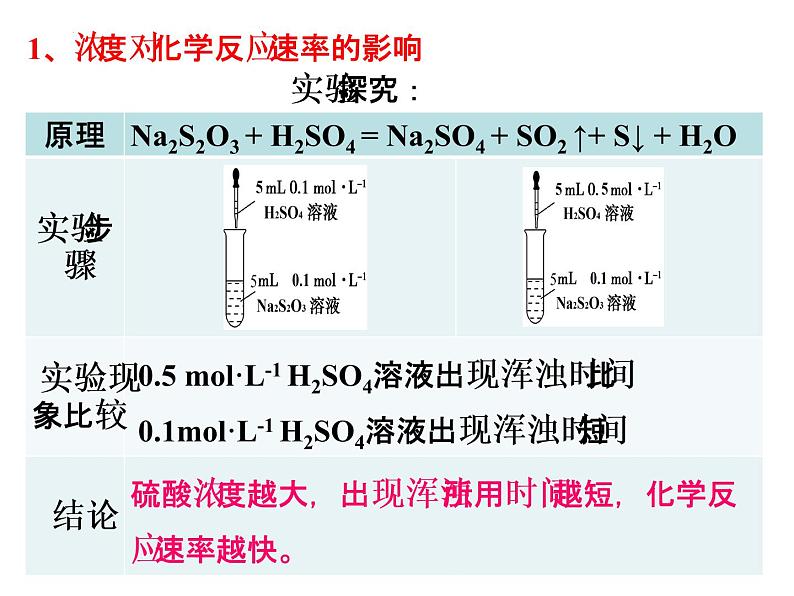
1、浓度对化学反应速率的影响
规律:当其它条件不变时, 增大反应物的浓度,可以提高化学反应速率; 减小反应物的浓度,可以降低化学反应速率。
注意事项:(1)固体和纯液体的浓度可视为常数,改变其物质的量,对反应速率无影响。(2)若某物质的浓度变化改变了其性质,反应实质可能发生改变,要具体分析反应速率的变化(如铁与稀硫酸反应,在一定浓度范围内反应速率与浓度有关,但常温下铁遇浓硫酸钝化)。(3)对于离子反应,只有实际参加反应的各离子浓度发生变化,才会引起化学反应速率的改变。
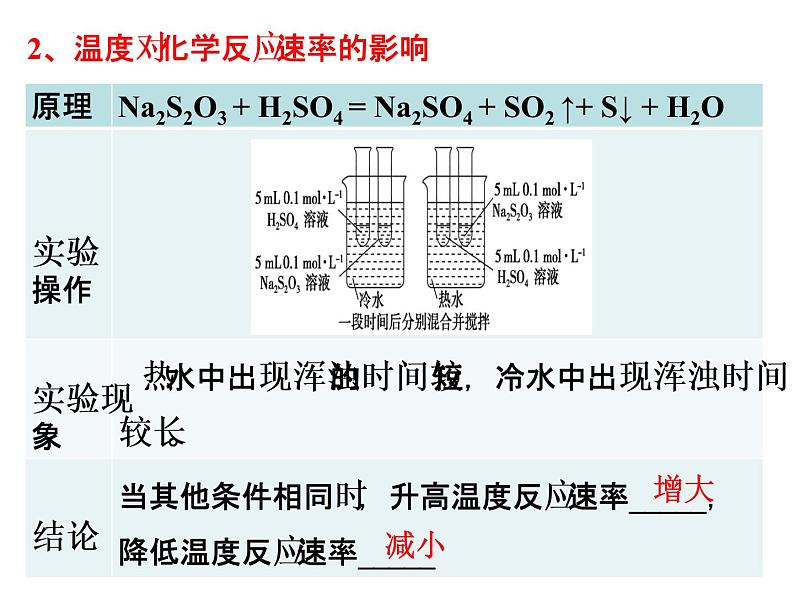
2、温度对化学反应速率的影响
规律:在其他条件不变时,升高温度反应速率增大,降低温度反应速率减小。
解释:一方面由于温度的升高使分子获得更高的能量,活化分子百分数提高;另一方面具有较高能量的分子之间碰撞频率也随之提高。从而使分子间有效碰撞的几率提高,反应速率加快。
注意: 在一般情况下,温度每升高10℃,化学反应速率增大到 2~4 倍。
3、催化剂对化学反应速率的影响
注意事项: (1)催化剂只能改变化学反应速率,不能改变反应方向,也不能改变反应热的大小。 (2)同一催化剂能同等程度地改变化学反应的正、逆反应速率。 (3)同一反应,用不同催化剂,反应速率不相同。正催化剂加快化学反应速率,负催化剂减慢化学反应速率(不说明指正催化剂)。
规律:加入催化剂可以加快(或减慢)反应的速率。
规律: 其他条件不变,增大压强,气体体积缩小,浓度增大,反应速率加快。
2、压强只对有气体参加的反应的速率有影响。
1、压强对于反应速率的影响是通过对浓度的影响实现的。
4、压强对化学反应速率的影响
对于气体反应体系有以下两种情况:
a. 充入气体反应物→总压增大→浓度增大→速率加快
b. 充入“惰性气体”→总压增大→反应物浓度不变→反应速率不变
b. 充入“惰性气体”→体积增大→各反应物浓度减小→反应速率减慢
a. 充入气体反应物→总压不变→浓度不变→速率不变
5、其他因素 光辐射、放射线辐射、超声波、电弧、强磁场、高速研磨等,总之向反应体系输入能量,都可能改变化学反应速率。
1.常温下,分别将四块形状相同、质量均为7 g的铁片同时放入下列四种溶液中,产生气体速率最快的是 ( ) A.150 mL 2 ml·L-1盐酸 B.500 mL 2ml·L-1 盐酸 C.50 mL 3 ml·L-1盐酸 D.50 mL 18.4 ml·L-1硫酸
2.一定条件下,对于反应:CaCO3(块状)+2HCl===CaCl2+CO2↑+H2O,为加快反应速率,下列方法可行的有 ( )①增加盐酸的浓度 ②增加同浓度盐酸的用量 ③加水 ④增加CaCO3(块状)的用量 ⑤将块状CaCO3改为粉末状CaCO3A.1项 B.2项 C.3项 D.4项
3.在C(s)+CO2(g)===2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强 ②增加碳的量 ③通入CO2 ④恒容下充入N2 ⑤恒压下充入N2能够使反应速率增大的措施是 ( )A.①④ B.②③⑤ C.①③ D.①②④4.通过缩小反应容器体积而增大压强对下列反应的速率无影响的是 ( )A.CO2(g)+Ca(OH)2===CaCO3↓+H2O B.H2(g)+I2(g) 2HI(g)C.NaCl+AgNO3===AgCl↓+NaNO3 D.N2(g)+3H2(g) 2NH3(g)
5.在恒温恒容的容器中发生N2O4(g) 2NO2(g),若反应物的浓度由0.1 ml·L-1降到0.06 ml·L-1需20 s,那么由0.06 ml·L-1降到0.036 ml·L-1,所需反应时间为 ( )A.10 s B.12 s C.大于12 s D.小于12 s
6.对反应A+B===AB来说,常温下按以下情况进行反应:①20 mL溶液中含A、B各0.01 ml ②50 mL溶液中含A、B各0.05 ml ③0.1 ml·L-1的A、B溶液各10 mL ④0.5 ml·L-1的A、B溶液各50 mL 四者反应速率的大小关系是 ( )A.②>①>④>③ B.④>③>②>① C.①>②>④>③ D.①>②>③>④
人教版 (2019)选择性必修1第一节 化学反应速率备课课件ppt: 这是一份人教版 (2019)选择性必修1第一节 化学反应速率备课课件ppt,共60页。PPT课件主要包含了目标素养,知识概览,自主预习,预习检测,实验方案等内容,欢迎下载使用。
化学选择性必修1第一节 化学反应速率课前预习课件ppt: 这是一份化学选择性必修1第一节 化学反应速率课前预习课件ppt,文件包含212pptx、213pptx、211pptx等3份课件配套教学资源,其中PPT共66页, 欢迎下载使用。
人教版 (2019)第一节 化学反应速率教课ppt课件: 这是一份人教版 (2019)第一节 化学反应速率教课ppt课件,文件包含选择性必修1第二章第一节第1课时化学反应速率-教学课件pptx、选择性必修1第二章第一节第1课时化学反应速率-教学设计docx、选择性必修1第二章第一节第1课时化学反应速率-学案docx、选择性必修1第二章第一节第1课时化学反应速率-作业设计docx等4份课件配套教学资源,其中PPT共20页, 欢迎下载使用。













