

【备战2023高考】化学考点全复习——3.1.2《钠的化合物》复习课件(新教材新高考)
展开Na2CO3>NaHCO3
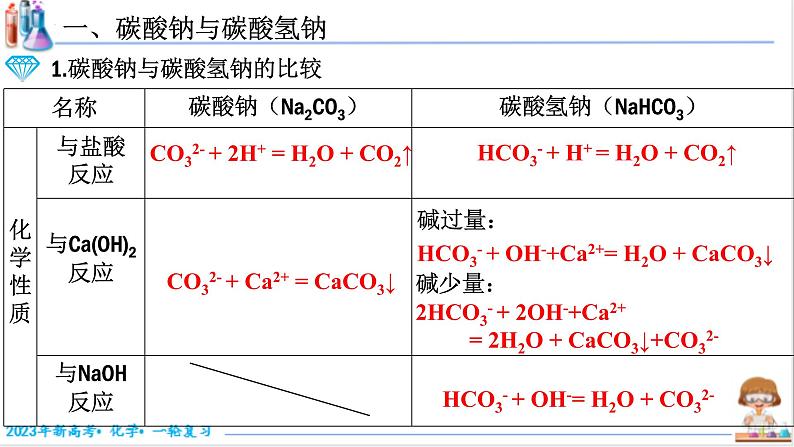
HCO3- + H+ = H2O + CO2↑
CO32- + 2H+ = H2O + CO2↑
CO32- + Ca2+ = CaCO3↓
HCO3- + OH-+Ca2+= H2O + CaCO3↓
2HCO3- + 2OH-+Ca2+ = 2H2O + CaCO3↓+CO32-
HCO3- + OH-= H2O + CO32-
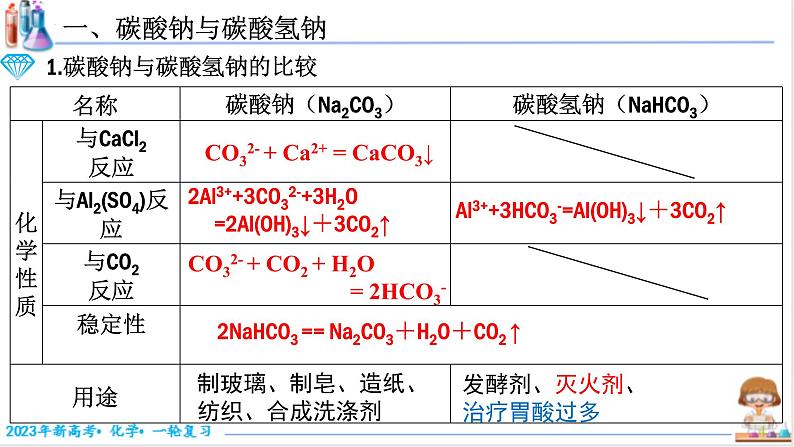
2Al3++3CO32-+3H2O =2Al(OH)3↓+3CO2↑
Al3++3HCO3-=Al(OH)3↓+3CO2↑
2NaHCO3 == Na2CO3+H2O+CO2 ↑
CO32- + CO2 + H2O = 2HCO3-
制玻璃、制皂、造纸、纺织、合成洗涤剂
发酵剂、灭火剂、治疗胃酸过多
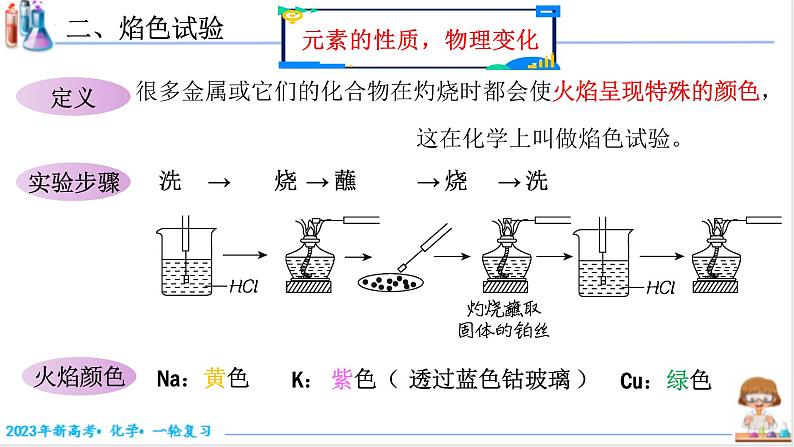
很多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色, 这在化学上叫做焰色试验。
洗 → 烧 → 蘸 → 烧 → 洗
K: 紫色( 透过蓝色钴玻璃 )
4Na+O2=2Na2O
2M+H2O=2MOH+H2↑
①碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠小。
②碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
③碱金属可与H2发生反应生成RH(R代表碱金属),RH属于离子化合物,氢元素显-1价,碱金属氢化物是强还原剂,如NaH+H2O══ NaOH+H2↑,NaH是还原剂,H2O是氧化剂,氧化产物是H2,还原产物也是H2。
一、碳酸钠与碳酸氢钠的鉴别与除杂
无明显变化的是Na2CO3
放出无色无味的使澄清石灰水变浑浊的气体是NaHCO3
产生气泡速率快的是NaHCO3
产生气泡速率慢的是Na2CO3
滴加盐酸立即产生气泡的是NaHCO3
滴加盐酸开始不产生气泡的是Na2CO3
产生白色沉淀的是Na2CO3
不产生白色沉淀的是NaHCO3
pH大的是Na2CO3
pH小的是NaHCO3
加入适量的NaOH溶液
例题:向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 ml·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )A.原NaOH溶液的浓度为0.2 ml·L-1B.通入CO2在标准状况下的体积为448 mLC.所得溶液中溶质物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3D.所得溶液中溶质物质的量之比为n(NaHCO3)∶n(Na2CO3)=1∶1
(1)用铂丝蘸取少量某溶液进行焰色试验,火焰呈黄色, 该溶液一定是钠盐溶液( )(2)用饱和NaHCO3溶液除去CO2中的SO2( )(3)分别向NaHCO3溶液和Na2CO3溶液中滴入Ba(OH)2溶液, 都产生白色沉淀( )(4)氯碱工业中发生主要反应的离子方程式:2Cl-+2H2O 2OH-+H2↑+Cl2↑( )
1.判断下列说法的正误(正确的画“√”,错误的画“×”)。
(5)实验室可用碳酸钠与氢氧化钙反应制取少量的氢氧化钠( )(6)金属钠着火时,可用干燥的沙土覆盖灭火( )(7)固体碳酸钠粉末中混有少量碳酸氢钠,可以用加热的方法将杂质除去( )(8)侯氏制碱法工业过程中应用了物质溶解度的差异( )(9)Na2CO3溶液呈碱性,可用于去除油污( )(10)钠和钾都可以保存在煤油中( )(11)用小苏打(NaHCO3)作焙制糕点的膨松剂( )(12)生活中常用苏打作发酵粉( )
2.侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,实验流程如图。回答下列问题:
(1) 从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是___________ (按气流方向,用小写字母表示)。为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或________________。
(2) B中使用雾化装置的优点是______________________________________ ___________________。(3) 生成NaHCO3的总反应的化学方程式为__________________________________________________。
增大CO2气体与氨盐水的接触面积,加快反应速率
NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl
(4) 反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14 g,则固体NaHCO3的质量为________g。②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)―→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为____________、____________、洗涤、干燥。
(5) 无水Na2CO3可作为基准物质标定盐酸浓度。称量前,若无水Na2CO3保存不当,吸收了一定量水分,用其标定盐酸浓度时,会使结果________(填标号)。偏高 B. 偏低 C. 不变
3.1.2 钠的化合物(课件帮)-备战2023年高考化学一轮复习考点帮(新教材新高考): 这是一份3.1.2 钠的化合物(课件帮)-备战2023年高考化学一轮复习考点帮(新教材新高考),共1页。
【备战2023高考】化学考点全复习——5.1.1《原子结构》复习课件(新教材新高考): 这是一份【备战2023高考】化学考点全复习——5.1.1《原子结构》复习课件(新教材新高考),共28页。PPT课件主要包含了知识梳理,原子的构成,原子核,中子N个不带电,原子的核外电子数,所带电荷数,+所带电荷数,元素化合价,离子所带电荷数,原子个数等内容,欢迎下载使用。
【备战2023高考】化学考点全复习——3.2.2《铁盐》复习课件(新教材新高考): 这是一份【备战2023高考】化学考点全复习——3.2.2《铁盐》复习课件(新教材新高考),共22页。PPT课件主要包含了知识梳理,亚铁盐,核心素养,浅绿色,产生红褐色絮状沉淀,棕黄色,加入氯水或H2O2,加过量铁粉后过滤,能力提升等内容,欢迎下载使用。