

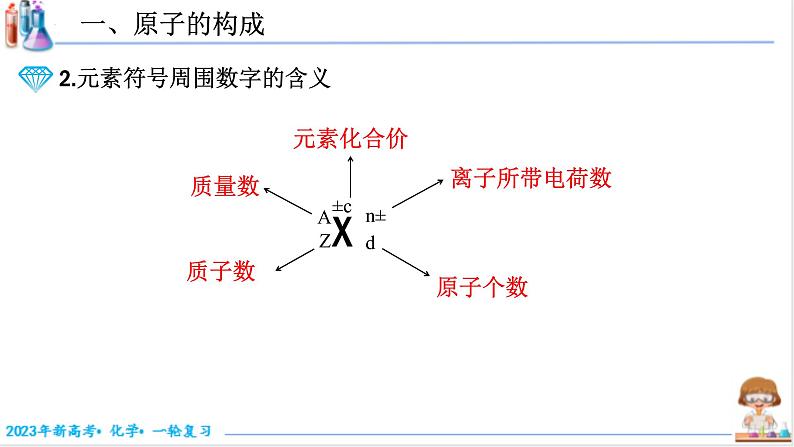


所属成套资源:(新教材新高考)备战2023高考 化学考点全 复习课件+复习精选题(含解析)
【备战2023高考】化学考点全复习——5.1.1《原子结构》复习课件(新教材新高考)
展开这是一份【备战2023高考】化学考点全复习——5.1.1《原子结构》复习课件(新教材新高考),共28页。PPT课件主要包含了知识梳理,原子的构成,原子核,中子N个不带电,原子的核外电子数,所带电荷数,+所带电荷数,元素化合价,离子所带电荷数,原子个数等内容,欢迎下载使用。
核外电子(Z个,带负电)
质子(Z个,带正电荷)
原子序数 = 核电荷数 = 质子数
原子序数:按照核电荷数由小到大给元素编号,得到的序号叫原子序数。
核电荷数:原子核所带的电荷数
阳离子的核外电子数=质子数
阴离子的核外电子数=质子数
原子的质量主要集中在原子核上,质子和中子的相对质量都近似为1,如果忽略电子的质量,将核内所有质子和中子的相对质量取近似值加起来,所得的数值叫做质量数。
质量数(A)= 质子数(Z)+ 中子数(N) A = Z + N
(1)任何粒子中,质量数=质子数+中子数,
但质子数与电子数不一定相等,如阴、阳离子中;
(2)有质子的粒子不一定有中子,如1H,
有质子的粒子不一定有电子,如H+;
(3)质子数相同的粒子不一定属于同一种元素,如F与OH-;
(4)核外电子数相同的粒子,其质子数不一定相同,
如Al3+和Na+、F-等,NH4+与OH-等。
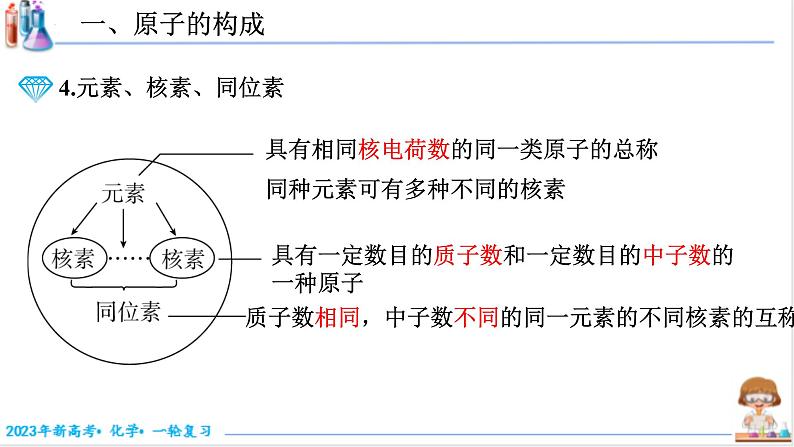
具有相同核电荷数的同一类原子的总称
同种元素可有多种不同的核素
具有一定数目的质子数和一定数目的中子数的一种原子
质子数相同,中子数不同的同一元素的不同核素的互称
(5)核变化不属于物理变化,也不属于化学变化。
(1)一种元素可以有多种核素,也可能只有一种核素
(2)有多少种核素就有多少种原子
(3)同位素:“位”即核素的位置相同,在元素周期表中占同一个位置
(4)不同的核素可能具有相同的质子数,如11H与13H;也可能具有相同的中子数,如 614C与 816O;也可能具有相同的质量数,如 614C与 714N;也可能质子数、中子数、质量数均不相同,如11H与 612C
②同一元素的各种核素的______不同,______相同,化学性质_____________,物理性质________。
①当某种元素具有多种天然、稳定的核素时,无论是游离态还是化合态,其各核素的________百分比一般是不变的。
①决定元素种类的是__________________。
②决定元素化学性质的是__________________。
③决定原子种类的是__________________。
④决定原子相对质量的是__________________。
核外电子数(最外层电子数)
二、常见“10e-”“18e-”微粒
(1)若10电子的微粒满足关系
(2)若10电子的微粒满足关系:
He、H-、Li+、Be2+、H2
—F、—OH、—NH2、—CH3
S、O2、C2H4、HCHO
三、“8电子稳定结构”的判断方法
(2)一般来说,在ABn型分子中, 若某元素原子最外层电子数+|化合价|=8, 则该元素原子的最外层满足8电子稳定结构。
(1)分子中的氢原子不满足8电子结构
如CO2分子中,碳元素的化合价为+4,碳原子最外层电子数为4,二者之和为8,则碳原子满足最外层8电子稳定结构,同理知氧原子也满足最外层8电子稳定结构。
若该原子达到所需成键数目,则为8电子结构
若未达到或超过所需成键数目则不为8电子结构,
如PCl5中的P,BeCl2中的Be
1.判断正误(正确的打“√”,错误的打“×”)。
(1)原子都是由质子、中子和电子组成的。( )(2)元素原子的多样性是由构成原子的质子数和中子数引起的。( )(3)质子数相同的粒子属于同种元素。( )(4)两种粒子的质子数和核外电子数分别相等,二者性质相同。( )(5)2964Cu原子核外有35个电子。( )(6)3 g 3He含有的中子数为1 NA。( )(7) 49115In的中子数与电子数的差值为17。( )(8)同种元素的原子均有相同的质子数和中子数。( )
2.判断正误(正确的打“√”,错误的打“×”)。
(1)H2、D2和T2互为同位素。( )(2)14C和14N的质量数相等,中子数不等。( )(3)16O与18O的相互转化为化学变化。( )(4)若两种粒子的质子数和核外电子数均相同,则它们可能是两种不同元素的原子和离子。( )(5)232Th转化成233U是化学变化。( )(6)中子数不同而质子数相同的粒子一定是同种元素的不同核素。( )(7)35Cl与37Cl的原子核外电子排布不同,得电子能力相同。( )
3.下列说法中,正确的是( )①16 8O与18 8O是不同的核素,因此分别由这两种原子构成的16 8O2与18 8O2化学性质不同 ②O2与O3互为同分异构体 ③C60与12C、14C互为同位素 ④科学家已发现了H3分子,H2与H3互为同素异形体⑤稀土元素144 62Sm与150 62Sm 的质量数不同,属于两种元素 ⑥H2O与D2O互称同素异形体 ⑦4822Ti和5022Ti质子数相同,互为同位素 ⑧1H2、2H2、3H2互为同位素A.④⑥ B.③⑦ C.②⑧ D.④⑦
4.“钚239”是氢弹的重要原料。下列有关说法正确的是( ) A.239Pu原子的原子核中含有239个质子B.238Pu、239Pu和241Pu属于不同的核素C.238Pu与238U在元素周期表中的位置相同D.239Pu衰变成235U属于化学变化
5.已知A、B、C、D分别是由短周期元素组成的四种微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒。请回答下列问题:
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:__________________。(2)若B、D属于同主族元素形成的单质分子,写出C的化学式:______。(3)若A、B均是含有2个原子核的微粒,且B中含有10个电子,D中含有18个电子,则A、B之间发生反应的离子方程式为_____________________。(4)若D是一种含有22电子的分子,则符合如图所示转化关系的A为____________(写出物质的化学式,如果是有机物则写出相应的结构简式)。
2F2+2H2O=4HF+O2
CH3CH3(或CH3OH)
HS-+OH-=S2-+H2O
相关课件
这是一份5.1.1 原子结构(课件帮)-备战2023年高考化学一轮复习考点帮(新教材新高考),共1页。
这是一份【备战2023高考】化学考点全复习——3.2.2《铁盐》复习课件(新教材新高考),共22页。PPT课件主要包含了知识梳理,亚铁盐,核心素养,浅绿色,产生红褐色絮状沉淀,棕黄色,加入氯水或H2O2,加过量铁粉后过滤,能力提升等内容,欢迎下载使用。
这是一份【备战2023高考】化学考点全复习——3.1.2《钠的化合物》复习课件(新教材新高考),共27页。PPT课件主要包含了知识梳理,碳酸钠与碳酸氢钠,纯碱或苏打,小苏打,白色粉末,白色晶体,碱过量,碱少量,焰色试验,Na黄色等内容,欢迎下载使用。