


所属成套资源:【高考引领教学】最新高考化学一轮针对性复习方案(全国通用)
第三节 化学平衡常数(考点考法剖析)-【高考引领教学】高考化学一轮针对性复习方案(全国通用)
展开
这是一份第三节 化学平衡常数(考点考法剖析)-【高考引领教学】高考化学一轮针对性复习方案(全国通用),文件包含第三节化学平衡常数考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用解析版docx、第三节化学平衡常数考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用原卷版docx等2份试卷配套教学资源,其中试卷共44页, 欢迎下载使用。
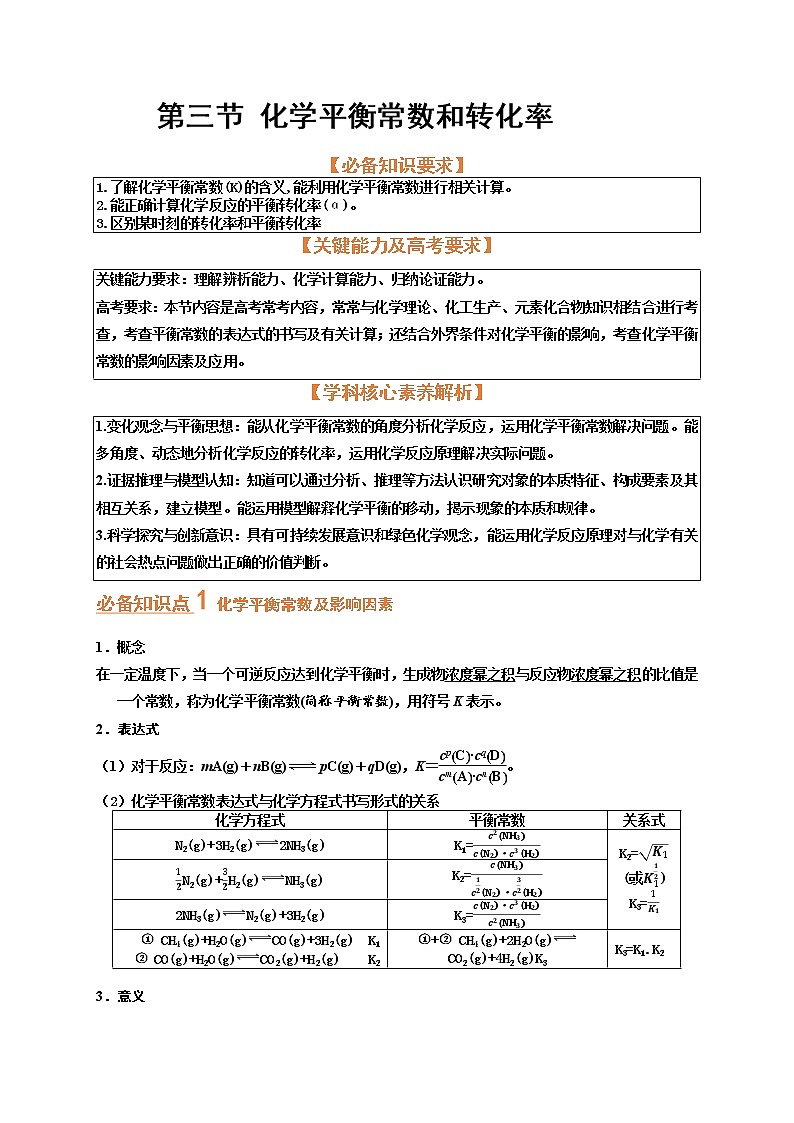
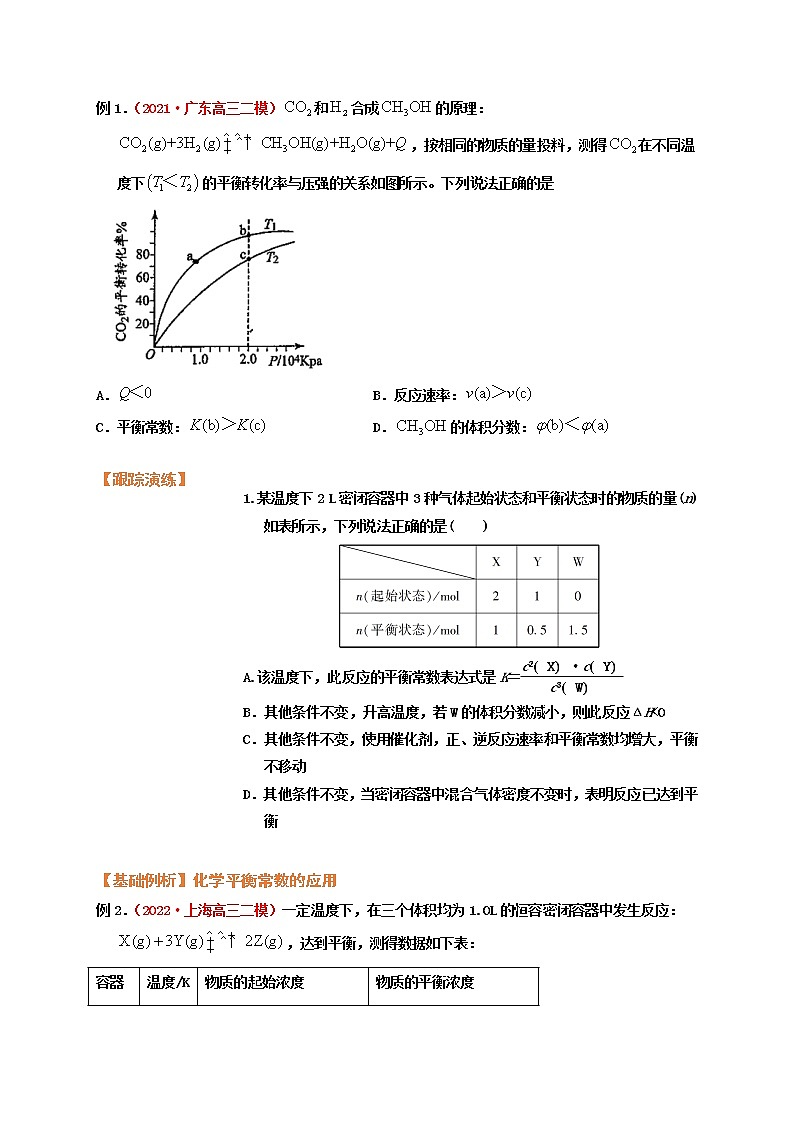
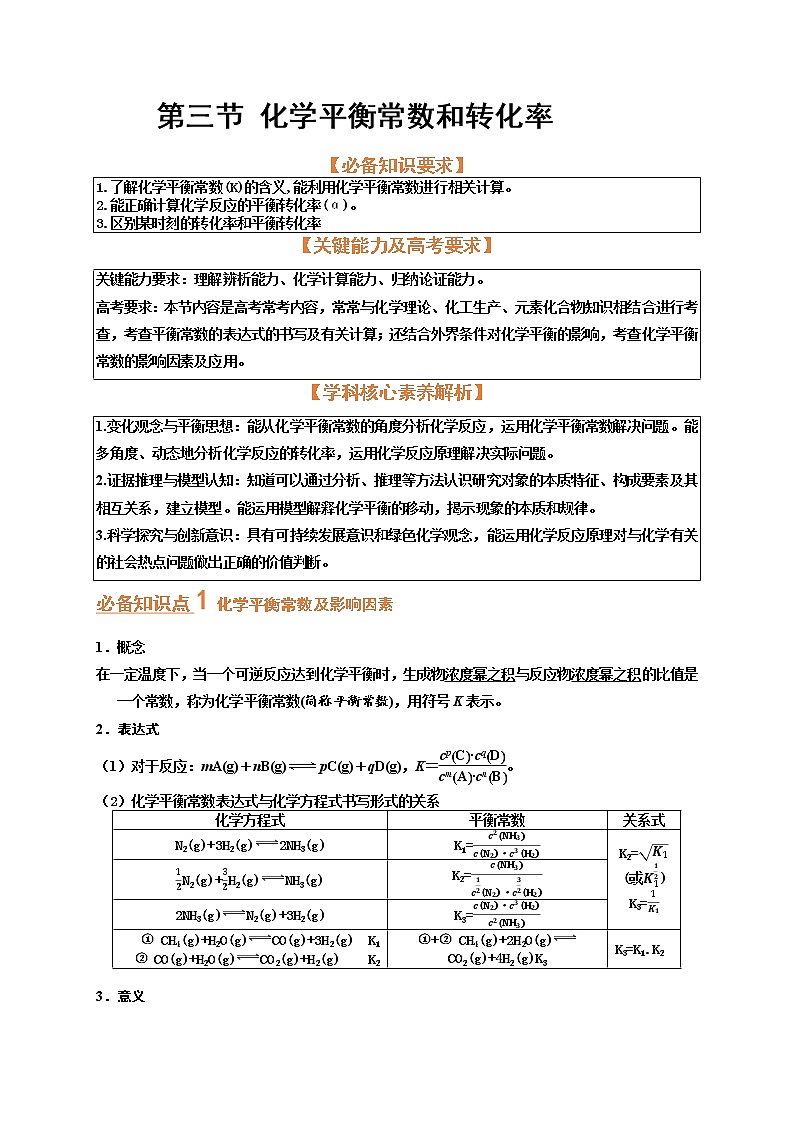
第三节 化学平衡常数和转化率
【必备知识要求】
1.了解化学平衡常数(K)的含义,能利用化学平衡常数进行相关计算。
2.能正确计算化学反应的平衡转化率(α)。
3.区别某时刻的转化率和平衡转化率
【关键能力及高考要求】
关键能力要求:理解辨析能力、化学计算能力、归纳论证能力。
高考要求:本节内容是高考常考内容,常常与化学理论、化工生产、元素化合物知识相结合进行考查,考查平衡常数的表达式的书写及有关计算;还结合外界条件对化学平衡的影响,考查化学平衡常数的影响因素及应用。
【学科核心素养解析】
1.变化观念与平衡思想:能从化学平衡常数的角度分析化学反应,运用化学平衡常数解决问题。能多角度、动态地分析化学反应的转化率,运用化学反应原理解决实际问题。
2.证据推理与模型认知:知道可以通过分析、推理等方法认识研究对象的本质特征、构成要素及其相互关系,建立模型。能运用模型解释化学平衡的移动,揭示现象的本质和规律。
3.科学探究与创新意识:具有可持续发展意识和绿色化学观念,能运用化学反应原理对与化学有关的社会热点问题做出正确的价值判断。
必备知识点1 化学平衡常数及影响因素
1.概念
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,称为化学平衡常数(简称平衡常数),用符号K表示。
2.表达式
(1)对于反应:mA(g)+nB(g)pC(g)+qD(g),K=。
(2)化学平衡常数表达式与化学方程式书写形式的关系
化学方程式
平衡常数
关系式
N2(g)+3H2(g)2NH3(g)
K1=c2(NH3)c(N2)·c3(H2)
K2=K1
(或K112)
K3=1K1
12N2(g)+32H2(g)NH3(g)
K2=c(NH3)c12(N2)·c32(H2)
2NH3(g)N2(g)+3H2(g)
K3=c(N2)·c3(H2)c2(NH3)
CH4(g)+H2O(g)CO(g)+3H2(g) K1
CO(g)+H2O(g)CO2(g)+H2(g) K2
+ CH4(g)+2H2O(g)CO2(g)+4H2(g)K3
K3=K1.K2
3.意义
平衡常数表明在一定条件下反应进行的程度。K越大,表示反应进行的程度越大。
4.影响因素
(1)内因:反应物本身的性质。
(2)外因:K只受温度的影响,与浓度、压强、催化剂等外界因素无关。
5.K值与可逆反应进行程度的关系
K
<10-5
10-5~105
>105
反应程度
很难进行
反应可逆
反应可接近完全
【知识理解提点】
1.固体物质和纯液体物质的浓度视为常数,通常不计入平衡常数表达式中。
2.代入平衡常数表达式中的浓度是平衡浓度。
3.化学平衡常数表达式与具体的化学方程式相对应,同一个化学反应,用不同的化学方程式表示时,其平衡常数表达式不同。
4.化学平衡常数的两大应用
(1)判断平衡移动的方向:
对于可逆反应:mA(g)+nB(g)pC(g)+qD(g),在任意状态下,生成物的浓度和反应物的浓度之间的关系用浓度商Q=表示,则:
(2)判断反应的热效应:若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
【惑点辨析】
判断正误(正确的打“√”,错误的打“×”)。
1.平衡常数发生变化,化学平衡不一定发生移动。( )
2.化学平衡发生移动,平衡常数不一定发生变化。( )
3.平衡常数表达式中,物质的浓度可以是任一时刻的浓度。 ( )
4.可逆反应2A(s)+B(g)2C(g)+3D(g)的平衡常数为K=c2(C)·c3(D)c2(A)·c(B)。( )
5.对于同一可逆反应,升高温度,则化学平衡常数增大。( )
6.增大反应物的浓度,平衡正向移动,化学平衡常数增大。( )
7.平衡常数和转化率都能体现可逆反应进行的程度。( )
8.对于反应:2SO2(g)+O2(g)2SO3(g),升高温度,K值减小,则ΔHS(s)。
2.反应能否自发进行需综合考虑焓变和熵变对反应的影响,复合判据ΔH-TΔS0、ΔS>0。( )
6.反应NH3(g)+HCl(g)NH4Cl(s)在室温下可自发进行,则该反应的ΔH”“”或
相关试卷
这是一份第三节 气体的制备(考点考法剖析)-【高考引领教学】高考化学一轮针对性复习方案(全国通用),文件包含第三节气体的制备考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用解析版docx、第三节气体的制备考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用原卷版docx等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。
这是一份专题解密(二) 化学计算(考点考法剖析)-【高考引领教学】高考化学一轮针对性复习方案(全国通用),文件包含专题解密二化学计算考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用解析版docx、专题解密二化学计算考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用原卷版docx等2份试卷配套教学资源,其中试卷共29页, 欢迎下载使用。
这是一份第三节 烃的含氧衍生物(考点考法剖析)-【高考引领教学】高考化学一轮针对性复习方案(全国通用),文件包含第三节烃的含氧衍生物考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用解析版docx、第三节烃的含氧衍生物考点考法剖析-高考引领教学高考化学一轮针对性复习方案全国通用原卷版docx等2份试卷配套教学资源,其中试卷共46页, 欢迎下载使用。








