




- 《认识有机化合物》第一课时课件PPT+教学设计 课件 70 次下载
- 《认识有机化合物》第二课时课件PPT+教学设计 课件 67 次下载
- 《乙烯与有机高分子材料》第二课时课件PPT+教学设计 课件 67 次下载
- 《乙醇与乙酸》第一课时课件PPT+教学设计 课件 70 次下载
- 《乙醇与乙酸》第二课时课件PPT+教学设计 课件 73 次下载
化学必修 第二册第二节 乙烯与有机高分子材料教学ppt课件
展开人教版高中化学必修二
《乙烯与有机高分子材料》第一课时 教学设计
课题名 | 《乙烯与有机高分子材料》第一课时 |
教学目标 | 1.掌握乙烯的结构、物理性质和化学性质。 2.通过对比烷烃和烯烃结构的不同理解乙烯的性质与碳碳双键密切相关。 3.了解乙烯的用途。 |
教学重点 | 乙烯的结构、物理性质和化学性质。 |
教学难点 | 乙烯的结构和化学性质。 |
教学准备 | 教师准备:PPT、实验 学生准备:预习课本 |
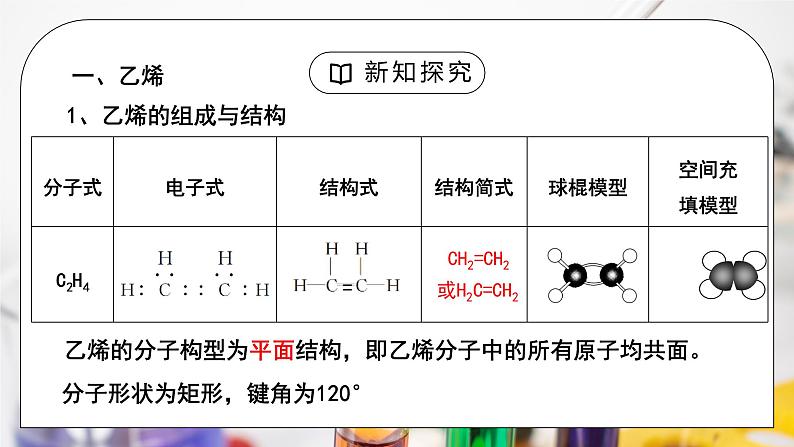
教学过程 | 新课导入 青香蕉和熟苹果放在同一个塑料袋里,系紧袋口,放置一段时间,你会发现青香蕉熟了。 这是谁的功劳? 乙烯的用途 乙烯产量是衡量一个国家石油化学工业的发展水平的重要标志。 新课讲授 一、乙烯 1、乙烯的组成与结构 乙烯的分子构型为平面结构,即乙烯分子中的所有原子均共面。 分子形状为矩形,键角为120° 结构特点:分子里有碳碳双键(其中含一个不稳定的共价键),键与键之间的夹角是120°,是平面型分子。 注意:① C=C中C原子不能绕键旋转(C—C可以) ② C=C不是两个C—C的简单组合 ③C=C中有一个键比较特殊,不稳定,比较活泼,键容易断裂。 2、乙烯(C2H4)的物理性质 思考:实验室收集乙烯气体,应该用什么方法收集? 排水集气法,不能用向下排空气法。 乙烯(CH2=CH2)的式量为28,空气的平均式量约为29,密度相差太近,分不开。 3.乙烯的化学性质 (1)氧化反应 ①在空气中燃烧 【实验7-2】(1)点燃纯净的乙烯,观察燃烧时的现象。 C2H4 + 3O2 2CO2 + 2H2O 现象: 火焰明亮,有黑烟产生,同时放出大量的热。 解释:含碳量高,燃烧不充分;火焰明亮是碳微粒受 灼热而发光。 思考:甲烷燃烧的实验现象? 应用:此法可用于鉴别CH4和C2H4 【实验7-2】(2)将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。 ②与酸性KMnO4溶液反应:乙烯能被酸性KMnO4 氧化,而使酸性KMnO4溶液褪色 。 思考:我们还可以用什么方法来鉴别甲烷和乙烯呢? 分别通入酸性高锰酸钾溶液中,不褪色的是 甲烷,褪色的是乙烯。 思考:能否用酸性KMnO4溶液除去混在甲烷中的乙烯气体呢? 注意:由于反应会生成CO2,所以不可以通过用酸性KMnO4溶液除去混在烷烃气体中的乙烯气体。 用酸性KMnO4溶液吸收后,通入NaOH溶液除去二氧化碳,再通入浓硫酸干燥。 【实验7-3】将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。 现象:溴的四氯化碳溶液褪色。 补充实验:把乙烯气体通入溴水中。 实验现象:溴水褪色,且反应后液体分层,下层为无色油状液体。 结论:乙烯可与溴反应 思考:乙烯和Br2是怎样反应的呢? (2)加成反应 定义:有机物分子中的不饱和碳原子(双键 或三键)与其他原子或原子团直接结合生成新的化合物的反应叫加成反应。 CH2=CH2+ Br2 CH2BrCH2Br 1,2-二溴乙烷 无色液体、不溶于水、密度比水大。 应用:(1)鉴别:乙烯与烷烃 (2)除杂:CH4(C2H4) (3)有机合成中制备卤代烃 思考:乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,哪一位同学正确呢?试设计实验验证。 方法:向反应后溶液中加AgNO3溶液或石蕊 现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;若发生加成反应,则无此现象。 小结:鉴别甲烷和乙烯的方法: (1)分别点燃两种气体,燃烧时有黑烟的是乙烯。 (2)分别通入酸性高锰酸钾溶液中,能使溶液褪色的是乙烯。 (3)分别通入溴的四氯化碳溶液或者溴水中,能使褪色的是乙烯。 除去甲烷中乙烯方法:将混合气体通入溴的四氯化碳溶液或者溴水中。 制取卤代烃方法:常用烯烃的加成而不用烷烃的取代 一定条件下,乙烯还可以与X2、H2、HX、H2O、等发生类似的反应请试着写出其反应的化学方程式。 比较烷烃取代反应与烯烃加成反应 (3)加聚反应 由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。聚合反应在有机高分子材料的生产中有着广泛的应用。乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。 聚乙烯无固定熔沸点,是混合物 高聚物:相对分子质量很大(大于10000)的高分子化合物(混合物) 链节:高聚物中最小的重复结构单元 —CH2— CH2— 单体:合成高分子的小分子 CH2= CH2 聚合度:链节的数目 n 烯烃: 1、定义:链烃分子里含有C=C碳碳双键的不饱和烃,称为烯烃。 2、单烯烃的通式:CnH2n(n≥2) 3、烯烃的化学性质—活泼 ①氧化反应 ②加成反应 ③加聚反应 课堂小结 |
布置作业 |
练习册上相应习题 |
板书设计 | 一、乙烯 1、乙烯的组成与结构 2、乙烯(C2H4)的物理性质 3.乙烯的化学性质 (1)氧化反应 ①在空气中燃烧 C2H4 + 3O2 2CO2 + 2H2O (2)加成反应 CH2=CH2+ Br2 CH2BrCH2Br (3)加聚反应 |
教学反思 |
本节课要求学生掌握乙烯的结构、物理性质和化学性质。重点是理解乙烯的性质与碳碳双键密切相关。教师应对比烷烃和烯烃结构上的不同,抓住碳碳双键的特点来讲解。
|
化学必修 第二册第二节 乙烯与有机高分子材料优秀ppt课件: 这是一份化学必修 第二册第二节 乙烯与有机高分子材料优秀ppt课件,共60页。PPT课件主要包含了尝试解答等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第二节 乙烯与有机高分子材料优质课件ppt: 这是一份高中化学人教版 (2019)必修 第二册第二节 乙烯与有机高分子材料优质课件ppt,共60页。PPT课件主要包含了第1课时乙烯,乙烯的组成和结构,乙烯的物理性质,乙烯的化学性质,微判断,尝试解答,微训练,烯烃的性质,问题探讨等内容,欢迎下载使用。
人教版 (2019)必修 第二册第二节 乙烯与有机高分子材料精品ppt课件: 这是一份人教版 (2019)必修 第二册第二节 乙烯与有机高分子材料精品ppt课件,共33页。PPT课件主要包含了科学史话,链状烃,环状烃,烃的分类,问题与讨论,有机高分子材料,4黏合剂和涂料,课堂练习等内容,欢迎下载使用。