


北京市北京市北交附高2022-2023学年高一上学期期中考试化学试题(Word版含答案)
展开北京交大附高 2022-2023 学年第一学期期中考试 高 一 化学
说明:本试卷共 8 页,共 100 分。考试时长 90 分钟。
可能用到的相对原子质量: H- 1 C- 12 N- 14 O- 16 Cl-35.5 Na-23 I- 127 Fe-56 第Ⅰ卷 (42 分)
选择题 (每小题只有一个选项符合题意,本题共 21 小题, 每小题 2 分, 共 42 分)
1. 我国酒文化源远流长,下列古法酿酒工艺中,以发生化学反应为主的过程是
2022.11
S-32
A. 酒曲捣碎 | B. 酒曲发酵 | C. 高温蒸馏 | D. 泉水勾兑 |
2.下列物质: ①纯碱②食盐水③浓盐酸④烧碱 ⑤液态氧⑥氯酸钾, 分类全部正确的是
A.碱——①④
C.混合物——②⑤
B.纯净物——③④⑤
D.盐——①⑥
3.KOH 是我国古代纺织业常用作漂洗的洗涤剂。古代制取 KOH 的流程如下:
上述流程中没有涉及的化学反应类型是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
4. 下列关于胶体的叙述中,不正确的是
A. 用半透膜除去氢氧化铁胶体中的Na+ 、 Cl −
B. 胶体中分散质粒子的直径在 1nm ~ 100nm 之间
C. 利用丁达尔效应可以区分溶液和胶体
D. 用滤纸能分离胶体和溶液
A.Al2 (SO4)3=2Al3++3SO42 ‐ B.NaHCO3 = Na+ + H+ + CO32 ‐
C.Ba(OH)2=Ba2+ + 2OH ‐ D.Na2CO3=2Na+ + CO32 ‐
6.有如下物质:①NaCl 溶液;②熔融 MgCl2 ;③CuSO4 固体;④NaOH 固体;⑤金属铜;⑥蔗糖。有关它们 的说法正确的是
A.属于非电解质的有①⑤⑥ B.不能导电的有③④⑥
C.属于电解质的有①②③④ D.属于混合物的有①②③⑥
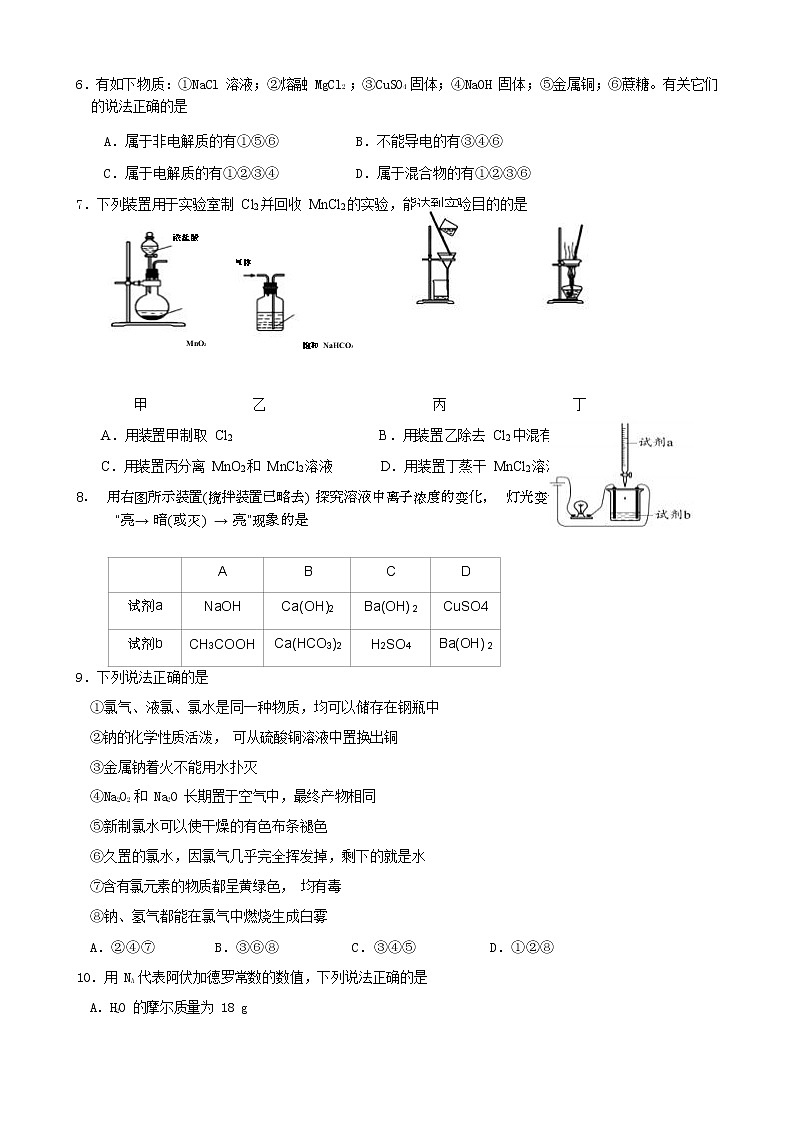
7.下列装置用于实验室制 Cl2 并回收 MnCl2 的实验,能达到实验目的的是
浓盐酸
气体
饱和 NaHCO3
甲 乙 丙 丁
A.用装置甲制取 Cl2 B.用装置乙除去 Cl2 中混有的少量 HCl
C.用装置丙分离 MnO2 和 MnCl2 溶液 D.用装置丁蒸干 MnCl2 溶液制得 MnCl2 •4H2O
8. 用右图所示装置(搅拌装置已略去) 探究溶液中离子浓度的变化, 灯光变化不可能 出现 “亮→ 暗(或灭) → 亮”现象的是
| A | B | C | D |
试剂a | NaOH | Ca(OH)2 | Ba(OH) 2 | CuSO4 |
试剂b | CH3COOH | Ca(HCO3)2 | H2SO4 | Ba(OH) 2 |
9.下列说法正确的是
①氯气、液氯、氯水是同一种物质,均可以储存在钢瓶中
②钠的化学性质活泼, 可从硫酸铜溶液中置换出铜
③金属钠着火不能用水扑灭
④Na2O2 和 Na2O 长期置于空气中,最终产物相同
⑤新制氯水可以使干燥的有色布条褪色
⑥久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
⑦含有氯元素的物质都呈黄绿色, 均有毒
⑧钠、氢气都能在氯气中燃烧生成白雾
A.②④⑦ B.③⑥⑧ C.③④⑤ D.①②⑧
10.用 NA 代表阿伏加德罗常数的数值,下列说法正确的是
A.H2O 的摩尔质量为 18 g
B.28gN2 和 CO 的混合气体中所含分子数是 NA
C.含有 NA 个氦原子的氦气在标准状况下的体积为 11.2L
D.0.5mol•L-1 的 NaCl 溶液中 Cl- 的个数为 0.5NA
11. M 与 N 反应时,不能实现图示电子转移的是
选项 | M | N | 电子转移 |
A | 铁粉 | O2 | -
M N |
B | Cl2 | H2O | |
C | 铝片 | Cu (NO3 ) 2 | |
D | Na2S | O2 |
12.下列溶液的物质的量浓度的相关计算正确的是
A.同浓度的三种物质的溶液:Na2 SO4 、MgSO4 、Al2(SO4)3 、溶液体积之比为 3 ∶2 ∶ 1 , 则 SO
B.将 1mol ·L- 1 的 NaCl 溶液和 0.5mol ·L- 1 的 BaCl2 溶液等体积混合后, 忽略溶液体积变化 (Cl-)=0.75mol ·L- 1
C.将 100mL 5mol ·L- 1 的盐酸加水稀释至 1L,再取出 5mL,这 5mL 溶液的物质的量浓度为 0.5 mol ·L- 1
D .标准状况下, 22.4 LHCl 溶于 1L 水, 盐酸的物质的量浓度为 1mol ·L- 1
13.下列离子方程式正确的是
A.盐酸滴在铜片上:Cu + 2H+ === Cu2+ + H2 ↑
B.铜片插入硝酸银溶液中:Cu + Ag+ === Cu2+ + Ag
C.Na2SO4 溶液和 Ba (OH) 2 溶液混合: SO42 - + Ba2+ === BaSO4 ↓
D.醋酸滴在大理石上: 2H+ + CaCO3 === Ca2+ + CO2 ↑+ H2O
粗食盐水中常含有少量 Ca2+ 、Mg2+ 、SO
固体 |
食盐 |
14 .过程 I 中, 不需要使用的实验仪器是
A .酒精灯 B.玻璃棒 C.漏斗 D.烧杯
15.关于实验过程中所选用的试剂、目的及所发生反应的离子方程式均正确的是
选项 | 试剂 | 目的 | 离子方程式 |
A | KOH 溶液 | 仅除去 Mg2+ | Mg2++2OH- ====Mg(OH)2 ↓ |
B | BaCl2 溶液 | 仅除去 4 | Ba2++Na2 SO4 ====BaSO4 ↓+2Na+ |
C | Na2CO3 溶液 | 仅除去 Ca2+ | Ca2++CO |
D | 盐酸 | 除去 OH-和 CO | H++OH-====H2O 2H++CO |
16.过程 III 中,用到的分离方法是
A.吸附 B .加热蒸发 C.过滤 D.冷却结晶
17.R2O7n –与 S2- 能在酸性溶液中发生反应:R2O7n− + 3 S2-+ 14H+ === 2R3+ + 3S ↓+ 7H2O,R2O7n−中 R 化合价为
A.+ 4 B.+ 5 C.+ 6 D.+ 7
18.在一个氧化还原反应体系中,反应物、生成物共有六种粒子: Fe3+、NO
A.该反应说明 Fe(NO3)2 溶液不宜加酸酸化
B.该反应中氧化剂与还原剂的个数之比为 8∶1 C.若有 1 个 NO
19.某溶液中仅含有 Na+、Mg2+ 、SO42-、Cl- 四种离子(不考虑水电离出的 H+和 OH- ),其物质的量浓度之 比为 c (Na+ ) ∶c (Mg2+ ) ∶c (Cl- )=5∶7∶7。若 c (Na+ )为 5 mol/L,则 c (SO42- )为
A.5 mol/L B.6mol/L C.7mol/L D.8mol/L
20.下列实验操作、现象和结论均正确, 且存在因果关系的正确的是
选项 | 实验操作 | 现象 | 结论 |
① |
将干燥纯净的氯气依次通过干燥的有色布条和湿 润的有色布条 |
只有湿润的有色布条 褪色 | 干燥的氯气没有漂 白性,湿润的氯气 有漂白性 |
② | 用坩埚钳夹住一束铁丝, 放入充满氯气的集气瓶 中 | 剧烈燃烧, 产生红棕 色烟 | 氯气与铁反应生成 氯化铁 |
③ | 向 Na2O2 的水溶液中滴入酚酞 | 溶液先变红色后褪色 | 反应生成 O2 |
④ |
向培养皿中加入适量水, 滴入 1~2 滴酚酞溶液, 取一块绿豆粒大小的金属钠放入水中 | 剧烈反应, 有气体产 生,溶液颜色由无色 变为红色 |
钠与水反应产生碱 性物质 |
A.①② B. ③④ C.①③ D. ①④
21. 研究小组探究 Na2O2 与水的反应。取 1.56 g Na2O2 粉末加入到 40 mL 水中,充分反应得溶液 A (溶液 体积几乎无变化),进行以下实验。
酚酞溶液
实验 ⅱ
先变红,20 s 后褪色
酚酞溶液
无气泡后
过滤
实验 ⅲ 实验ⅳ 实验 ⅴ
产生大量能使 溶液变为红色, 溶液变为红色
带火星木条复 10 min 后褪色
燃的气体
下列说法中,不正确的是
A .由实验ⅲ中现象可知, Na2O2 与 H2O 反应有 H2O2 生成
B.由实验ⅱ、ⅲ、ⅳ可知,实验ⅱ中溶液褪色与 H2O2 有关
C.由实验ⅳ、ⅴ可知,实验ⅳ中溶液褪色的原因是 c(OH-)大
D .向实验ⅱ褪色后的溶液中滴加盐酸, 溶液最终变为红色
第Ⅱ卷 (共 58 分)
22.(10 分) I 阅读下面两条科普信息,回答问题:
科普 I: 一个体重 50Kg 的健康人含铁 2g,这 2g 铁在人体中不是以单质金属的形式存在,而是以 Fe2+ 和 Fe3+ 的形式存在。亚铁离子易被吸收, 给贫血者补充铁时, 应给予含亚铁离子的亚铁盐, 如硫酸 亚铁。服用维生素 C ,可使食物中的铁离子还原成亚铁离子, 有利于铁的吸收。
科普 II: 在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它 们的皮鞘(可以用 Fe2O3 来表示其中的铁),后来便沉积下来形成铁矿;该反应的另一种反应物是 CO2 ,反应后 CO2 转变成有机物(用甲醛:CH2O 表示,其中氢为+1价,氧为-2 价)。
问题: 这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物) 相互转化的事实、方法和途径。
(1) 这说明亚铁离子具有 性,铁离子具有 性;(填“氧化”或“还原”,下同)
(2) 科普 I 中的维生素 C 是 剂;
科普 II 中的 CO2 剂, 写出科普 II 中的离子方程式 。
II、A-E 五种物质都含有钠元素,它们之间的转化关系如图所示(反应条件、部分反应物及生成物 省略),其中 A 为淡黄色固体化合物、 B 为单质、C 为一种强碱。
写出下列化学方程式
① B→ C
② A→C
③ B→E
④ B→A
23.(6 分)某无色透明溶液中可能存在大量阳离子 Ag+ 、 Mg2+ 、 Cu2+中的一种或几种,请填写下列.
(1) 不用做任何实验就可以肯定溶液中不存在的离子是____________.
(2) 取少量原溶液,加入过量稀盐酸,有白色沉淀生成, 再加入过量稀硝酸,沉淀不消失, 说明原溶液
.
(3) 取(2)的滤液加过量的 NaOH 溶液,出现白色沉淀, 说明原溶液中肯定存在某离子,加过量 NaOH 溶液时发生所有反应的离子方程式为:________________、________________________.
(4) 原溶液中可能大量存在的阴离子是____________ (填序号).
A.Cl- B.NO3- C.CO32- D.SO42-
24.(9 分) 要配制 480mL 0.2mol ·L-1 的 FeSO4 溶液,配制过程中有如下操作步骤:
①把称量好的绿矾(FeSO4 ·7H2O)放入小烧杯中, 加适量蒸馏水溶解;
②把①所得溶液小心转入___________中;
③继续向容量瓶中加蒸馏水至液面距离刻度 l~2cm 处,改用_______滴加蒸馏水至液面与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒 2~3 次, 每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,反复上下颠倒,摇匀; ⑥待溶液恢复到室温。
请填写下列空白:
(1) 完成实验操作②_ _____,③_ _
(2) 实验操作步骤的正确顺序为(填序号) _______,完成此配制实验。
(3) 实验室用绿矾(FeSO4 ·7H2O)来配制该溶液, 用托盘天平称量绿矾___________g。
(4) 由于错误操作,使得实际浓度比所要求的偏小的是___________ (填写编号)。
A. 把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
B.使用容量瓶配制溶液时,俯视液面定容,
C.没有用蒸馏水洗烧杯 2~3 次,并将洗液移入容量瓶中
D.容量瓶刚用蒸馏水洗净,没有干燥
E.定容时,滴加蒸馏水,先使液面略高于刻度线, 再吸出少量水使液面凹面与刻度线相切
(5) 定容时, 若加蒸馏水时不慎超过刻度线, 处理方法是___________
25. (12 分) 自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。
常用的自来水消毒剂有氯气、二氧化氯(ClO2 )和高铁酸钾(K2FeO4 ) 氯气等。
(1) 将氯气通入水中制得氯水,发生反应的离子方程式是
(2) 某研究小组用下图装置制备少量 ClO2 (夹持装置已略去)。
资料:ClO2 常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,11℃
时液化成红棕色液体。 以 NaClO3 和 HCl 的乙醇溶液为原料制备 ClO2 的 反应为 2NaClO3 + 4HCl==== 2ClO2 ↑+ Cl2 ↑+ NaCl + 2H2O。
冰水浴的作用是 。
(3) ClO2 在杀菌消毒过程中会产生副产物亚氯酸盐(ClO2- ),需将其转化为 Cl-除 去。下列试剂中,可将 ClO2-转化为 Cl- 的是 (填字母序号)。
a. FeSO4 b. O3 c. KMnO4 d. SO2
(4) 氯气与石灰乳制备漂白粉的化学方程式为
(5) K2FeO4 是一种新型、绿色的多功能净水剂,集氧化、吸附、絮凝、沉淀、灭菌、 消毒、脱色、除臭等性能为一体。实验室制备 K2FeO4 的方法如下:
在冰水浴中,向 KClO 和 KOH 的混合溶液中少量多次加入硝酸铁,并不断搅拌, 反应后的溶液中检验出氯离子。
①高铁酸钾的电离方程式是____________ __ _____
②上述制备 K2FeO4 反应的离子方程式为 。
26. (9 分) 某小组同学用图 1 装置研究去除 Cl2 的方法, 并探究不锈钢制的注射器针头 出现异常现象的原因。
I .研究去除 Cl2 的方法
试剂X 不锈钢针头 Cl2 图 1 | 实验 序号 | 注射器中试剂 X | 实验现象 | |
瓶内液面上方 | 3 分钟时不锈钢针头 | |||
i | 2 mL NaOH 溶液 | 无色 | 无明显变化 | |
ii | 2 mL 水 | 黄绿色略变浅 | 表面附着黄色物质 | |
(1) 实验 i 说明 NaOH 溶液可以吸收 Cl2 ,用离子方程式解释原理: 。
(2) 取实验 ii 中针头表面黄色物质, 加水溶解,滴加少量 NaOH 溶液,观察到 , 证明针头中 Fe 被氧化为 Fe3+。
II .探究不锈钢针头出现黄色物质的原因 小组同学提出了如下 3 种假设。
假设 1:Fe 被干燥的 Cl2 氧化为 Fe3+;
假设 2:Fe 被氯水中的HClO 氧化为 Fe3+;
假设 3:Fe 被氯水中的 H+ 氧化为 Fe2+ , 。
(3) 补全假设 3 : 。
(4) 小组同学用图 1 装置进行实验 iii 证明假设 1 不成立。实验 iii 的操作及现象为 。
(5) 小组同学进行实验 iv,验证假设 2 和假设 3。
实验 iv :分别向 pH 相同的盐酸和氯水中加入足量的铁粉,记录反应过程中溶液 pH 的变化,、 如图 2 所示。
已知: pH 相同的溶液中, c(H+)相同; pH 越大,c(H+)越小。
① 补全假设 2 中反应的离子方程式:
1 Fe +1 HClO +1 ==== 1 +1 +1 。
② 根据图 2 数据推测假设 2 可能成立, 理由是 。
27. (12 分) KMnO4 在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
Ⅰ .将软锰矿(主要成分 MnO2 ) 粉碎后, 与 KOH 固体混合,通入空气充分焙烧,生成暗绿色熔融物。
Ⅱ .冷却, 将固体研细, 用稀 KOH 溶液浸取, 过滤,得暗绿色溶液。
Ⅲ .向暗绿色溶液中通入 CO2 ,溶液变为紫红色, 同时生成黑色固体。
Ⅳ .过滤, 将紫红色溶液蒸发浓缩, 冷却结晶,过滤,洗涤, 干燥,得 KMnO4 固体。
资料:K2MnO4 为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应 (Mn 的化 合价既升高又降低)。
(1) Ⅰ 中,软锰矿(主要成分 MnO2 ) 提纯后可用于实验室制取氯气,反应的离子方程式为:
。
(2)Ⅰ 中,生成 K2MnO4 的化学方程式是 。
(3) Ⅱ中,浸取时用稀 KOH 溶液的原因是 。
(4) Ⅲ中,CO2 和 K2MnO4 在溶液中反应的化学方程式是 。
(5)将 K2MnO4 溶液采用惰性电极隔膜法电解, 也可制得 KMnO4 。装置如下图:
a 极发生 (填“氧化”或“还原”) 反应;
判断依据是: 。
(6) 用滴定法测定某高锰酸钾产品的纯度,步骤如下: 已知: Na2C2O4 + H2SO4 == H2C2O4 + Na2SO4
5H2C2O4 + 2MnO4 −+ 6H+ == 2Mn2+ + 10CO2 ↑+ 8H2O
摩尔质量:Na2C2O4 134 g ·mol− 1 KMnO4 158 g ·mol− 1 Mn2+颜色为肉粉色
ⅰ .称取 a g 产品,配成 50 mL 溶液。
ⅱ .称取 bg Na2C2O4 ,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。
ⅲ .将锥形瓶中溶液加热到 75℃~80℃,恒温, 用 ⅰ 中所配溶液滴定至 (填现象), 消耗溶液 VmL (杂质不参与反应)。 则产品中 KMnO4 的质量分数的表达式为: 。
北京市北交附高2023-2024学年高三上学期12月月考化学试题含答案: 这是一份北京市北交附高2023-2024学年高三上学期12月月考化学试题含答案,共17页。试卷主要包含了5 Ag1 08, 下列图示正确的是, 下列性质的比较,不正确的是, 氧化铈是应用广泛的稀土氧化物等内容,欢迎下载使用。
北京市首师附高2023-2024学年高一上学期10月适应性考试化学试题(扫描版含答案): 这是一份北京市首师附高2023-2024学年高一上学期10月适应性考试化学试题(扫描版含答案),共7页。
北京市首师附高2022-2023学年高二下学期期中练习化学试题(Word版含答案): 这是一份北京市首师附高2022-2023学年高二下学期期中练习化学试题(Word版含答案),共14页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。












