

湖北省宜城一中、枣阳一中等六校联考2022-2023学年高三化学上学期期中考试试题(Word版附答案)
展开湖北省宜城一中、枣阳一中等六校联考2022-2023学年
高三上学期期中考试化学试题
时限:75(分钟) 分值:100(分)
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写在试卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷、草稿纸和答题卡上的非答题区域均无效。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5 Fe 56
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 湖北是“千湖之省”,“鱼米之乡”,历史悠久,人杰地灵,物产丰富。下列说法错误的是
A. 神农架盛产的中草药中常含有苷类、生物碱、有机酸等成分,煎煮中草药不适宜用铁锅
B. 湖北博物馆镇馆之宝元青花瓷器“四爱图梅瓶”,其主要成分是二氧化硅
C. 潜江小龙虾烹饪时,虾壳变红的过程中发生了化学变化
D. 三峡脐橙富含多种氨基酸、维生素和微量元素,其中维生素C具有还原性
2. 化学用语是学习化学的重要工具,下列化学用语正确的是
A. 的结构式:
B. 的电子式:
C. 的空间填充模型:
D. 的离子结构示意图:
3. 化学与科技、生产、环境密切相关。下列说法错误的是
A. “燃煤脱硫”技术有利于我国早日实现“碳达峰、碳中和”
B. “天宫二号”空间站所用太阳能电池材料砷化镓属于新型无机非金属材料
C. “中国奋斗者号”载人潜水器的钛合金比纯金属钛具有更高的硬度
D. “天问一号”火星车的热控保温材料—纳米气凝胶,可产生丁达尔现象
4. 下列除杂过程中,所选用的试剂和操作方法正确的是
选项 | 物质 | 杂质(少量) | 试剂和操作方法 |
A | 固体 | 加热 | |
B | 溶液 | 加入过量的铜粉后过滤 | |
C | 固体 | 置于硬质玻璃管中充分加热 | |
D | 二氧化硫气体 | 氯化氢气体 | 通过饱和溶液,洗气 |
A. A B. B C. C D. D
5. 化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是
A. 定性检验溶液中是否含有时,先用稀硝酸酸化,再向所得溶液中加溶液
B. 为提高溶液的氧化能力,用盐酸将溶液酸化
C. 配制溶液时,为了抑制的水解可用稀硝酸酸化
D. 检验溴乙烷中的溴元素时,先用溶液与其混合加热,再用稀硝酸酸化,然后再滴加硝酸银溶液
6. 为阿伏加德罗常数的值。下列说法正确的是
A. 0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数小于
B. 标准状况下,11.2L甲烷和乙烯的混合气体中含氢原子数目为
C. 被完全还原为Fe时转移电子数为
D. 9.2g乙醇中含极性共价键的数目为
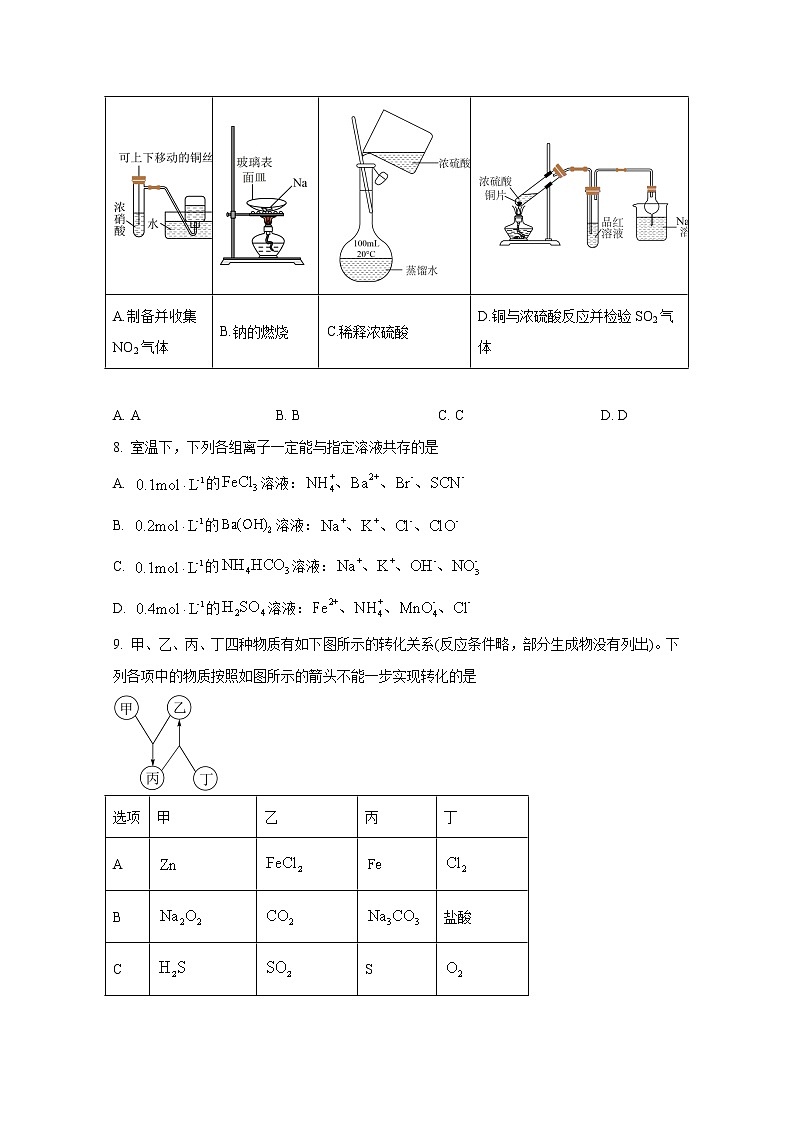
7. 下列实验操作或装置(部分夹持装置略)正确的是
A.制备并收集NO2气体 | B.钠的燃烧 | C.稀释浓硫酸 | D.铜与浓硫酸反应并检验SO2气体 |
A. A B. B C. C D. D
8. 室温下,下列各组离子一定能与指定溶液共存的是
A. 的溶液:
B. 的溶液:
C. 的溶液:
D. 的溶液:
9. 甲、乙、丙、丁四种物质有如下图所示的转化关系(反应条件略,部分生成物没有列出)。下列各项中的物质按照如图所示的箭头不能一步实现转化的是
选项 | 甲 | 乙 | 丙 | 丁 |
A | ||||
B | 盐酸 | |||
C | S | |||
D | 溶液 | 溶液 | 溶液 |
A. A B. B C. C D. D
10. 宏观辨识与微观探析是化学学科核心素养之一、下列物质性质实验对应的反应的离子方程式书写正确的是
A. 溶液与硝酸溶液混合:
B. 向烧碱溶液中加入一小段铝片:
C. 向溶液中加入足量的氨水:
D. 和在碱性条件下反应制备:
11. 1943年我国化学工程专家侯德榜发明了侯氏制碱法,又称联合制碱法,为我国化工事业的发展做出了卓越贡献。其部分工艺流程如下,下列说法错误的是
沉淀池中发生反应的化学方程式为
A. 该工艺利用了不同物质溶解度的差异
B. 该工艺能将原料氯化钠的利用率从70%提高到90%以上,主要是设计了循环I
C. 沉淀池中先通入足量的,再通入
D. 该工艺提取的副产品为,可用于化肥工业
12. 根据下列实验操作和现象能得到相应结论的是
| 实验操作 | 实验现象 | 实验结论 |
A | 往含有淀粉的溶液中滴加几滴HI溶液 | 溶液变蓝 | 氧化性: |
B | 将炽热的木炭加到浓硝酸中 | 有红棕色气体产生 | 加热条件下,浓硝酸被木炭还原成 |
C | 向某溶液中加入足量溶液,出现白色沉淀;再加入足量稀盐酸 | 部分沉淀溶解 | 该溶液中的部分已经变质 |
D | 向溶有的溶液中通入气体X | 有白色沉淀生成 | 气体X具有较强的氧化性 |
A. A B. B C. C D. D
13. 一种新型医用麻醉剂的分子结构式如图所示。X元素在所有元素中原子半径最小,元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素R的原子比W原子多8个电子。下列说法正确的是
A. XRZ是一种强酸
B. 最简单氢化物的稳定性:
C. 最高化合价:
D. 该麻醉剂分子中所有原子都满足8电子稳定结构
14. 标准电极电势可用来比较对应氧化剂的氧化性强弱。现有5组标准电极电势数据如下:
氧化还原电对氧化型/还原型 | 电极反应式氧化型还原型 | 电极电势 |
下列分析错误的是
A. 标准电极电势越大,对应氧化剂的氧化性越强
B. 还原性:
C. 向氯化亚铁溶液中加少量可观察到黄绿色气体生成
D. 与酸性溶液反应的离子方程式:
15. 碳酸锰 (MnCO3)是制造电信器材软磁铁氧体,合成二氧化锰和制造其他锰盐的原料。利用软锰矿(主要成分是,含有少量的等)制备碳酸锰的工艺流程如下。下列说法错误的是
A. “浸取”时发生反应的离子方程式为
B. “转化”的主要目的是将滤液中的氧化为,以便后续操作除去
C. 滤渣2的主要成分为
D. 该工艺流程中没有气体放出
二、非选择题:本题共4小题,共55分。
16. 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸 (CH3COOOH)、氯仿等均可有效灭活病毒。其中含氯消毒剂在抗疫防疫中发挥了重要的作用。
84消毒液 有效成分NaClO 质量分数25% 密度 规格1000mL 使用方式稀释100倍(体积比)之后使用 |
(1)“84消毒液”是常用的消毒剂,防疫物资中的一瓶“84消毒液”部分标签如图所示。
①上述“84消毒液”的物质的量浓度为_______。某同学取该“84消毒液”,稀释100倍后用于消毒,稀释后溶液中_______。
②该同学参阅上述“84消毒液”配方,用固体配制质量分数为的消毒液,下列仪器中不需要使用的有_______(写仪器名称)。
③“84消毒液”不可与酸性清洁剂混用的原因是_______(用离子方程式表示)。
(2)二氧化氯 (ClO2)是国际上公认的最新一代广谱、高效、安全、环保的杀菌消毒剂,因其稳定性差,常制备成固体以便运输和贮存。其工艺流程示意图如下图所示:
已知:浓度较大时易分解爆炸,一般用稀有气体或空气稀释到以下;饱和溶液在温度低于时析出的晶体是,高于时析出的晶体是,高于时分解成和。
①步骤1中通入空气的作用是_______。步骤2中发生反应的化学方程式为_______。
②步骤3中从溶液中获得晶体的操作步骤为:(Ⅰ)减压,蒸发结晶;(Ⅱ)趁热过滤;(Ⅲ)温水洗涤;(Ⅳ)低于干燥,得到成品。其中第(Ⅲ)步洗涤时水的温度范围为_______。
17. 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。
回答下列问题:
(1)写出物质R的电子式。_______。
(2)下列有关图中所示含N、S物质的叙述,正确的是_______(填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是_______。
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析,晶体中所含化学键的类型有_______,水溶液显_______(填“酸性”、“碱性”或“中性”)。
(5)(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入的溶液中,可制得该物质:,上述反应中,物质R体现的性质有_______,该反应每生成转移电子_______。其中被氧化的元素是_______(填元素符号)。
18. 三氯氧磷(POCl3)和氯化亚砜(SOCl2)都是重要的化工原料,三氯氧磷常作为半导体掺杂剂及光导纤维原料,氯化亚砜可用于农药、医药、染料等的生产。在实验室利用在时反应联合制备和:。所用实验装置和相关物质的性质的如下图所示(气体制备装置、夹持、加热及搅拌装置略):
相关性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
76.1 | 遇水强烈水解,易与反应 | ||
1.25 | 105.8 | 遇水强烈水解,能溶于 | |
78.8 | 遇水强烈水解,受热易分解 |
回答下列问题:
(1)氯气可由二氧化锰与浓盐酸反应制备,该反应的离子方程式为_______。
(2)装置A中的试剂是_______,装置C处最好采用的加热方式是_______,装置D的作用为_______。
(3)反应装置的虚线框中未画出的仪器最好选用_______(填“甲”或“乙”)。反应结束后应采用_______(填操作名称)提纯产品。
(4)用与混合加热可得无水,其反应化学方程式为_______。小王同学认为和混合加热可制得无水,但小张同学认为该实验可能发生副反应使产品不纯。小张同学设计如下实验判断副反应可能性:取少量于试管中,加入足量,充分反应后向试管中加水溶解,用四支试管各取溶解后的溶液少许,分别进行下列实验,通过现象能验证发生副反应的是_______(填标号)。
a.滴加酸性溶液 b.滴加溶液
c.滴加溶液 d.滴加溴水
19. 钇(Y)是稀土元素中含量丰富的元素之一,钇及其化合物在航天、电子、超导等方面有着广泛的应用。湖北应山-大悟地区含有较为丰富硅铍钇矿[],工业上通过如下生产流程可获得氧化钇。
已知:元素与元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
(1)在自然界中,钇只有一种稳定同位素,Y位于元素周期表的第_______周期第ⅢB族。硅铍钇矿[]中Y的化合价为+3价,的化合价为_______。
(2)焙烧目的是将矿石中的Y元素转化为,并将元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是_______。硅铍钇矿与熔融氢氧化钠焙烧后含铁元素的产物是_______(写化学式)。
(3)“萃取分液”实验需要的玻璃仪器有_______。
(4)滤液Ⅱ中的_______(填物质名称)可参与循环使用。
(5)反应过程中,测得Y的沉淀率随的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是_______。
(6)“焙烧”过程生成的化学方程式为_______。
湖北省宜城一中、枣阳一中等六校联考2022-2023学年
高三上学期期中考试化学试题
时限:75(分钟) 分值:100(分)
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写在试卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷、草稿纸和答题卡上的非答题区域均无效。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5 Fe 56
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
【1题答案】
【答案】B
【2题答案】
【答案】D
【3题答案】
【答案】A
【4题答案】
【答案】C
【5题答案】
【答案】D
【6题答案】
【答案】B
【7题答案】
【答案】D
【8题答案】
【答案】B
【9题答案】
【答案】A
【10题答案】
【答案】B
【11题答案】
【答案】C
【12题答案】
【答案】C
【13题答案】
【答案】B
【14题答案】
【答案】C
【15题答案】
【答案】D
二、非选择题:本题共4小题,共55分。
【16题答案】
【答案】(1) ①. 4 ②. 0.04 ③. 圆底烧瓶、分液漏斗 ④. ClO-+Cl-+2H+=Cl2+H2O
(2) ①. 稀释产生的ClO2,防止其分解爆炸 ②. 2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2↑ ③. 38°C~60°C
【17题答案】
【答案】(1) (2)ac
(3)
(4) ①. 离子键和共价键 ②. 碱性
(5) ①. 碱性、还原性 ②. 1 ③. S、N
【18题答案】
【答案】(1)
(2) ①. 饱和食盐水 ②. 水浴加热 ③. 防止空气中水蒸气进入装置C,使产品水解
(3) ①. 乙 ②. 蒸馏
(4) ①. ②. bc
【19题答案】
【答案】(1) ①. 五 ②. +2
(2) ①. 增大反应物的接触面积,提高原料利用率 ②. Fe(OH)3
(3)分液漏斗、烧杯 (4)盐酸
(5)草酸与Y3+离子形成可溶性配位化合物
(6)
2022-2023学年湖北省宜城一中、枣阳一中等六校联考高一上学期期中考试化学试题PDF版含答案: 这是一份2022-2023学年湖北省宜城一中、枣阳一中等六校联考高一上学期期中考试化学试题PDF版含答案,文件包含湖北省宜城一中枣阳一中等六校联考2022-2023学年高一上学期期中考试化学试题pdf、高一化学答案及评分标准pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
2022-2023学年湖北省宜城一中、枣阳一中等六校联考高一上学期期中考试化学试题PDF版含答案: 这是一份2022-2023学年湖北省宜城一中、枣阳一中等六校联考高一上学期期中考试化学试题PDF版含答案,文件包含湖北省宜城一中枣阳一中等六校联考2022-2023学年高一上学期期中考试化学试题pdf、高一化学答案及评分标准pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
2023湖北省宜城一中、枣阳一中等六校联考高三上学期期中考试化学试题含答案、答题卡: 这是一份2023湖北省宜城一中、枣阳一中等六校联考高三上学期期中考试化学试题含答案、答题卡,文件包含湖北省宜城一中枣阳一中等六校联考2022-2023学年高三上学期期中考试化学试题含答案docx、高三联考化学试题答题卡pdf等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。












